La missione di SPA – SOCIETA’ PRODOTTI ANTIBIOTICI S.p.A. è soddisfare nel migliore dei modi le necessità e le aspettative dei pazienti, con prodotti di qualità, in grado di tutelare la salute e migliorare la qualità della vita.
Per essere leader in ognuna delle aree terapeutiche nelle quali operiamo è indispensabile che le nostre attività imprenditoriali siano caratterizzate da standard di professionalità elevati. In questo Codice Etico gli standard di professionalità richiesti sono chiaramente espressi e SPA chiede a tutti i suoi dipendenti di rispettarli ed applicarli.
In quanto organizzazione responsabile sotto il profilo etico, sociale e ambientale, SPA ritiene importante instaurare un rapporto leale con i dipendenti, i collaboratori, i partner commerciali, le autorità ed il pubblico.
Il successo della nostra attività imprenditoriale dipende, infatti, dalla capacità di mantenere la fiducia di tutti coloro che hanno rapporti con la nostra Società: consulenti, fornitori, clienti, agenti, prestatori d’opera, partner commerciali, operatori sanitari, dipendenti ecc. Il Codice Etico, approvato dal Consiglio di Amministrazione in data 30 settembre 2021, svolge un ruolo fondamentale nel creare e mantenere questa fiducia.
Società Prodotti Antibiotici S.p.A.
CODICE ETICO
0. Premessa: scopo e ambito di applicazione del Codice Etico 1. Diffusione. 2. Il rispetto della legalità. 3. Regole di condotta nella selezione e nell’assunzione del personale e nell’esecuzione del rapporto di lavoro con dipendenti e collaboratori. 4. L’ambiente di lavoro. 5. I principi in materia di sicurezza e salute dei lavoratori. 6. Il conflitto di interessi. 7. L’utilizzo dei beni aziendali 8. La tutela della segretezza delle informazioni. 9. La tutela della proprietà intellettuale.10. La tutela della privacy. 11. Il riciclaggio, l’auto riciclaggio, la ricettazione e l’impiego di capitali illeciti e le caratteristiche delle operazioni contabili e delle transazioni economico/finanziarie. 12. La trasparenza verso il mercato. 13. I rapporti con la Pubblica Amministrazione. 14. I rapporti con il mercato ed i clienti. 15. I rapporti con i fornitori. 16. I rapporti con operatori sanitari e società scientifiche. 17.I rapporti con le Autorità di Vigilanza; 18. La tutela ambientale; 19. L’efficacia del Codice Etico e le conseguenze sanzionatorie. 20. Disposizioni finali.
* * *
0. Premessa: scopo e ambito di applicazione del Codice Etico.
Il presente Codice Etico (di seguito anche semplicemente “il Codice”) è volto a descrivere i principi ed i valori che costituiscono il fondamento dell’attività economica di Società Prodotti Antibiotici S.p.A., orientandola al rispetto di rigorosi standard etici e deontologici.
In considerazione della sua importanza, tale documento è portato a conoscenza di tutti i soggetti che prestano la propria attività lavorativa all’interno di Società Prodotti Antibiotici S.p.A., dovendo essere conosciuto e rispettato anche da coloro che collaborano a qualsivoglia titolo con la medesima.
Il Codice è ispirato al Codice Deontologico di Farmindustria — Associazione Nazionale Dell’industria Farmaceutica — alla quale Società Prodotti Antibiotici S.p.A. aderisce, nonché a quanto previsto dalle Linee Guida di Farmindustria per la certificazione delle procedure relative all’attività di informazione scientifica.
Il Codice Etico rappresenta un elemento essenziale per garantire il successo imprenditoriale della società, che fa della correttezza e della trasparenza la base della propria reputazione commerciale. La comprensione ed il rispetto dei valori fondanti su cui si basa l’operato di Società Prodotti Antibiotici S.p.A. rappresentano infatti un punto di riferimento essenziale nella gestione dei rapporti interni ed esterni, in cui il profitto o l’interesse economico non può mai giustificare una condotta contraria ai principi di integrità, correttezza, onestà, buona fede e trasparenza, oltre che alle leggi ed ai regolamenti vigenti.
Società Prodotti Antibiotici S.p.A. vuole continuare a meritare la fiducia di tutti i suoi interlocutori, impegnandosi a comprendere a fondo le loro esigenze e offrendo la disponibilità a lavorare per uno sviluppo duraturo dei rapporti di collaborazione.
Le norme contenute nel presente Codice Etico hanno come destinatari:
- i soggetti in posizione apicale di Società Prodotti Antibiotici S.p.A., laddove per “apicali” debbono intendersi tutti coloro che rivestono – anche di fatto – funzioni di rappresentanza, di amministrazione o di direzione della Società ovvero di una sua unità organizzativa dotata di autonomia finanziaria e funzionale;
- tutte le persone sottoposte alla direzione o alla vigilanza dei predetti soggetti che siano dipendenti di Società Prodotti Antibiotici S.p.A.;
- tutti i soggetti che, senza essere dipendenti di Società Prodotti Antibiotici S.p.A., collaborano a qualsivoglia titolo con la medesima, svolgono attività presso, per conto o nell’interesse di tale Società, intrattengono con essa rapporti commerciali, ricevono dalla stessa incarichi o hanno con essa rapporti durevoli (consulenti, fornitori, clienti, agenti, prestatori d’opera, partner commerciali, operatori sanitari, dipendenti ecc.).
Tali soggetti (di seguito semplicemente “i destinatari”) devono rispettare e a dare piena applicazione alle norme contenute nel Codice Etico per tutto il periodo di tempo in cui prestano la loro attività lavorativa alle dipendenze di Società Prodotti Antibiotici S.p.A. o collaborano (nel senso ampio sopra descritto) con essa.
Coloro che hanno il compito di decidere la politica aziendale nonché di amministrare e gestire sotto tutti i punti di vista la Società devono inoltre ispirare ogni scelta decisionale ai principi ed alle regole contenute nel presente documento.
- Diffusione.
Il Codice Etico è portato a conoscenza dei destinatari mediante apposite ed idonee attività di comunicazione e/o formazione. Esso costituisce parte integrante e sostanziale del contratto di lavoro di ogni dipendente o dirigente di Società Prodotti Antibiotici S.p.A. e verrà consegnato – in versione integrale o riassuntiva – ad ogni nuovo assunto.
Ogni nuovo assunto o dipendente/dirigente/collaboratore della Società deve leggere e sottoscrivere un documento con il quale si impegna ad osservare le prescrizioni contenute nel presente Codice Etico.
L’osservanza del Codice Etico costituisce, per tutti i prestatori di lavoro, ai sensi dell’art. 2104 c.c., un obbligo contrattuale, la cui violazione integra un inadempimento grave alle obbligazioni derivanti dal contratto di lavoro e fonte di illecito civile, con ogni conseguente responsabilità personale.
La Società si riserva inoltre di tutelare i propri interessi in ogni sede competente nei confronti dei terzi collaboratori, clienti e/o partner commerciali, che abbiano violato le norme del Codice Etico, il cui rispetto deve sempre formare oggetto di specifica pattuizione contrattuale con la Società.
I destinatari hanno inoltre l’obbligo di riferire al proprio superiore gerarchico tutte le condotte contrastanti con le disposizioni ed i principi contenuti nel Codice Etico posti in essere da dipendenti o collaboratori (nel senso ampio sopra descritto) di Società Prodotti Antibiotici S.p.A., collaborando nel corso dell’istruttoria finalizzata a valutare la fondatezza di quanto segnalato.
Il segnalante non potrà subire alcuna ritorsione, discriminazione (diretta o indiretta) o altra conseguenza negativa quale effetto della segnalazione o per motivi indirettamente collegati alla stessa, a meno che non abbia effettuato la segnalazione con dolo o colpa grave. In particolare, il licenziamento o demansionamento ritorsivo o discriminatorio del soggetto segnalante è nullo.
- Il rispetto della legalità.
Il rispetto della legalità è un requisito inderogabile per Società Prodotti Antibiotici S.p.A. e per tutti i suoi dirigenti, dipendenti e/o collaboratori, che, nello svolgimento della propria attività, sono tenuti ad uniformarsi allo statuto, alle leggi ed ai regolamenti vigenti in tutti i Paesi in cui la stessa opera o dovesse trovarsi ad operare.
Ognuno dei predetti soggetti, debitamente preparato e formato attraverso i training o i corsi organizzati dalla società, deve essere a conoscenza delle norme di legge che disciplinano l’attività di sua competenza.
Laddove vi possa essere un apparente conflitto tra le norme di diligenza professionale e disposizioni di legge, e comunque in caso di difficile interpretazione e applicazione della legge, il lavoratore dovrà astenersi dallo svolgere qualsiasi attività e dovrà chiedere gli opportuni chiarimenti al proprio superiore gerarchico, il quale fornirà al richiedente tempestive indicazioni.
- Le Persone di SPA. Condotta nella selezione e nell’assunzione del personale e nell’esecuzione del rapporto di lavoro.
Il contributo avuto dalle proprie Persone ha consentito all’Azienda di creare valore e di conquistare la fiducia dei pazienti, dei medici, delle Istituzioni e di tutti altri interlocutori.
La SPA si riconosce nei principi stabiliti dalla Dichiarazione Universale dei Diritti dell’Uomo e dall’International Labour Organization, si attiene ai dettami delle normative in materia di diritto del lavoro.
SPA vuole che la capacità di rispettare ed ascoltare le Persone sia un fattore distintivo e si sforza di offrire disponibilità e solidarietà affinché la crescita dell’Azienda costruisca opportunità per il futuro di chi ci lavora. Per questo motivo, l’Azienda chiede a chi occupa posizioni di responsabilità su funzioni organizzative o anche solo su specifiche attività, di svolgere il proprio ruolo con obiettività, equilibrio e rispetto dei diritti della persona.
La valutazione e selezione del personale da assumere è effettuata nel rispetto delle pari opportunità di lavoro, senza discriminazione di sesso, età, razza, lingua, religione, opinioni politiche e sindacali o condizioni personali e sociali.
Le informazioni richieste al lavoratore sono esclusivamente quelle rilevanti ai fini della valutazione dell’attitudine professionale dello stesso, nel rispetto della normativa sulla privacy e delle opinioni personali del lavoratore.
La Società vieta fermamente qualunque atto di favoritismo, nepotismo, discriminazione o clientelismo in qualunque ambito della vita sociale (selezione del personale – per esempio, evitando che il selezionatore sia legato da vincoli di parentela con il candidato – promozioni, premi, ecc.).
È fatto assoluto divieto di sollecitare o accettare promesse o versamenti di denaro ovvero prestazioni di alcun tipo, che possano essere finalizzati all’assunzione, al trasferimento ovvero alla promozione di un lavoratore.
I lavoratori sono assunti con regolare contratto di lavoro, conformemente alle norme di legge ed ai contratti collettivi nazionali di lavoro applicabili. È obiettivo della Società far sì che ciascun dipendente e/o collaboratore non subordinato, nell’ambito delle sue mansioni, riceva una formazione idonea ad evitare i possibili rischi per la salute e la sicurezza derivanti dall’attività lavorativa ed a garantire il miglioramento progressivo delle conoscenze e delle competenze.
Compatibilmente con l’efficienza generale del lavoro, verranno favorite quelle flessibilità nell’organizzazione del lavoro che agevolino la gestione dello stato di maternità e in generale della cura dei figli.
- L’ambiente di lavoro.
Società Prodotti Antibiotici S.p.A. si impegna a valorizzare le competenze professionali dei propri collaboratori, fornendo agli stessi adeguati strumenti di formazione e aggiornamento professionale e pari opportunità di sviluppo.
A tal fine la Società si impegna a tutelare il diritto dei lavoratori e delle lavoratrici a vivere in un ambiente di lavoro sereno in cui i rapporti interpersonali siano improntati alla correttezza e al reciproco rispetto della libertà e dignità della persona.
Si impegna altresì a rimuovere ogni ostacolo all’attuazione di questi diritti, in modo da garantire il rispetto dell’inviolabilità della persona umana, e da tutelare tutti coloro che operano all’interno di Società Prodotti Antibiotici S.p.A. da qualsiasi atto o comportamento che produca effetto pregiudizievole nei rapporti interpersonali e che discrimini, anche in via indiretta, in ragione di sesso, età, razza, lingua, religione, opinioni politiche e sindacali o condizioni personali e sociali.
I responsabili delle Direzioni e delle funzioni aziendali hanno il dovere di prevenire il verificarsi di discriminazioni e di ogni atto lesivo della dignità della persona, intervenendo tempestivamente qualora vengano riscontrate condotte contrarie ai detti principi.
- I principi in materia di sicurezza e salute dei lavoratori.
Fermo restando che l’azienda non ha sedi produttive proprie, disponendo unicamente di uffici amministrativi e di due magazzini dove vengono stoccati e/o distribuiti i prodotti aziendali, Società Prodotti Antibiotici S.p.A. promuove e protegge la salute e la sicurezza dei propri lavoratori che rappresenta un cardine essenziale ed imprescindibile del proprio modello di business.
A tal fine, la Società, quale datore di lavoro, nonché il Responsabile del Servizio di Prevenzione e Protezione e le atre figure previste dal D.l.gs 81/08 – per quanto di loro competenza – hanno l’obbligo:
- di adempiere a tutti gli obblighi originariamente introdotti dal D. Lgs. 626/1994, ed ora contenuti nel D. Lgs. n. 81 del 9 aprile 2008;
- di rispettare ed osservare tutte le norme poste a tutela della salute e della sicurezza sui luoghi di lavoro, promuovendo altresì le condotte responsabili da parte di tutti i dipendenti e/o collaboratori;
- di adottare uno o più Documenti di Valutazione dei Rischi (c.d. DVR) o, in presenza di rischi interferenziali, di adottare un Documento di Valutazione dei Rischi Interferenziali (c.d. DUVRI);
- di garantire una corretta formazione di tutti i dipendenti che prestano la loro attività a favore di Società Prodotti Antibiotici S.p.A.;
- di fornire i dispositivi di protezione individuale e tutta la strumentazione idonea a svolgere le attività in piena sicurezza, garantendone la corretta manutenzione e ricambio;
- di pretendere il rispetto della normativa in tema di salute e sicurezza sul lavoro anche da parte delle imprese cui venga eventualmente affidata l’esecuzione di date attività e/o lavori.
I dipendenti e/o collaboratori, a loro volta, devono rispettare gli obblighi previsti nella normativa sopra richiamata, contribuendo all’adempimento di tutti gli obblighi imposti dalla legge o dall’autorità competente. In presenza di anomalie, irregolarità o violazioni delle procedure/istruzioni operative interne o delle disposizioni del D.Lgs. 81/08, gli stessi debbono effettuare le debite segnalazioni al Responsabile del Servizio di Prevenzione e Protezione dei rischi (RSPP). A tale organo occorrerà rivolgersi anche in presenza di dubbi interpretativi circa la normativa applicabile, situazione in cui le lavorazioni debbono essere sempre sospese.
- Il conflitto di interessi.
I destinatari, nell’esecuzione delle prestazioni loro assegnate e nell’esercizio dei compiti di rispettiva competenza, devono perseguire l’interesse primario della Società, fermo restando il rigoroso rispetto della legge e delle norme e dei principi fissati nel presente Codice.
Essi dovranno inoltre evitare situazioni che possano creare conflitti di interesse sia reale, sia potenziale tra attività personali e aziendali. Per conflitto di interesse si intende la situazione nella quale il soggetto apicale, il dipendente o il collaboratore, in relazione ad una determinata operazione, abbia (anche solo potenzialmente), per conto proprio o di terzi, un interesse in conflitto con quello della Società.
A titolo meramente esemplificativo, integrano un conflitto di interessi:
- la cointeressenza – a qualsiasi titolo, palese od occulta – di un destinatario o di suoi familiari in attività di fornitori, clienti, concorrenti;
- lo svolgimento di attività lavorative di qualunque tipo presso clienti, fornitori, concorrenti o presso terzi in contrasto con gli interessi della Società;
- la stipulazione di contratti o l’avvio di trattative per conto della Società, che abbiano come controparte familiari o soci del dipendente, ovvero soggetti in qualunque modo allo stesso riconducibili;
- in generale la strumentalizzazione della propria posizione all’interno della Società per la realizzazione di interessi contrastanti con quelli della Società.
Nel caso in cui si verifichi una situazione, anche solo potenziale, di conflitto di interessi, il dipendente o collaboratore coinvolto deve immediatamente darne comunicazione al proprio superiore gerarchico, il quale individuerà le misure necessarie a far cessare tale situazione e, ove vi sia una possibile violazione delle disposizioni del presente Codice Etico, della normativa interna o di disposizioni di legge, valuterà, unitamente alla competente funzione aziendale, l’eventualità di procedere all’instaurazione di un procedimento disciplinare.
- L’utilizzo dei beni aziendali.
Ogni destinatario è tenuto ad operare con la diligenza dovuta per tutelare le risorse aziendali, attraverso comportamenti responsabili ed in linea con le procedure e le istruzioni operative aziendali predisposte per regolamentarne l’utilizzo.
In particolare, ogni destinatario deve utilizzare con scrupolo le risorse a lui affidate o di cui abbia la responsabilità, evitando utilizzi impropri che possano essere di danno o, comunque, in contrasto con l’interesse dell’azienda o con le normative vigenti.
- La tutela della segretezza delle informazioni.
I destinatari che vengono a conoscenza di informazioni riservate inerenti Società Prodotti Antibiotici S.p.A. o ulteriori società con le quali la stessa si rapporti nello svolgimento della propria attività commerciale, hanno il divieto di rivelarle a persone non autorizzate, sia all’interno, sia all’esterno dell’azienda.
Per informazioni riservate si intendono, a titolo esemplificativo e non esaustivo:
- le informazioni tecniche relative a prodotti e procedure;
- i programmi d’acquisto;
- le strategie di costi, dei prezzi, di marketing o di servizi;
- relazioni di carattere finanziario non pubbliche;
- informazioni relative a vendite, fusioni ed acquisizioni;
- ogni altra informazione inerente il c.d. “know how” tecnico-scientifico” e “know how” commerciale e industriale della Società.
Ogni comunicazione all’esterno di documenti e informazioni riguardanti la Società dovrà comunque avvenire nel rispetto delle leggi, dei regolamenti e delle pratiche di condotta professionale vigenti, e dovrà essere realizzata con chiarezza, trasparenza, completezza e tempestività.
- La tutela della proprietà intellettuale.
Società Prodotti Antibiotici S.p.A. promuove le attività di ricerca e innovazione da parte dei propri dipendenti, ciascuno nell’ambito delle funzioni e responsabilità ricoperte, assicurando il rispetto delle norme interne, comunitarie e internazionali poste a tutela della proprietà industriale e intellettuale.
Le informazioni relative ad attività di ricerca in ambito scientifico e tecnologico possono essere scambiate, con università, istituti di ricerca pubblici e privati, enti ospedalieri, dopo che siano stati approntati gli strumenti di tutela della proprietà industriale, in conformità alle procedure aziendali ed apprestando gli opportuni mezzi di tutela della confidenzialità.
In ogni caso, tutti i destinatari sono tenuti ad assicurare la riservatezza di tutto ciò che costituisce la proprietà industriale ed intellettuale della Società, ivi incluse le informazioni tecniche, documentazioni contrattuali, know-how (comprese informazioni, conoscenze e dati acquisiti o elaborati durante lo svolgimento delle proprie mansioni), brevetti, marchi.
Allo stesso modo, devono rispettare i legittimi diritti di proprietà industriale ed intellettuale di terzi, astenendosi dall’uso non autorizzato di tali diritti.
- La tutela della privacy.
La Società assicura la riservatezza dei dati personali e sensibili in proprio possesso, nel rispetto delle regole poste dalla normativa vigente ed in particolare dal Regolamento UE 2016/679 (GDPR) e dal D.Lgs. 196/03, così come modificato dal D.L. 14 giugno 2019, n. 53, dal D.M. 15 marzo 2019 e dal D.Lgs 10 agosto 2018, n. 101.
Viene garantita, in particolare, la tutela di tutti i dati, sensibili e non, che riguardino tutti i soggetti che lavorino alle dipendenze di Società Prodotti Antibiotici S.p.A., i terzi fornitori, i partner commerciali e gli ulteriori operatori con cui la Società abbia dei rapporti economico/commerciali. Viene infine garantita, secondo le norme vigenti in materia, la privacy dei clienti, i cui dati personali, economici e di consumo non possono essere comunicati o diffusi, salvi gli obblighi di legge.
A tal fine, è fatto divieto di comunicare e/o diffondere informazioni personali senza previo consenso dell’interessato, ad esclusione dei casi in cui ciò è consentito o imposto dalla legge.
- Il riciclaggio, l’autoriciclaggio, la ricettazione e l’impiego di capitali illeciti: le caratteristiche delle operazioni e delle transazioni, e gli altri adempimenti in materia contabile.
La Società persegue l’obiettivo di condurre affari esclusivamente con clienti, consulenti e controparti commerciali di comprovata buona reputazione, che svolgano la propria attività nel pieno rispetto della normativa applicabile e le cui capacità finanziarie siano di provenienza lecita.
E’ pertanto assolutamente vietato acquistare, ricevere, occultare o impiegare in qualunque modo beni la cui provenienza delittuosa sia nota ovvero sia desumibile sulla base di indizi di gravità ed univocità tale da autorizzarne tale logica conclusione. Rispetto a tali beni è inoltre vietato compiere qualsiasi operazione potenzialmente idonea ad ostacolarne la provenienza illecita.
I destinatari che nutrano sospetti in ordine alla legittima provenienza di denaro o altri beni acquistati, ricevuti, impiegati o pervenuti a qualsiasi titolo in Società, ovvero abbiano notizia di possibili operazioni di riciclaggio, devono segnalarlo immediatamente al superiore gerarchico, il quale dovrà informare tempestivamente il Consiglio di Amministrazione della Società nonché darne comunicazione mediante i canali appositamente dedicati all’Organismo di Vigilanza eventualmente insediato.
I destinatari devono, inoltre, osservare scrupolosamente tutte le disposizioni e procedure previste in materia di contabilità, gestione delle casse, registrazione e reporting finanziario applicabili ai flussi monetari e ai pagamenti connessi con transazioni e contratti.
Con riguardo a tutte queste attività, Società Prodotti Antibiotici S.p.A. assicura il rispetto dei principi di trasparenza e tracciabilità.
Ogni operazione o transazione viene correttamente registrata nel sistema di contabilità aziendale secondo i criteri indicati dalla legge e dai principi contabili, e deve essere debitamente autorizzata, verificabile, legittima, coerente e congrua. A tal fine, debbono essere utilizzati strumenti di pagamento che assicurino la piena tracciabilità e trasparenza delle operazioni effettuate.
Per ogni operazione deve esservi un adeguato supporto documentale idoneo a consentire, in ogni momento, l’effettuazione di controlli in grado di attestare le caratteristiche e le motivazioni dell’operazione contabile e la verifica del processo di decisione, di autorizzazione e di realizzazione, nonché l’individuazione dei soggetti che hanno rispettivamente autorizzato, effettuato, registrato e verificato l’operazione stessa.
A tal fine la documentazione di supporto deve essere in ogni momento facilmente reperibile ed ordinata secondo criteri logici.
Ciascun dipendente e collaboratore è tenuto a collaborare – nell’ambito delle rispettive funzioni – affinché qualsiasi fatto relativo alla gestione della Società sia correttamente e tempestivamente registrato nella contabilità della Società.
I destinatari che vengano a conoscenza di irregolarità, omissioni, falsificazioni o in generale di violazioni del presente Codice nelle registrazioni contabili devono darne immediata comunicazione al superiore gerarchico, il quale dovrà informare tempestivamente il Consiglio di Amministrazione della Società nonché darne comunicazione mediante i canali appositamente dedicati all’Organismo di Vigilanza eventualmente insediato.
- La trasparenza verso il mercato.
La Società persegue la propria missione assicurando, nel contempo, piena trasparenza nelle scelte effettuate; adotta presidi idonei a garantire la correttezza e veridicità delle comunicazioni sociali (bilanci, relazioni periodiche, prospetti informativi, ecc.) e ad impedire la commissione dei reati societari, quali falso in bilancio, false comunicazioni sociali.
La redazione dei documenti contabili societari, delle relazioni e della altre comunicazioni sociali previste dalla legge, dirette ai soci o al pubblico, ovvero comunque di tutti i documenti elaborati e le comunicazioni emesse dalla Società, viene realizzata nel rispetto della legge e dei regolamenti vigenti, con l’osservanza delle prassi e dei principi contabili più avanzati, mediante la rappresentazione chiara e fedele di tutti i fatti relativi alla gestione economica, patrimoniale e finanziaria.
- I rapporti con la Pubblica Amministrazione.
Integrità, correttezza e trasparenza sono i valori che devono essere rispettati dai destinatari in tutti i rapporti, all’interno ed all’esterno dell’azienda.
I rapporti con la Pubblica Amministrazione, pubblici ufficiali o soggetti incaricati di pubblico servizio, ed in generale con tutti i soggetti pubblici devono caratterizzarsi per la rigorosa osservanza delle disposizioni di legge e regolamentari applicabili e devono uniformarsi a principi di diligenza, trasparenza ed onestà.
Tali rapporti possono essere tenuti esclusivamente dalle funzioni aziendali a ciò preposte e dal personale a ciò autorizzato, e devono essere analiticamente ricostruiti in apposita documentazione, che deve essere custodita con cura così da poter essere messa a disposizioni delle Autorità per il caso di eventuali controlli.
È proibito concedere, offrire o promettere denaro, doni o regalie di ogni tipo a dirigenti, funzionari o dipendenti della Pubblica Amministrazione o a loro parenti per compensare o ripagare gli stessi di un atto del loro ufficio ovvero per ottenere il compimento di un atto contrario ai doveri del loro ufficio. Il divieto si applica anche a regalie di modico valore.
In quei paesi dove è nel costume offrire doni a clienti od altri, è possibile agire in tal senso quando questi doni siano di natura appropriata e di valore modico, ma sempre nel rispetto delle leggi. Ciò non deve comunque mai essere interpretato come una ricerca di favori.
Sono assolutamente vietate, nel corso di gare, procedure, trattative o in qualunque tipo di rapporto commerciale con la Pubblica Amministrazione le seguenti azioni (dirette o indirette):
- esaminare o proporre opportunità di impiego e/o commerciali a favore del dipendente della P.A. che rappresenta la P.A. nella trattativa in corso, di suoi familiari o di persone a quello comunque riconducibili;
- offrire o fornire omaggi di qualunque tipo;
- sollecitare o ottenere informazioni riservate che possano compromettere la correttezza della gara e/o procedura o l’integrità o la reputazione di entrambe le parti;
- influenzare impropriamente le decisioni della controparte.
Non è consentito destinare a finalità diverse da quelle per cui sono stati concessi contributi, sovvenzioni o finanziamenti ottenuti dallo Stato o da altro ente pubblico. È fatto assoluto divieto di servirsi di artifici, raggiri, dazioni e/o promesse di denaro o altra utilità per ottenerli.
Se la Società si avvale di un consulente o di un soggetto terzo per essere rappresentata nei rapporti verso la Pubblica Amministrazione, nei confronti di tale soggetto si applicano le stesse direttive impartite ai dipendenti o dirigenti della Società. Società Prodotti Antibiotici S.p.A. non dovrà farsi rappresentare nei rapporti con la Pubblica Amministrazione da un soggetto terzo quando si possano creare conflitti d’interesse.
In occasione di ispezioni da parte di Autorità Pubbliche (es. Ministero della Salute, AIFA, ASL, INPS, NAS, Ispettorato del Lavoro, Guardia di Finanza, Vigili del Fuoco, Agenzia delle Entrate, ecc.) all’interno dei locali in uso a Società Prodotti Antibiotici S.p.A., la Società dovrà assicurare il tempestivo ed integrale riscontro delle richieste effettuate, mettere a disposizione (laddove necessario) idonei locali per consentire ai pubblici funzionari lo svolgimento dei compiti loro demandati e fornire tutte i chiarimenti o approfondimenti ritenuti necessari.
E’ in ogni caso proibito in modo assoluto ostacolare il regolare svolgimento dell’attività di verifica attraverso occultamento o distruzione di documentazione.
A fine di agevolare le visite ispettive, debbono essere identificati due dipendenti o dirigenti di Società Prodotti Antibiotici S.p.A. che avranno il compito di rapportarsi con l’Autorità presente in azienda.
Qualsiasi violazione (effettiva o potenziale) commessa dall’ente o da terzi va segnalata tempestivamente al superiore gerarchico, il quale dovrà informare immediatamente il Consiglio di Amministrazione della Società nonché darne comunicazione mediante i canali appositamente dedicati all’Organismo di Vigilanza eventualmente insediato.
- I rapporti con il mercato ed i clienti.
La Società garantisce al mercato, agli investitori ed alla comunità in genere, una completa trasparenza nella propria attività. Essa inoltre si impegna a promuovere una competizione leale e corretta, considerata quale elemento finalizzato al raggiungimento anche dei propri interessi, oltre che di quelli dei clienti, degli operatori del mercato e di tutti coloro che vengono direttamente o indirettamente in contatto con l’attività della stessa (quali i dipendenti, i clienti, i consumatori, i fornitori, i finanziatori, ecc.).
Vengono pertanto evitati:
- coinvolgimenti in operazioni di divisione dei mercati con altri concorrenti ed altre condotte finalizzate a limitare la produzione e la vendita, in violazione dei principi della libera concorrenza;
- condotte diffamatorie nei confronti di concorrenti attraverso l’utilizzo di espedienti commerciali o attività di marketing finalizzate a gettare discredito sull’affidabilità e la competenza dei competitors;
- accordi con gli altri operatori del mercato volti ad uniformare le condizioni contrattuali applicate ai clienti e ad uniformare il prezzo dei servizi o prodotti.
I rapporti contrattuali con i clienti sono improntati a principi di correttezza ed onestà, professionalità, trasparenza e, comunque, contraddistinti dalla massima collaborazione da parte della Società. In particolare, tutti i rapporti con i clienti (comunicazioni, contratti, informazioni pubblicitarie), oltre a rispettare tutte le normative vigenti ed il principio della buona fede nei rapporti contrattuale, dovranno presentare le seguenti caratteristiche:
- l’utilizzo di un linguaggio chiaro e comprensibile;
- la descrizione di tutte le circostanze che possano rilevare ai fini della sottoscrizione del contratto;
- la prospettazione delle condizioni dei servizi offerti, con una trasparente indicazione dei costi che dovranno essere sostenuti;
- ogni variazione del contratto dovrà essere tempestivamente comunicata al cliente.
- I rapporti con i fornitori.
La selezione dei fornitori e la determinazione delle condizioni d’acquisto sono basate su una valutazione obiettiva dal sistema di gestione qualità e sulle certificazioni conseguite dai fornitori, sulla qualità ed il prezzo del bene o servizio, nonché delle garanzie di assistenza e di tempestività.
In particolare, i destinatari adibiti alla funzione di selezione e di gestione dei rapporti con i fornitori, appartenenti alla Divisione “Supply Chain”, dovranno rispettare i seguenti principi:
- rispettare le norme di legge, le procedure e/o le istruzioni operative interne nonché gli obblighi derivanti da contratto;
- conformare l’attività di selezione al principio di imparzialità, garantendo pari opportunità ai candidati e finalizzando le proprie scelte all’interesse della Società (sempre nel rispetto della legge);
- utilizzare criteri di scelta pubblici ed obbiettivi (qualità del servizio, prezzo, integrità, tempestività nella consegna, disponibilità di mezzi e strutture, competenze, ecc.);
- denunciare situazioni di conflitto di interesse, anche potenziali, che possano indebitamente influire sulla selezione di un fornitore;
- rispettare sempre il principio di buona fede nei rapporti contrattuali con i fornitori;
- effettuare un’attività di monitoraggio e verifica sulla persistenza dei requisiti di legge e delle certificazioni in materia ambientale e/o di salute e sicurezza sul lavoro.
Oltre ai prodotti offerti dai fornitori dovrà essere oggetto di valutazione anche la condivisione dei valori descritti nel presente Codice Etico da parte dei singoli fornitori, ed al riguardo sarà rilevante anche l’accettazione da parte di questi ultimi delle specifiche clausole contrattuali di adesione ai principi riportati nel presente codice etico.
- Attività pubblicitarie e rapporti con il mondo scientifico, sanitario e con le associazioni dei pazienti.
SPA Società Prodotti Antibiotici S.p.A. attua le attività pubblicitarie relative ai farmaci commercializzati in conformità ai requisiti previsti dalla normativa vigente.
In particolare, nell’attuazione delle attività promozionali rivolte agli operatori sanitari, SPA Società Prodotti Antibiotici S.p.A. rispetta e recepisce nelle procedure aziendali i requisiti di legge e le prescrizioni del Codice Deontologico di Farmindustria.
Nel quadro dell’attività di informazione e presentazione dei medicinali svolta presso medici o farmacisti è vietato concedere, offrire o promettere premi, vantaggi pecuniari o in natura, salvo che siano di valore trascurabile e comunque collegabili all’attività espletata dal medico o dal farmacista.
SPA Società Prodotti Antibiotici S.p.A. può intrattenere rapporti di collaborazione con medici, Società Scientifiche, Associazioni mediche e Associazioni di Pazienti purché vengano sempre rispettati i relativi requisiti previsti dal Codice Deontologico.
Nell’ambito della pubblicità su giornali e riviste, occorre garantire la netta separazione tra informazione e pubblicità, assicurando sempre al lettore l’immediata riconoscibilità del messaggio promozionale, in qualunque sua forma (redazionale o tabellare).
Società Prodotti Antibiotici S.p.A. potrà intrattenere rapporti di collaborazione con le Società scientifiche e le Associazioni mediche, purché ispirati alla divulgazione della conoscenza scientifica ed al miglioramento della conoscenza professionale, e svolti in collaborazione con enti di provata affidabilità e di levatura nazionale, di cui sia ben nota la missione.
È infine cura della Società rispettare l’indipendenza delle associazioni di pazienti e stabilire con esse rapporti integri e trasparenti.
- I rapporti con le Autorità di Vigilanza.
Società Prodotti Antibiotici S.p.A. rispetta scrupolosamente le regole antitrust e quelle dettate dagli organi regolatori del mercato (ad esempio, l’Autorità Garante della Concorrenza e del Mercato, l’Autorità Garante per la Protezione dei Dati Personali, etc.).
Nei confronti delle autorità di vigilanza competenti, le informazioni devono essere presentate solo dai dipendenti specificamente incaricati dalla Società. I dipendenti, nell’ambito delle rispettive competenze, hanno l’obbligo di collaborare con tali autorità e di rispondere con correttezza e tempestività ad ogni loro richiesta.
- La tutela ambientale.
Società Prodotti Antibiotici S.p.A., considerando l’ambiente un bene primario, orienta le proprie attività al fine di garantire il miglior equilibrio possibile tra iniziative economiche e esigenze ambientali, nel rispetto delle leggi, ma anche in considerazione di un uso sostenibile delle risorse naturali.
Al fine di tutelare l’ambiente in ogni attività aziendale, il Gruppo promuove il ricorso a processi produttivi, tecnologie e materiali che consentano altresì la riduzione dei consumi energetici, evitando o limitando gli impatti derivanti dalle attività aziendali in termini di inquinamento, emissioni in atmosfera, produzione di rifiuti e disagi per la comunità locale.
- L’efficacia del Codice Etico e le conseguenze sanzionatorie.
L’osservanza delle disposizioni del presente Codice Etico deve considerarsi parte essenziale delle obbligazioni contrattuali dei dipendenti della Società ai sensi e per gli effetti degli artt. 2104 e 2105 cod. civ. L’eventuale violazione delle disposizioni del Codice Etico potrà costituire inadempimento delle obbligazioni del rapporto di lavoro e/o illecito disciplinare, in conformità alle procedure previste dall’art. 7 dello Statuto dei Lavoratori, con ogni conseguenza di legge, anche con riguardo alla conservazione del rapporto di lavoro, e potrà comportare il risarcimento dei danni dalla stessa derivanti.
Il rispetto dei principi del presente Codice Etico forma parte essenziale delle obbligazioni contrattuali di coloro che intrattengono rapporti di natura commerciale con la Società. In conseguenza, l’eventuale violazione delle disposizioni ivi contenute potrà costituire inadempimento delle stesse obbligazioni con ogni conseguenza di legge.
- Disposizioni finali.
Il presente Codice Etico è stato adottato con delibera del 30/09/2021 e, da tale data le disposizioni ivi contenute devono essere rispettate da tutti i destinatari.
Al presente codice viene data la più ampia diffusione possibile attraverso la pubblicazione sul sito internet della Società e l’eventuale diffusione tramite affissione sugli albi e le bacheche riservate al personale; ne verrà inoltre consegnata una copia ai neo-assunti, in formato integrale o riassuntivo, ai collaboratori ed ai fornitori abituali.
Ogni variazione e/o integrazione di esso dovrà essere approvata dal Consiglio di Amministrazione di Società Prodotti Antibiotici S.p.A. e comunicata tempestivamente ai destinatari, con le medesime modalità sopra indicate.
Milano, 30/09/2021
Società Prodotti Antibiotici S.p.A.
MODELLO DI ORGANIZZAZIONE, GESTIONE E CONTROLLO EX D.LGS 231/01
PARTE GENERALE
- IL DECRETO LEGISLATIVO 231/01 E LA RESPONSABILITA’ AMMINISTRATIVA DEGLI ENTI DIPENDENTE DA REATO: BREVI CENNI TEORICI.
1.1 La peculiare natura della responsabilità amministrativa derivante da reato;
1.2. I criteri di imputazione oggettivi e soggettivi ed il ruolo centrale del Modello di Organizzazione e Gestione;
1.3. Le sanzioni applicabili all’ente e l’autonomia della responsabilità amministrativa derivante da reato;
- LA STRUTTURA E LE CARATTERISTICHE DI SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A. ED IL MODELLO DI ORGANIZZAZIONE E GESTIONE APPROVATO A LIVELLO AZIENDALE;
2.1. Le caratteristiche di Società Prodotti Antibiotici e la sua struttura;
2.1.1. La storia della Società e l’oggetto sociale della stessa;
2.1.2. L’attuale sistema di amministrazione e controllo;
2.1.3. La struttura organizzativa della società;
2.2. I criteri normativi e paranormativi seguiti per la redazione del presente Modello di Organizzazione e Gestione e la struttura del presente documento;
2.3. Le finalità del Modello di Organizzazione e Gestione ed i destinatari dello stesso;
2.4. Le modalità operative concretamente seguite per la costruzione del Modello di Organizzazione e Gestione;
- IL SISTEMA DI CONTROLLO INTERNO IMPLEMENTATO DA SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A. AL FINE DI GESTIRE I RISCHI CONNESSI ALLO SVOLGIMENTO DELLE ATTIVITÀ AZIENDALI.
3.1. Il sistema di deleghe e procure;
3.2. l’adozione di un Codice Etico;
3.3. la stringente proceduralizzazione dei processi aziendali;
3.4. il conseguimento di certificazioni;
3.5. la predisposizione di diversi livelli di controllo;
- L’ORGANISMO DI VIGILANZA.
4.1. Premessa: i requisiti normativi e paranormativi alla luce delle integrazioni giurisprudenziali;
4.2. L’Organismo di Vigilanza istituito da Società Prodotti Antibiotici S.p.A;
4.3. Il regolamento dell’OdV: rinvio;
- I FLUSSI INFORMATIVI ED I CANALI DI SEGNALAZIONE.
5.1. I flussi informativi in entrata;
5.2. I flussi informativi in uscita;
5.3. Le segnalazioni all’OdV (whistleblowing);
- IL SISTEMA DISCIPLINARE ADOTTATO DA SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A.
6.1. Premessa e principi generali del sistema disciplinare adottato da Società Prodotti Antibiotici S.p.A.;
6.2. Le diverse parti del sistema disciplinare;
6.2.1. le sanzioni applicabili ai dipendenti che non ricoprono ruoli apicali;
6.2.2. le sanzioni applicabili ai soggetti in posizione apicale ed ai soggetti che ricoprono cariche sociali;
6.2.3. Le sanzioni applicabili ai soggetti e/o società terze che collaborano con Società Prodotti Antibiotici S.p.A.;
6.2.4. Brevi cenni sul procedimento disciplinare;
- L’APPROVAZIONE, LA MODIFICA E L’INTEGRAZIONE DEL MODELLO DI ORGANIZZAZIONE E GESTIONE.
- LA DIFFUSIONE DEL MODELLO DI ORGANIZZAZIONE E GESTIONE E LA FORMAZIONE DEL PERSONALE.
CAPITOLO 1: IL DECRETO LEGISLATIVO 231/01 E LA RESPONSABILITA’ AMMINISTRATIVA DEGLI ENTI DIPENDENTE DA REATO: BREVI CENNI TEORICI.
1.1. La peculiare natura della responsabilità amministrativa derivante da reato.
Il D.Lgs. 8 giugno 2001, n. 231 sulla “disciplina della responsabilità amministrativa delle persone giuridiche, delle Società e delle associazioni anche prive di personalità giuridica”, emanato in attuazione della delega al Governo contenuta nella L. 29 settembre 2000, n. 300, ha introdotto per la prima volta nell’ordinamento giuridico italiano la responsabilità amministrativa degli enti per alcune tipologie di reato (c.d. “reati presupposto”) commessi nel suo interesse o a suo vantaggio da soggetti apicali o sottoposti.
Riprendendo le parole della Relazione di accompagnamento ministeriale, l’innovativa responsabilità prevista dal Decreto, fondata su un illecito penale ma nominalmente amministrativa, rappresenta una sorta di tertium genus giuridico che coniuga “i tratti essenziali del sistema penale e di quello amministrativo nel tentativo di contemperare le ragioni dell’efficacia preventiva con quelle, ancor più ineludibili, della massima garanzia». Tale atipica forma di responsabilità è stata ritenuta perfettamente “compatibile con i principi costituzionali di responsabilità per fatto proprio e di colpevolezza”, in quanto fondata su specifici criteri di imputazione soggettivi ed oggettivi che presuppongono una “colpa d’organizzazione” in capo all’ente.
L’illecito amministrativo ascrivibile ai sensi del D.Lgs. 231/01, non coincide dunque con il reato che ne costituisce il presupposto, ma rappresenta “qualcosa di diverso che addirittura lo ricomprende”. In tale prospettiva, ribadita anche dalla nota sentenza della Corte Costituzionale n. 218/14, la condotta illecita posta in essere dai vertici o dai dipendenti della società è soltanto uno degli elementi che compongono l’articolata struttura dell’illecito amministrativo, che rappresenta una fattispecie complessa nella quale, accanto al presupposto della commissione del delitto, confluiscono anche l’elemento della qualifica soggettiva del reo, la sussistenza dell’interesse e del vantaggio in capo all’ente e la mancata predisposizione di presidi organizzativi idonei a prevenire o minimizzare il rischio di commissione dei reati presupposto.
1.2. I criteri di imputazione oggettivi e soggettivi ed il ruolo centrale del Modello di Organizzazione, Gestione e Controllo.
Al fine di garantire che la responsabilità degli enti sia compatibile con il principio costituzionale di colpevolezza e non violi il divieto di responsabilità per fatto “altrui”, il legislatore ha (come detto) stabilito stringenti criteri d’imputazione soggettivi ed oggettivi. In particolare, sotto il profilo oggettivo:
(a) anzitutto, è necessario che il reato appartenga al novero tassativo delle fattispecie elencate (o altrimenti richiamate) dagli artt. 24 e ss. del D. Lgs. 231/01, che, in quanto fondamento della responsabilità amministrativa, sono definiti “reati presupposto”. Sul punto, fermo restando che al presente Modello è allegato l’elenco aggiornato e completo di tutte le fattispecie contemplate dal Legislatore (vedi all.1), le stesse possono sin da ora essere raggruppate nelle seguenti categorie:
- reati dei pubblici ufficiali contro la Pubblica Amministrazione ovvero, più in generale, reati contro il patrimonio della PA (i soli inizialmente introdotti dal decreto legislativo);
- delitti informatici e trattamento illecito di dati (introdotti dalla L. n. 48 del 18 marzo 2008);
- reati associativi (introdotti dalla Legge 16 marzo 2006, n. 146);
- reati in materia di falsità in monete, in carte di pubblico credito e in valori di bollo (introdotti dal D.L. n. 350/2001), nonché in strumenti o segni di riconoscimento (introdotti dall’articolo 17, comma 7, lettera a, n. 4, della legge 23 luglio 2009, n. 99);
- delitti contro l’industria e il commercio (introdotti dall’articolo 17, comma 7, lett. b, della legge 23 luglio 2009, n. 99);
- reati in materia societaria (introdotti dal D.Lgs. n. 61/2002);
- delitti con finalità di terrorismo o di eversione dell’ordine democratico (introdotti dalla L. n. 7/2003);
- delitti relativi alle pratiche di mutilazione degli organi genitali femminili e delitti contro la libertà individuale (rispettivamente introdotti dalla L. 7/2006 e dalla L. n. 228/2003);
- abusi di mercato (introdotti dalla L. 18 aprile 2005, n. 62);
- delitti connessi alla violazione di norme antinfortunistiche e sulla tutela dell’igiene e della salute sul lavoro (introdotti dalla L. 3 agosto 2007, n. 123);
- delitti di ricettazione, riciclaggio, impiego di beni di provenienza delittuosa nonché di autoriciclaggio (introdotti dal D.Lgs. 21 novembre 2007, n. 231 e dalla L. 186/14);
- delitti in materia di violazione del diritto d’autore (introdotti dall’articolo 15, comma 7, lett. c, della legge 23 luglio 2009, n. 99);
- induzione a non rendere dichiarazioni o a rendere dichiarazioni mendaci all’autorità giudiziaria (si tratta dell’unico reato contro l’amministrazione della giustizia, inserito dall’articolo 4, comma 1, della legge 3 agosto 2009, n. 116, come sostituito dall’articolo 2 del D.Lgs. 7 luglio 2011, n. 121);
- reati ambientali (introdotti dall’articolo 2 del D.Lgs. 7 luglio 2011, n. 121 e ampiamente modificati ad opera della L. 68/15);
- reati transnazionali (Legge 16 marzo 2006, n. 146, artt. 3 e 10);
- impiego di cittadini di paesi terzi il cui soggiorno è irregolare (fattispecie inserita dal D.Lgs. 109/12);
- delitti in materia di razzismo e xenofobia (introdotti dall’art. 5, comma 2, della Legge 20 novembre 2017, n. 167),
- frode in competizioni sportive, esercizio abusivo di gioco o di scommessa e giochi d’azzardo esercitati a mezzo di apparecchi vietati (introdotto dalla L. 3 maggio 2019 n. 39);
- delitti tributari (introdotti attraverso il D.L. 124/19 così come convertito dalla L. 157/19 ed ampliati con il D.Lgs. 75/2020);
- reati di contrabbando previsti dal D.P.R. 43/1973 (introdotti con il D.Lgs. 75/2020).
(b) occorre dimostrare la sussistenza di un interesse o un vantaggio dell’ente. In considerazione della particella disgiuntiva utilizzata dal Legislatore, tali criteri di imputazione sono stati interpretati quali alternativi e concorrenti tra loro: in questo senso, “il criterio dell’interesse esprime una valutazione teleologica del reato, apprezzabile “ex ante”, cioè al momento della commissione del fatto e secondo un metro di giudizio marcatamente soggettivo, mentre quello del vantaggio ha una connotazione essenzialmente oggettiva, come tale valutabile “ex post”, sulla base degli effetti concretamente derivati dalla realizzazione dell’illecito” (Cass. pen., SS.UU., 24 aprile 2014, n. 38343).[1]
(c) la commissione del reato presupposto deve essere riconducibile a soggetti che all’interno dell’ente ricoprono una posizione “apicale” (ovvero che rivestono funzioni di rappresentanza, di amministrazione o di direzione dell’ente o di una sua unità organizzativa o che esercitano, anche di fatto, la gestione o il controllo dello stesso) o di persone che sono sottoposte alla direzione o vigilanza di uno dei soggetti in posizione apicale.
È importante sottolineare che, conformemente a quanto stabilito dalla Linee Guida di Confindustria, la responsabilità dell’ente può sussistere anche laddove il dipendente autore dell’illecito abbia concorso nella sua realizzazione con soggetti estranei all’organizzazione dell’ente medesimo.[2]
Sotto il profilo soggettivo, l’elemento caratterizzante di detta nuova forma di responsabilità è costituito dalla previsione di una cd. “colpa di organizzazione”, che – essendo fondata sulla mancata predisposizione di idonei presidi volti a prevenire o minimizzare il rischio di commissione di reati presupposto – si sostanzia, secondo la dottrina, in un “deficit di compliance” che costituisce un’anomala forma “normativa di colpevolezza per omissione organizzativa e gestionale”.
Ai sensi dell’art. 6 del D.Lgs. 231/01, la rimproverabilità per il reato commesso nell’interesse o a vantaggio dell’ente si articola differentemente a seconda che questo sia ascrivibile al soggetto in posizione apicale o al sottoposto.
Nel primo caso (apicali), l’ente non risponde solo se fornisce la prova:
- di avere adottato ed efficacemente attuato, prima della commissione del reato, modelli di organizzazione e gestione idonei a prevenire i reati della specie di quello verificatosi;
- di aver affidato il compito di vigilare sul funzionamento, l’osservanza e l’aggiornamento dei predetti modelli ad un organismo dell’ente stesso dotato di autonomi poteri di iniziativa e di controllo;
- che le persone che hanno commesso il reato hanno eluso fraudolentemente i modelli di organizzazione e di gestione;
- che non vi è stata omessa o insufficiente vigilanza da parte dell’organismo di controllo.
Nel secondo caso (soggetti sottoposti all’altrui direzione e vigilanza), la responsabilità discende dalla inosservanza degli obblighi di vigilanza o direzione, salvo che l’ente abbia, prima della commissione del fatto, adottato ed efficacemente attuato un modello di organizzazione, gestione e controllo idoneo a prevenire reati del tipo di quello verificatosi. Ciò significa, in altri termini, che l’ente è responsabile in presenza di due condizioni:
- la mancata adozione ed attuazione, prima del reato, di idoneo modello organizzativo;
- la prova che il reato sia stato reso possibile dalla inosservanza degli obblighi di vigilanza o direzione.
Per ciò che attiene il considerevole profilo processuale relativo all’onere della prova, quindi nella prima ipotesi – reato commesso da soggetto in posizione apicale – l’ente deve provare di avere soddisfatto i requisiti richiesti dall’art. 6, comma 1, lettere da a) a d) del D.Lgs. 231, mentre nella seconda ipotesi – reato commesso dai sottoposti – ricade sull’accusa l’onere di provare sia la mancata adozione ovvero la mancata attuazione del modello organizzativo sia il fatto che il reato sia stato reso possibile dall’inosservanza degli obblighi di vigilanza o direzione.
In ogni caso, sia che il reato presupposto sia commesso da un soggetto in posizione apicale sia che sia posto in essere da una persona sottoposta all’altrui direzione o vigilanza, risulta assolutamente evidente il ruolo “centrale” del Modello di Organizzazione e Gestione, che, assume il valore di auto normazione dell’ente cui si fa riferimento per stabilirne la responsabilità, costituendo il fulcro di un sistema politico-criminale fondato sulla prevenzione piuttosto che sulla (sola) repressione.
1.3. Le sanzioni applicabili all’ente e l’autonomia della responsabilità amministrativa derivante da reato.
Laddove siano dimostrati i criteri oggettivi e soggettivi di imputazione e sussista, nel senso precisato, la c.d. “colpa di organizzazione” dell’ente, quest’ultimo può essere direttamente destinatario di diverse tipologie di sanzioni. In particolare, sono previste: (a) sanzioni pecuniarie; (b) sanzioni interdittive aventi ad oggetto l’attività cui si riferisce l’illecito dell’ente; (c) la confisca; (d) la pubblicazione della sentenza.
(a) sanzioni pecuniarie: la determinazione delle sanzioni pecuniarie irrogabili ai sensi del decreto 231 si fonda su un sistema di quote. Per ciascun illecito, la legge determina infatti in astratto un numero minimo e massimo di quote, sul modello delle cornici edittali che tradizionalmente caratterizzano il sistema sanzionatorio. In questo senso, l’articolo 10 del D.Lgs. 231/01 si limita a prevedere che il numero di quote non può mai essere inferiore a cento e superiore a mille e che l’importo delle singole quote può oscillare tra un minimo di circa 258 euro a un massimo di circa 1549 euro.
(b) sanzioni interdittive: laddove espressamente previsto dalla legge e qualora sussistano ulteriori condizioni (profitto di rilevante entità, gravi carenze organizzative o reiterazione degli illeciti) è prevista l’applicazione di sanzioni interdittive che, incidendo sull’attività aziendale, pregiudicano o precludono l’operatività dell’ente destinatario delle stesse. Le sanzioni interdittive possono consistere: a. nell’interdizione dall’esercizio dell’attività; b. nella sospensione o la revoca delle autorizzazioni, licenze o concessioni funzionali alla commissione dell’illecito; c. nel divieto di contrattare con la pubblica amministrazione, salvo che per ottenere le prestazioni di un pubblico servizio; d. nell’esclusione da agevolazioni, finanziamenti, contributi o sussidi e l’eventuale revoca di quelli già concessi; e. nel divieto di pubblicizzare beni o servizi.
(c) confisca: qualora venga pronunciata una sentenza di condanna, nei confronti dell’ente è sempre disposta la confisca del prezzo o del profitto del reato, salvo che per la parte che può essere restituita al danneggiato e fatti salvi i diritti acquisiti dai terzi in buona fede. Quando non è possibile eseguire la confisca sui beni costituenti direttamente prezzo o profitto del reato, la stessa può avere ad oggetto somme di denaro, beni, o altre utilità di valore equivalente al prezzo o al profitto del reato.
(d) pubblicazione della sentenza di condanna: infine, il giudice, se applica sanzioni interdittive, può anche disporre la pubblicazione della sentenza di condanna, misura capace di recare un grave impatto sull’immagine dell’ente. La pubblicazione della sentenza di condanna in uno o più giornali, per estratto o per intero, può essere disposta dal giudice, unitamente all’affissione nel comune dove l’ente ha la sede principale, quando è applicata una sanzione interdittiva.
In ottemperanza al principio di autonomia della responsabilità dell’ente, sancito dall’art. 8 del D. Lgs. 231/01, l’ente è responsabile del reato commesso nel suo interesse o a suo vantaggio anche qualora sia ignoto l’autore materiale del reato o quando questo sia non imputabile, così come quando il reato sia estinto per una causa diversa dalla amnistia.
CAPITOLO 2: LA STRUTTURA E LE CARATTERISTICHE DI SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A. ED IL MODELLO DI ORGANIZZAZIONE E GESTIONE APPROVATO A LIVELLO AZIENDALE.
Atteso che il Modello di Organizzazione e Gestione costituisce il perno su cui si imposta la valutazione di colpevolezza dell’ente, Società Prodotti Antibiotici S.p.A., al fine di adeguarsi ai precetti del D.Lgs. 231/01 e di consolidare la sua cultura di governance e compliance, ha predisposto il presente Modello Organizzativo contenente misure volte a garantire la prevenzione o la minimizzazione del pericolo di commissione dei reati-presupposto,
Prima di soffermarsi sui criteri seguiti per la redazione di tale documento ed analizzarne per sommi capi la struttura, è preliminarmente necessario approfondire le caratteristiche di Società Prodotti Antibiotici S.p.A., descrivendone l’oggetto sociale e la struttura organizzativa.
2.1. Le caratteristiche di Società Prodotti Antibiotici e la sua struttura.
2.1.1. La storia della Società e l’oggetto sociale della stessa.
Società Prodotti Antibiotici S.p.A. opera in ambito farmaceutico e diagnostico ed è stata fondata nel 1947 su iniziativa del fisiologo Rodolfo Ferrari e del microbiologo Carlo Callerio. Dopo essere stata la prima realtà di settore in Italia a produrre la penicillina nell’immediato dopoguerra, l’azienda ha vissuto una crescita costante, ampliando le proprie attività a diversi ambiti terapeutici, soprattutto osteoarticolare, urologico e cardiovascolare.
Nel 1987 è nata BIOSPA, la Divisione diagnostica di Società Prodotti Antibiotici inizialmente deputata alla promozione e commercializzazione di reagenti per diagnostica in vitro (sviluppati e prodotti direttamente nei laboratori di biotecnologia) e successivamente estesa alla distribuzione esclusiva di prodotti biotecnologici. Attualmente, tale Divisione rappresenta un affidabile produttore e fornitore, specializzato in biologia cellulare, biologia molecolare, immunologia, strumentazione, istocompatibilità e materie prime. Nel dettaglio la Divisione commercializza:
- diagnostici in vitro (IVD) per tipizzazione tissutale (HLA);
- reagenti chimici e biochimici per uso ricerca biomedica;
- materie prime per IVD;
produce:
- reagenti accessori per IVD basati sulla tecnologia Avidina-Streptavidina/Biotina;
- materie prime per IVD e uso generico di laboratorio quali Biotina/Avidina
- modificata e Streptavidina ottenuta per fermentazione, della quale BIOSPA è l’unico produttore a livello europeo.
Come si evince dallo Statuto, Società Prodotti Antibiotici S.p.A. ha per oggetto esclusivo:
- “la ricerca, lo sviluppo, la produzione in conto proprio o in conto terzi, la sperimentazione e l’analisi, la registrazione, la fornitura e la commercializzazione, sia in Italia che all’estero” dei seguenti beni:
- prodotti base per l’industria farmaceutica e veterinaria (comprese le materie prime, gli intermedi, i prodotti semifiniti, i principi attivi farmaceutici sia organici che inorganici, i prodotti biologici, biotecnologici e affini, prodotti finiti farmaceutici, galenici, generici e da banco);
- prodotti cosmetici;
- integratori alimentari;
- dispositivi medici.
- ogni altra attività di “prestazione di servizi” nei predetti settori industriali, tra cui “lo sviluppo dei processi di produzione, di laboratorio, pilota, industriali, commerciali, per tali prodotti, l’acquisto, la licenza attiva e passiva, lo scambio e la cessione di tecnologie in questo campo, l’assunzione e la concessione di agenzie e rappresentanze commerciali nel settore”;
- l’organizzazione di seminari medici e scientifici, la distribuzione e divulgazione di studi medici o di altro materiale finalizzato alla prevenzione/trattamento di patologie, lo svolgimento di attività didattiche o promozionali a favore di medici o farmacisti;
- il compimento di tutte le operazioni economico-finanziarie utili e la stipulazione di qualsiasi negozio giuridico (inclusi, in via esemplificativa e non limitativa, la locazione anche finanziaria e la vendita di beni mobili o immobili) utile o necessarie per il conseguimento dell’oggetto sociale;
- l’assunzione diretta o indiretta di interessenze o partecipazioni in altre società o imprese, costituite o costituende, aventi un oggetto analogo, affine o comunque connesso al proprio, così come la concessione di mutui o fideiussioni alle stesse.
2.1.2. L’attuale sistema di amministrazione e controllo.
La società è attualmente amministrata secondo il sistema “tradizionale” di amministrazione e controllo cui agli artt. 2380 bis – 2409 septies c.c., annoverando un Consiglio d’Amministrazione composto da numero tre membri e da un collegio sindacale composto da tre membri effettivi e due membri supplenti.
Quanto all’organo amministravo, lo stesso, coerentemente con le previsioni statutarie, elegge tra i suoi membri un Presidente ed un Amministratore Delegato, cui è attribuita la rappresentanza legale della società. In base alla delibera del CdA sono stati conferiti sia al Presidente che all’amministratore poteri a firma singola o congiunta a seconda del raggiungimento di determinate soglie economiche. Come si dirà meglio nel prosieguo del presente Modello, il Presidente e l’AD, nei limiti dei poteri ad essi conferiti, hanno la facoltà di nominare procuratori o mandatari per il compimento di specifici atti, alla cui nomina dovrà essere data tempestiva pubblicità attraverso l’iscrizione presso il Registro delle Imprese. Il solo Amministratore Delegato – in qualità di soggetto incaricato della “sicurezza dei lavoratori e della tutela ambientale” e di datore di lavoro ex D.Lgs. 81/08 – potrà poi conferire specifiche deleghe di funzioni.
Quanto all’organo di controllo, Società Prodotti Antibiotici S.p.A. si è dotata (come detto) di un collegio sindacale composto da numero tre (3) membri effettivi e due (2) membri supplenti, a cui è affidato il compito di vigilare sull’osservanza della legge e dello statuto, sul rispetto dei principi di corretta amministrazione ed in particolare sull’adeguatezza dell’assetto organizzativo, amministrativo e contabile adottato dalla società e sul suo concreto funzionamento ex art 2403 cod. civ.
Atteso che la società non rientra tra i soggetti che hanno l’obbligo di sottoporre il proprio bilancio a revisione, il controllo contabile è attualmente affidato a professionisti terzi che si interfacciano con la Direzione Amministrazione, Finanza e Controllo.
2.1.3. La struttura della società e le sedi in cui si svolgono le attività aziendali.
Tanto premesso in ordine al sistema di gestione, Società Prodotti Antibiotici S.p.A. si caratterizza per una struttura dinamica e flessibile, ripartita tra una parte “amministrativo-gestionale” – che opera all’interno delle sedi presenti a Milano in via Biella ed in via Modica – ed una parte di informazione scientifica, che svolge la propria attività sul territorio a seconda della specifica area territoriale assegnata.
Quanto alla struttura amministrativo-gestionale, la stessa si suddivide in Divisioni, Direzioni ed Uffici che riportano tutti direttamente all’Amministratore Delegato.
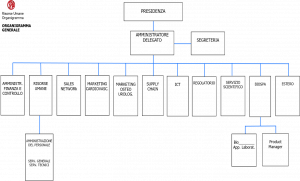
In conformità ai dettami legislativi, è stato altresì individuato un Responsabile del Servizio di Farmacovigilanza al fine di garantire e monitorare costantemente la qualità, sicurezza e la performance dei prodotti aziendali mediante l’analisi e la trasmissione delle segnalazioni di eventuali eventi avversi relativi ai propri prodotti. Le attività in tema di Farmacovigilanza sono svolte da un soggetto estraneo alla struttura della società.
Un discorso a parte merita BIOSPA. Se da un lato la stessa non ha una propria personalità giuridica ed è una mera divisione di Società Prodotti Antibiotici SPA (dipendendo da quest’ultima quanto alla gestione economica ed amministrativa, alla gestione del personale, all’approvvigionamento di prodotti ad uso laboratorio ed al sistema informatico), dall’altro tale Divisione presenta degli indubbi tratti di autonomia organizzativa e decisionale che la differenziano notevolmente dalle Direzioni della società. Al riguardo, occorre evidenziare che BIOSPA:
- ha una propria segreteria, ulteriore e diversa da quella a diretto riporto dell’Amministratore Delegato;
- dispone di un laboratorio;
- ha delle autonome figure manageriali (Product Manager e Product Specialist) ed un proprio ufficio commerciale;
- si avvale di agenti di vendita pluri o monomandatari anziché della rete degli Informatori Scientifici del farmaco;
- è certificata ISO 9001 e dispone, oltre che di un “Manuale della qualità”, anche di alcune procedure specifiche.
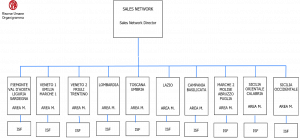
Di seguito si riporta l’organigramma della predetta Divisione.

In particolare, la divisione BIOSPA è composta da alcune risorse che si occupano prevalentemente di seguire le linee commercializzate di sei società e da due persone che seguono la produzione interna e la vendita, producendo e distribuendo prodotti sia su scala nazionale che all’estero. Il mercato a cui si rivolge BIOSPA è rappresentato da laboratori universitari ed ospedalieri su tutto il territorio italiano, ditte produttrici di vaccini e farmaci per uso umano e veterinario e industrie produttrici di IVD.
Il mercato italiano è gestito prevalentemente attraverso undici agenzie plurimandatarie, che seguono i clienti in funzione dell’area geografica di competenza: il mercato estero per i reagenti prodotti dall’area tecnica, è invece affidato in completa autonomia al personale di tale area.
Al di là del laboratorio di BIOSPA – caratterizzato da un’attività di produzione estremamente limitata e dall’impiego di risibili risorse – è importante rilevare che Società Prodotti Antibiotici non dispone di proprie sedi produttive o di magazzini, demandando a società terze la produzione, lo stoccaggio, la gestione e la spedizione dei prodotti commercializzati. In questo senso, SPA si avvale di partner specializzati e debitamente certificati, che sono periodicamente oggetto di verifiche ed audit ispettivi da parte della Funzione Quality Assurance.
Con riguardo, invece, alla struttura legata all’informazione scientifica – ricompresa nella più ampia Direzione “Sales Network” ed inglobante il 65% delle risorse umane di SPA – la stessa si fonda sulla capillare rete degli Informatori Scientifici del Farmaco e degli Area Manager che, operando in relazione ad una determinata area geografica, svolgono le proprie attività prevalentemente fuori sede.
2.2. I criteri normativi e paranormativi seguiti per la redazione del presente Modello di Organizzazione e Gestione e la struttura del presente documento.
Tanto premesso in ordine alla struttura organizzativa e gestionale di Società Prodotti Antibiotici S.p.A., la società, come detto, ha adottato il presente Modello di Organizzazione e Gestione per la prevenzione o la minimizzazione del pericolo di commissione dei reati-presupposto. Nella redazione di tale documento, Società Prodotti Antibiotici S.p.A., ha fatto riferimento:
- ai requisiti normativi previsti dal D. Lgs. 231/01, descritti sommariamente all’interno dell’art. 6 del D.Lgs. 231/01 e , per quanto attiene specificamente la gestione dei rischi connessi alla salute e sicurezza dei lavoratori, all’interno dell’art. 30 del D.Lgs. 81/08;[3]
- alle indicazioni che provengono dalle linee guida delle Associazioni di categoria più rappresentative quali, a titolo esemplificativo e non esaustivo Confindustria e Farmindustria (c.d. “criteri paranormativi”). Indicazioni che, come ammesso dalla giurisprudenza, “possono certamente essere assunte come paradigma, come base di elaborazione del Modello in concreto da adottare” sia pur nella piena consapevolezza che lo stesso “deve poi essere calato nella realtà aziendale nella quale è destinato a trovare attuazione”;[4]
- ai principi giurisprudenziali che si sono affermati in tema di responsabilità da reato dell’ente e di adeguatezza dei Modelli, che hanno precisato ed integrato quanto stabilito dall’articolato del D. Lgs. 231/01 (c.d. “criteri giurisprudenziali”).
Tanto premesso sotto il profilo teorico, il presente Modello di Organizzazione e Gestione si articola in:
UNA PARTE GENERALE: che descrive i profili essenziali della responsabilità amministrativa degli enti dipendente da reato, i principi base e gli obiettivi del MOG, le modalità di adozione, diffusione ed applicazione dello stesso, le caratteristiche e la struttura della società, la natura ed i compiti dell’Organismo di Vigilanza (di seguito anche più semplicemente “OdV”) ed il sistema disciplinare previsto per assicurarne un’efficace attuazione, così come i presidi adottati per garantire la tempestiva segnalazione degli illeciti.
DIVERSE PARTI SPECIALI dedicate alle specifiche tipologie di reato che, sulla base di quanto emerso dall’attività di risk assesment, debbono considerarsi a maggiore rischio di commissione nell’ambito dei processi aziendali di SPA. In questo senso, sono previste nove Parti speciali:
- Parte Speciale “Reati contro la Pubblica Amministrazione, reati di corruzione tra privati ed istigazione alla corruzione tra privati ed associazione a delinquere (artt. 24, 24ter, 25 e 25ter, comma 1, lett. s bis)”;
- Parte Speciale: “Delitti informatici e di trattamento illecito di dati nonché delitti in materia di violazione del diritto d’autore (artt. 24bis e 25novies)”;
- Parte Speciale “Reati societari” (art. 25ter);
- Parte Speciale: “Reati contro l’industria ed il commercio e contro la fede pubblica (artt. 25bis e 25bis1)”;
- Parte Speciale: “Reati di omicidio colposo o lesioni gravi o gravissime commesse con violazione delle norme sulla tutela della salute e sicurezza sul lavoro (Art. 25septies)”;
- Parte Speciale: “induzione a non rendere dichiarazioni o a rendere dichiarazioni mendaci all’Autorità Giudiziaria e favoreggiamento personale transnazionale art. 25decies e combinato disposto degli artt. 378 c.p. e artt. 3 e 10 della L. 146/06”;
- Parte Speciale: “Reati ambientali (Art. 25undecies)”;
- Parte Speciale “Reati di ricettazione, riciclaggio, impiego di denaro, beni o utilità di provenienza illecita, autoriciclaggio e delitti tributari (artt. 25octies e 25quinquiesdecies)”;
- Parte Speciale: “L’impiego di cittadini di paesi terzi il cui soggiorno è irregolare, intermediazione illecita e sfruttamento del lavoro e reati di razzismo e xenofobia (artt. 25quinquies, duodecies e terdecies D.Lgs. 231/01)”.
Il Modello è completato da una serie di allegati che, benché richiamati in modo generico all’interno del testo, ne costituiscono una parte integrante ed essenziale, contribuendo a precisare alcuni concetti giuridici di cui al D.Lgs. 231/01, a descrivere la struttura della società ed a comprendere i presidi adottati dalla stessa per prevenire o minimizzare il rischio di commissione delle predette condotte illecite. Si tratta in particolare dei seguenti documenti:
- l’appendice normativa (all. 1), contenente una sintetica descrizione di tutte le fattispecie presupposto contemplate negli artt. 24 ss. del D.Lgs. 231/01, comprese quelle che, secondo le valutazioni compiute all’esito dell’attività di risk assesment non presentano (nemmeno astrattamente) un rischio di commissione nell’ambito delle attività aziendali di Società Prodotti Antibiotici S.p.A.;
- il Codice Etico (all. 2), volto a descrivere i principi ed i valori che costituiscono il fondamento dell’attività economica di Società Prodotti Antibiotici S.p.A., orientandola al rispetto di rigorosi standard etici e deontologici.
- gli Organigrammi concernenti la struttura organizzativa e funzionale di SPA e della Divisione BIOSPA (all. 3);
- le Standard Operative Procedures (di seguito anche “SOP”) adottate sia con riguardo a SPA che in relazione alla Divisione BIOSPA, che, come detto, si caratterizza per un autonomo sistema di gestione della qualità e per il conseguimento della certificazione UNI EN ISO 9001:2015 ( all. 4);
- le deleghe di funzioni adottate in ambito ambientale ed in tema di salute e sicurezza dei lavoratori (all. 5).
2.3. Le finalità del Modello di Organizzazione e Gestione ed i destinatari dello stesso.
Il presente Modello ha l’obiettivo di descrivere il sistema di regole operative e comportamentali che disciplinano le attività “sensibili” della società, precisando i presidi e/o i controlli adottati al fine di garantire il pieno rispetto dei principi etici su cui si fonda il business aziendale e di evitare la commissione dei reati presupposto. Atteso che l’efficace attuazione delle disposizioni ivi contenute non può prescindere dalla creazione di una cultura aziendale fondata sulla consapevolezza della centralità di un sistema compliant, il Modello di Organizzazione ha altresì la finalità:
- di chiarire ai dipendenti di Società Prodotti Antibiotici i confini tra le condotte ammesse in quanto conformi alle disposizioni attualmente vigenti e/o alle SOP adottate internamente e quelle vietate;
- di illustrare le conseguenze previste in caso di violazione delle disposizioni ivi riportate, sia sotto il profilo personale (eventuale commissione di un reato e/o di un illecito disciplinare) sia sotto il profilo societario (sanzioni amministrative applicate all’ente);
- di radicare la filosofia di un business etico e sostenibile, che va al di là di mere logiche di profitto;
- di consentire – grazie ai canali di segnalazione ed ai flussi informativi – un costante continuo monitoraggio sulle aree sensibili o strumentali alla commissione dei reati, intervenendo tempestivamente per prevenire o contrastare eventuali condotte illecite o contrarie alla normativa adottata internamente.
In questo senso, i soggetti destinatari del Modello devono essere individuati:
- nei componenti degli Organi sociali ed in coloro che svolgono, anche di fatto, funzioni di gestione, amministrazione, direzione e controllo della società o di una sua unità organizzativa dotata di autonomia finanziaria e funzionale;
- nei dirigenti o dipendenti della società che si trovino ad operare sotto la vigilanza ed il controllo delle persone indicate sub a).
Nei confronti dei fornitori e i professionisti esterni – soggetti separati dall’Ente e, in quanto tali, non destinatari del Modello di organizzazione gestione e controllo adottati ai sensi del d.lgs. 231/2001 – giova precisare che Società Prodotti Antibiotici ha comunque sviluppato presidi di controllo atti a garantire il rispetto delle procedure e del Codice Etico, attraverso idonei strumenti di carattere contrattuale (ad esempio attraverso specifiche clausole) e una costante attività di informazione degli stessi in merito ai contenuti essenziali del Modello.
2.4. Le modalità operative concretamente seguite per la costruzione del Modello di Organizzazione e Gestione.
Come anticipato, il Modello di Organizzazione e Gestione è stato redatto sulla base dei criteri normativi, paranormativi e giurisprudenziali offerti dal Legislatore, dalle principali Associazioni di Categoria e dalla giurisprudenza. In questo senso – sul presupposto che l’art. 6 del D.Lgs. 231/01 stabilisce che il Modello deve identificare le attività aziendali nel cui ambito possono essere commessi i reati presupposto e deve descrivere gli “specifici protocolli diretti a programmare l’attuazione e la formazione delle decisioni dell’ente in relazione ai reati da prevenire” – il presente documento rappresenta l’esito di un’approfondita attività di studio ed analisi della struttura aziendale di Società Prodotti Antibiotici S.p.A., nel corso della quale:
- sono state reperite ed inventariate tutte le Standard Operative Procedures aziendali (sia riferite a SPA che alla specifica Divisione BIOSPA) ed è stata esaminata ogni ulteriore documentazione relativa al sistema “compliance” e di gestione del rischio (anzitutto il Manuale della Qualità concernente BIOSPA);
- è stato studiato l’assetto organizzativo della Società con particolare attenzione alla distribuzione dei poteri ed all’eventuale sistema di procure e/o deleghe di funzioni;
- sono stati intervistati i soggetti che, secondo quanto risultante dall’organigramma e dai documenti societari, dirigono e coordinano le aree di attività c.d. “sensibili”, in cui sussiste un astratto rischio di commissione di uno dei reati presupposto disciplinati dal D.Lgs. 231/01.
In questo modo, per utilizzare le parole utilizzate dalle Linee Guida di Confindustria, è stata compiuta la valutazione dei “rischi potenziali”, ovvero “l’analisi del contestato aziendale per individuare in quali aree o settori di attività e secondo quali modalità si potrebbero astrattamente verificare eventi pregiudizievoli per gli obiettivi indicati dal decreto 231”.[5] Analisi che, come chiarito in diverse occasioni dalla giurisprudenza, deve avvenire attraverso un concreto ed effettivo studio delle dinamiche organizzative e/o di controllo dell’azienda, senza che sia sufficiente una valutazione meramente giuridica e formale,
Le considerazioni circa i “rischi” – definiti dalle predette linee guida come “qualsiasi variabile o fattore che nell’ambito dell’azienda, da soli o in correlazione con altre variabili, possano incidere negativamente sul raggiungimento degli obiettivi indicati nel Decreto 231”,[6] sono state compendiate nel documento di risk assesment e gap analiysis che, sulla base dello studio della documentazione societaria e delle circostanze riferite nel corso dei verbali di intervista, ha stabilito:
- quali sono le aree maggiormente a rischio di commissione dei reati presupposto e attraverso quali modalità gli stessi possono essere posti in essere nel contesto operativo interno ed esterno in cui opera l’azienda;
- quali sono i presidi ed i controlli attualmente predisposti dalla società, “fotografando” il sistema già esistente all’interno dell’ente per la prevenzione dei reati;
- quali sono i rischi che non possono considerarsi adeguatamente prevenuti e quali interventi debbano essere posti in essere al fine di implementare un sistema di gestione del rischio idoneo ed efficace. In questo modo, è stato possibile desumere le aree di miglioramento del sistema di controllo interno esistente e, sulla base di quanto emerso, è stato predisposto un piano di attuazione teso ad individuare i requisiti organizzativi e le azioni da adottare per garantire un idoneo ed efficace sistema di gestione del rischio.
La predetta metodologia – oltre che essere rispettosa dei requisiti normativi nonché delle indicazioni emanate dalle principali associazioni di categoria e dalla giurisprudenza – garantisce che il Modello di Organizzazione e Gestione di SPA non si aggiunga in modo aprioristico e irrazionale a tutte le strutture compliance ma, al contrario, realizzi una sinergica sovrapposizione e coincidenza con le procedure già adottate e con i sistemi di controllo già in essere.
- IL SISTEMA DI CONTROLLO INTERNO IMPLEMENTATO DA SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A. AL FINE DI GESTIRE I RISCHI CONNESSI ALLO SVOLGIMENTO DELLE ATTIVITÀ AZIENDALI.
Alla luce del fatto che il “Sistema 231” si inserisce nel più ampio insieme dei controlli interni, gli obiettivi di prevenzione o minimizzazione dei rischi di commissione dei reati presupposti e rappresenta nient’altro che una parte dei più generali obiettivi riconducibili alla compliance, è bene soffermarsi sui principi generali che debbono caratterizzare il business della società e sul sistema di controllo interno. Con tale espressione, si intende l’insieme delle regole, delle procedure e delle strutture organizzative volte a consentire attraverso un adeguato processo di identificazione, misurazione, gestione e monitoraggio dei principali rischi, una conduzione delle attività aziendali che, oltre ad essere idonea ad assicurare il raggiungimento degli obiettivi aziendali, sia sana e corretta.
La definizione del sistema di controllo interno è compito del Consiglio di Amministrazione che, su proposta dell’Amministratore Delegato, provvede a stabilirne le linee essenziali e a verificarne periodicamente l’efficacia e l’effettivo funzionamento.
Al fine di garantire l’adeguatezza dei processi aziendali in termini di efficacia, di conformità a leggi e normative, di affidabilità ed integrità dei dati contabili, e di tutela del patrimonio aziendale, Società Prodotti Antibiotici S.p.A. ha istituito un sistema fondato su:
3.1. il conferimento di procure e/o deleghe di funzioni;
3.2. l’adozione di un Codice Etico;
3.3. la stringente proceduralizzazione dei processi aziendali;
3.4. il conseguimento di certificazioni;
3.5. la predisposizione di diversi livelli di controllo.
3.1. Il sistema di deleghe e procure.
La società ha anzitutto adottato un sistema di procure e di deleghe di funzioni che attribuisce a taluni soggetti i poteri per la gestione delle attività di competenza. In conformità a quanto stabilito dalle Linee Guida di Confindustria – che precisano come i poteri autorizzativi e di firma “vanno assegnati in coerenza con le responsabilità organizzative e gestionali (…) in modo chiaro e univoco” con una puntuale indicazione delle soglie di approvazione delle spese – il sistema organizzativo di cui si è dotata SPA si conforma ai seguenti principi:
- formalizzazione e tracciabilità delle procure e/o deleghe;
- chiara definizione delle responsabilità attribuite;
- corrispondenza tra le responsabilità attribuite ed i poteri decisionali e/o autorizzativi;
- competenza e professionalità dei
- esistenza di una contrapposizione di funzioni;
- implementazione di flussi informativi aziendali.
Il Consiglio di Amministrazione è l’organo preposto a conferire ad approvare formalmente i poteri di firma ed autorizzativi: a tal fine, è stato nominato un Amministratore Delegato (di seguito anche più semplicemente AD), cui sono stati conferiti ampi poteri di ordinaria amministrazione. Le decisioni di gestione strategica e straordinaria della società devono comunque essere gestite ed approvate dal CdA.
Oltre ad individuare un AD, il Consiglio di Amministrazione, al fine di coadiuvare l’Amministratore Delegato nell’esercizio delle funzioni attribuitegli e di assicurare il buon funzionamento delle attività cui lo stesso deve presiedere, ha nominato uno o più procuratori, attribuendo agli stessi determinati e specifici poteri accompagnati da una precisa individuazione dei limiti di spesa. Società Prodotti Antibiotici potrà essere impegnata verso soggetti terzi unicamente da dipendenti e/o dirigenti cui sia stata conferita una procura scritta, formalizzata davanti ad un Notaio e riportata all’interno delle visure aziendali.
Ai sensi della normativa in tema di salute e sicurezza sul lavoro, fermi restando i perduranti obblighi di controllo sussistenti in capo agli ulteriori componenti del Consiglio di Amministrazione e la responsabilità gravante sugli stessi,[7] l’Amministratore Delegato riveste la qualifica di “datore di lavoro” a norma dell’art. 2, comma primo, lettera b) del D. Lgs. 81/08 (di seguito anche “T.U.”).[8] In tale qualità l’Amministratore Delegato, alla luce dell’articolata organizzazione aziendale, ha conferito specifiche deleghe di funzioni ex art. 16 D.Lgs. 81/08 per assicurare il pieno ed effettivo rispetto della normativa in tema di salute e sicurezza sul lavoro. Tale scelta – così come la sussistenza di sub-deleghe – è coerente con la costante giurisprudenza di merito e di legittimità che ha da tempo sottolineato come la complessità dei processi gestionali ed operativi all’interno di un’impresa di medie o rilevanti dimensioni imponga necessariamente, per essere fronteggiata, l’esistenza di una pluralità di figure che, in virtù di valide deleghe o procure, possano intervenire a garantire un presidio dei rischi legati alla commissione di un reato presupposto.[9]
Il conferimento di deleghe e sub-deleghe di funzioni ha altresì interessato la materia della tutela ambiente, in relazione alla quale, per quanto limitati, sussistono astratti rischi di commissione di alcuni dei reati presupposto di cui all’art. 25undecies D.Lgs. 231/01. La stessa Corte di Cassazione ha al riguardo evidenziato che “in materia ambientale, come peraltro in materia di sicurezza sul lavoro, allorquando si tratti di aziende di non modeste dimensioni, il legale rappresentante può, a fronte della molteplicità dei compiti istituzionali o della complessità dell’organizzazione aziendale, affidare in base a precise disposizioni preventivamente adottate secondo le disposizioni statutarie, la direzione di singoli rami o impianti a persone, dotate di capacità tecnica e autonomia decisionale” avvalendosi dell’istituto della “delega di funzioni” (Cassazione, sez. III penale, 1 giugno 2017 n.31364).
La società si impegna ad assicurare la documentabilità e l’aggiornamento del sistema di deleghe e procure.
3.2. L’adozione di un Codice Etico.
Al fine di descrivere i principi ed i valori che costituiscono il fondamento dell’attività economica di Società Prodotti Antibiotici S.p.A., SPA ha poi approvato un Codice Etico.
Fermo restando che tale documento costituisce un allegato del presente Modello e che si rimanda allo stesso per ogni più approfondita considerazione, in questa sede è sufficiente ribadire che il business aziendale è orientato al rispetto di rigorosi standard etici e deontologici, fondandosi sull’imprescindibile osservanza di leggi (oltre che di regolamenti, ordini o discipline), sulla tutela della salute, sul rispetto della persona umana, dei lavoratori e sulla leale concorrenza nei confronti degli altri competitor che si trovano ad operare sul mercato. In questo senso, nel Codice Etico sono ribaditi i punti essenziali ed irrinunciabili della politica aziendale, ed in particolare:
- il rispetto dell’ambiente e la sostenibilità ecologica;
- la tutela della salute e della sicurezza sul lavoro;
- la parità di trattamento e l’assenza di discriminazioni fondate su sesso, razza, condizione sociale/familiare o convinzioni politiche e/o religiose;
- la trasparenza e correttezza delle condotte commerciali, che deve essere richiesta anche ai soggetti che siano fornitori e/o partner di Società Prodotti Antibiotici S.p.A.;
- il rispetto delle norme interne, comunitarie e internazionali poste a tutela della proprietà industriale e intellettuale;
- la completezza, chiarezza e trasparenza delle informazioni attinenti i farmaci e/o gli altri prodotti commercializzati;
- l’eticità, scientificità ed economicità delle manifestazioni congressuali, convegni, riunioni scientifiche e a corsi di aggiornamento o delle ulteriori attività di informazione scientifica poste in essere da Società Prodotti Antibiotici S.p.A.;
- la trasparenza e la tracciabilità di tutte le operazioni economiche e finanziarie, con particolare riguardo ai trasferimenti di valore;
- la correttezza e trasparenza dei rapporti con le Pubbliche Amministrazioni nonché con gli operatori sanitari e le società scientifiche;
- la promozione di rapporti con le Associazioni mediche o con le associazioni di pazienti che siano ispirati alla divulgazione della conoscenza scientifica ed al miglioramento della conoscenza professionale.
Le disposizioni del Codice sono vincolanti per i comportamenti di tutti gli amministratori dell’Azienda, di coloro che ricoprono cariche sociali, dei soggetti alle dipendenze della società, dei consulenti e di chiunque vi instauri, a qualsiasi titolo, direttamente o indirettamente, stabilmente o temporaneamente, in Italia o all’estero, rapporti di collaborazione o di partnership. I destinatari delle norme del Codice sono tenuti ad osservare le prescrizioni in esso contenute e ad adeguare i propri comportamenti e le proprie azioni ai principi espressi.
3.3. La stringente proceduralizzazione dei processi aziendali e i principi generali di controllo.
Coerentemente con quanto previsto dalle Linee guida di Confindustria e di Farmindustria nonché dal “documento di riferimento per la certificazione delle procedure relative alle attività di informazione scientifica”, le attività individuate come sensibili e (in generale) tutti i processi aziendali sono regolamentati da Standard Operative Procedures (in sigla e più brevemente anche “SOP”), al fine di assicurare il pieno rispetto dei seguenti principi generali:[10]
- a)“nessuno può gestire in totale autonomia un intero processo aziendale” l’autorizzazione di un’azione o di un atto deve essere accordata da soggetto diverso da quello che compie l’azione o l’atto ed il controllo interno sul compimento dell’azione o dell’atto è esercitato da soggetto ulteriormente diverso;
- b)“devono essere rispettati i poteri autorizzativi e di firma”, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti;
- c)“ogni operazione, transazione e/o azione deve essere: verificabili, documentata, coerente e congrua”. La documentabilità consente – com’è ovvio – di procedere in qualsiasi momento all’effettuazione di controlli, permettendo di individuare il soggetto o i soggetti che hanno autorizzato l’operazione, chi l’ha materialmente compiuta e chi era preposto a svolgere le adeguate verifiche o i controlli. L’esigenza di “tracciabilità” delle attività aziendali può essere soddisfatta anche mediante l’implementazione di sistemi informatici in grado di gestire l’operazione;
- d)“i controlli effettuati devono essere documentati”. Le procedure con cui vengono effettuati i controlli devono garantire la possibilità di ripercorrere le attività di controllo effettuate, in modo tale da consentire la valutazione circa la coerenza delle metodologie adottate e la correttezza dei risultati emersi;
- e)“occorre individuare e correggere tempestivamente le non conformità” attraverso l’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi.
La procedimentalizzazione delle attività sensibili rappresenta un elemento imprescindibile per la costruzione di un idoneo ed efficace sistema di gestione del rischio e, non a caso, è indicata dalle Linee Guida di Confindustria come “il primo obiettivo per la costruzione di un modello organizzativo”.[11]
3.4. Il conseguimento di certificazioni.
Società Prodotti Antibiotici è da sempre impegnata nel perseguimento di politiche gestionali finalizzate ad assicurare la qualità dei prodotti e dei processi produttivi, la sostenibilità ambientale e sociale del modello di business ed il rispetto della salute e della sicurezza dei lavoratori. In questo senso:
- Società Prodotti Antibiotici è certificata in conformità a quanto previsto dal Codice Deontologico di Farmindustria che, nel paragrafo 1.13 dell’art. 1 (rubricato “principi generali”) prevede che “entro il 28 febbraio di ogni anno le aziende associate dovranno acquisire ed inviare al Presidente della Farmindustria specifica certificazione, riferita all’anno precedente, relativamente al rispetto delle procedure inerenti le attività di marketing e di informazione scientifica. Tale certificazione dovrà essere effettuata da Enti accreditati da ACCREDIA (Ente Italiano di Accreditamento) e potrà prevedere, in via esclusiva, per le aziende appartenenti al Comitato Nazionale della Piccola Industria il ricorso ad una procedura semplificata secondo le indicazioni dei rispettivi Enti di Certificazione”;
- La Divisione BIOSPA, ha conseguito negli ultimi anni diverse ed importanti certificazioni, quali la ISO 9001, che attesta la conformità dei processi aziendali alle normative e linee guida sviluppate dall’Organizzazione internazionale per la normazione (ISO), che, come noto, definiscono i requisiti per la realizzazione di un sistema di gestione della qualità che consenta di migliorare l’efficacia e l’efficienza nella realizzazione del prodotto e nell’erogazione del servizio, nonché di ottenere ed incrementare la soddisfazione del cliente.
3.5. La predisposizione di diversi livelli di controlli.
Il controllo sul rispetto dei principi contenuti nel Codice Etico, delle norme di legge, delle procedure e/o istruzioni operative che regolamentano i processi aziendali e del presente Modello di Organizzazione e Gestione si struttura in diversi livelli:
Un primo livello di controllo, “svolto generalmente dalle risorse interne della struttura, sia in autocontrollo da parte dell’operatore, sia da parte del presposto/dirigente” e che, “per aspetti specialistici”,[12] può ricorrere ad altre risorse interne ed esterne all’azienda. Lo stesso è composto:
- dai singoli dipendenti coinvolti nelle attività aziendali, in capo ai quali sussiste l’obbligo di attenersi scrupolosamente alle regole di condotta riportate nelle policies e che sono state oggetto dei corsi di formazione organizzati da Società Prodotti Antibiotici S.p.A.: In caso di anomalie o di dubbi in ordine al comportamento da adottare, gli stessi dovranno rivolgersi ai propri responsabili nonché segnalare tempestivamente quanto riscontrato;
- dai responsabili di Direzione e/o Divisione che coordinano e dirigono l’attività lavorativa di più soggetti o che sono incaricati di vigilare sulla corretta esecuzione delle attività aziendali. Per quanto concerne l’identificazione degli stessi, si rimanda ai diversi organigrammi disponibili sull’intranet aziendale nonché ai documenti adottati ai sensi e per gli effetti del D.Lgs. 81/08;
Un secondo livello di controllo, costituito:
- dalle verifiche ispettive interne così come descritte dalla SOP QA.SQ.16.04. che possono essere programmate o non programmate.
Le prime sono quelle che rientrano nella pianificazione annuale ad opera del Responsabile QA ed hanno prevalentemente ad oggetto le aree aziendali coinvolte in attività ad impatto GMP/GDP nonché quelle di Informazione Scientifica.
Le seconde sono le verifiche che, pur non preventivate, si rendono necessarie a fronte di esigenze specifiche e contingenti quali cambiamenti organizzativi o procedurali, eventi particolarmente critici (infortunio sul lavoro) o deviazioni, non conformità o reclami. Questo tipo di verifica può essere richiesta da qualsiasi funzione aziendale senza alcun preavviso e la decisione in ordine alla stessa viene assunta dal Responsabile QA.
Laddove le attività ispettive ravvisino non conformità, viene formulata tempestivamente una proposta in ordine alle azioni correttive o preventive da adottare, che viene trasmessa al Responsabile della Direzione/Divisione interessata dall’accertamento ed all’organo amministrativo. Qualora la non conformità abbia una rilevanza anche ai fini del presente Modello Organizzativo, la stessa viene altresì comunicata all’Organismo di Vigilanza di Società Prodotti Antibiotici S.p.A.
Tra le attività di verifica interna rientrano anche gli audit svolti periodicamente da BIOSPA per stabilire se il sistema di gestione della qualità è conforme a quanto pianificato nonché ai requisiti ISO 9001:2015 e se lo stesso è stato efficacemente attuato e mantenuto aggiornato. Agli audit possono partecipare anche valutatori esterni.
- accanto alle attività di verifica ispettive interne, sono poi organizzati audit c.d. “esterni” e/o sopralluoghi che interessano i depositi deputati allo stoccaggio ed alla distribuzione dei medicinali nonché i fornitori di materie prime e/o prodotti finiti di cui si avvale Società Prodotti Antibiotici S.p.A. Tali attività possono essere svolte sia dal Responsabile QA che da auditor esterni dotati della necessaria competenza e professionalità.
Annualmente, Società Prodotti Antibiotici provvede poi ad un “Riesame di Direzione” con riguardo a tutte le attività connesse direttamente o indirettamente all’informazione scientifica al fine di assicurare il rispetto dei requisiti e dei criteri stabiliti all’interno del “Documento di riferimento per la certificazione delle procedure relative all’attività di informazione scientifica”.
Tutta la documentazione redatta nell’ambito del riesame di Direzione o delle attività ispettive – quale, a titolo esemplificativo, i verbali delle operazioni compiute nonché gli eventuali piani di azioni correttive o preventive – è debitamente archiviata a cura del Responsabile QA e conservata per un periodo di dieci anni.
Un terzo livello di controllo, costituito dall’Organismo di Vigilanza e dal Comitato Covid.
Quest’ultimo – composto dal Datore di Lavoro, dal delegato ex art. 16 D.Lgs. 81/08, dall’RSPP, dal Medico competente e dall’RLS – è un organo istituito in ottemperanza a quanto stabilito dai protocolli sottoscritti dalle parti sociali per far fronte all’attuale situazione di emergenza epidemiologica ed è specificamente deputato a monitorare la corretta attuazione delle misure finalizzate a minimizzare o prevenire i rischi derivanti dalla diffusione del virus Sars-Covid19.
L’Organismo di Vigilanza, invece, a norma dell’art. 6 del D. Lgs. 231/01, è chiamato in generale a vigilare sull’efficace attuazione del presente Modello da parte della Società. Al fine di consentire il corretto espletamento delle sue funzioni, l’OdV è destinatario di periodici flussi informativi da parte di tutte le componenti di Società Prodotti Antibiotici S.p.A.
Alla luce del carattere essenziale di quest’ultimo organo – che rappresenta un perno imprescindibile del “sistema 231” e costituisce un presupposto indispensabile per esonerare l’ente dalla responsabilità amministrativa legata alla commissione dei reati presupposto – occorre soffermarsi sulle caratteristiche e sulle funzioni dello stesso, illustrandone i requisiti normativi e l’applicazione concreta all’interno di Società Prodotti Antibiotici S.p.A.
- L’ORGANISMO DI VIGILANZA.
4.1. Premessa: i requisiti normativi e paranormativi alla luce delle integrazioni giurisprudenziali.
Come noto, ai sensi dell’art. 6, comma 1, del D. Lgs. 231/2001, l’ente non risponde del reato presupposto commesso dal soggetto apicale se prova, tra le altre cose, che il “compito di vigilare sul funzionamento e l’osservanza dei modelli di curare il loro aggiornamento” è stato affidato “a un organismo dell’ente dotato di autonomi poteri di iniziativa e di controllo” (lett. b) e che non vi è stata “omessa o insufficiente vigilanza da parte dell’organismo di cui alla lett. b)” (lett. d).
Ai fini dell’esonero dalla responsabilità amministrativa da reato è dunque essenziale che l’ente affidi il controllo circa la corretta attuazione del Modello di Organizzazione e Gestione ad un Organismo di Vigilanza, che non deve essere un mero presidio formale ma deve svolgere un’attività continuativa all’interno della realtà aziendale. Senza di esso, il Modello sarebbe privo di efficacia concreta e, in quanto tale, potrebbe non essere ritenuto adeguato a esimere l’ente da un’ipotesi di responsabilità amministrativa derivante da reato. L’istituzione di un simile organo soddisfa dunque il requisito normativo dell’“efficace attuazione” previsto dall’art. 7, comma quarto, D. Lgs. 231/01 che stabilisce come il Modello debba essere sottoposto “a verifica periodica” e ad “eventuali modifiche quando sono scoperte significative violazioni delle prescrizioni ovvero quando intervengono mutamenti nell’organizzazione o nell’attività”. In accordo alle indicazioni normative, l’Organismo di Vigilanza:
(a) deve essere dotato di “autonomi poteri di iniziativa e controllo”.
L’autonomia va intesa nel senso che la posizione dell’OdV nell’ambito dell’ente deve garantire l’autonomia dell’iniziativa di controllo da ogni forma di interferenza o condizionamento da parte di qualunque componente dell’ente e, in particolare, dell’organo dirigente. Nel sistema disegnato dal decreto 231, infatti, quest’ultimo è uno dei soggetti controllati dall’Organismo di vigilanza.
Su tale requisito si è recentemente pronunciata la Corte di Cassazione, osservando che l’”iniziativa e controllo possono essere ritenuti effettivi e non meramente “cartolari”, soltanto ove risulti la non subordinazione del controllante al controllato: infatti, l’articolo 6, comma 2, lettera d), del decreto citato prevede una serie di obblighi di informazione nei confronti dell’organo di vigilanza, al fine evidente di consentire l’esercizio “autonomo” del potere di vigilanza; inoltre, l’articolo 6, comma 2, lettera e), citato prevede un sistema disciplinare idoneo. Da ciò deriva, quindi, che non può definirsi idoneo a esimere la società da responsabilità amministrativa da reato, il modello organizzativo che preveda l’istituzione di un organismo di vigilanza sul funzionamento e sull’osservanza delle prescrizioni adottate non provvisto di autonomi ed effettivi poteri di controllo, ma sottoposto alle dirette dipendenze del soggetto controllato”.
Oltre ad essere “autonomo”, l’Organismo di Vigilanza deve anche essere “indipendente”, in quanto, come opportunamente osservato dalle Linee Guida di Confindustria, “il primo requisito sarebbe svuotato di significato se i membri dell’Organismo di Vigilanza risultassero condizionati a livello economico o personale o versassero in situazioni di conflitto di interesse, anche potenziale”.
La caratterizzazione dell’OdV come organo imparziale impone che i suoi componenti non siano direttamente coinvolti nelle attività gestionali e/o amministrative della società, così da evitare un’indebita confusione tra controllanti e controllati. Solo in questo modo, l’OdV potrà essere garantito da eventuali interferenze, pressioni o condizionamenti che possano essere esercitati da organi o uffici della Società. Al riguardo, sul presupposto che le associazioni di categoria e la Giurisprudenza maggioritaria ammettono la presenza di un componente interno negli Oganismi collegiali, giova precisare che le Linee Guida di Confindustria precisano che “se l’Organismo di vigilanza ha composizione collegiale mista, poiché vi partecipano anche soggetti interni all’ente – preferibilmente privi di ruoli operativi – da questi ultimi non potrà pretendersi una assoluta indipendenza. Dunque, il grado di indipendenza dell’Organismo dovrà essere valutato nella sua globalità.” [13]
Come riconosciuto dalle Linee Guida e dalla giurisprudenza, entrambi i requisiti possono essere assicurati riconoscendo all’Organismo in esame una posizione autonoma e imparziale, prevedendo la dotazione di un budget annuale a supporto delle attività di verifica tecniche necessarie per lo svolgimento dei compiti e, come detto, evitando che allo stesso siano attribuiti compiti operativi.[14] Sempre a tal fine, dovranno poi essere previste cause di ineleggibilità e decadenza che “garantiscano onorabilità, assenza di conflitti di interesse e di relazioni di parentela con gli organi sociali e con il vertice”.[15]
(b) deve essere costituito da soggetti competenti e professionali, che, in quanto tali, siano in grado di svolgere efficacemente le attività che sono demandate a tale Organismo dalla legge. Come chiarito dalla giurisprudenza, non è sufficiente un generico rinvio al curriculum vitae dei singoli ma è necessario esigere che i membri dell’OdV abbiano competenze in “attività ispettiva, consulenziale, ovvero la conoscenza di tecniche specifiche, idonee a garantire l’efficacia dei poteri di controllo e del potere propositivo ad esso demandati” (così Trib. Napoli, 26 giugno 2007).[16]
Con riguardo alla “professionalità” dei membri, le linee guida delle principali associazioni di categoria hanno poi chiarito che è “auspicabile che almeno taluno dei membri dell’Organismo di vigilanza abbia competenze in tema di analisi dei sistemi di controllo e di tipo giuridico e, più in particolare, penalistico” in quanto “la disciplina in argomento ha natura sostanzialmente punitiva e lo scopo del modello è prevenire la realizzazione di reati” ed è pertanto “essenziale la conoscenza della struttura e delle modalità di consumazione dei reati, che potrà essere assicurata mediante l’utilizzo delle risorse aziendali ovvero della consulenza esterna”.[17]
(c) deve essere caratterizzato da una “continuità di azione”, assicurata dalla eventuale destinazione di risorse aziendali a supporto, dalla previsione di un numero minimo di riunioni durante l’anno, dalla presenza di un membro interno che, in quanto tale, è costantemente aggiornato sull’evoluzione organizzativa e sulle dinamiche societarie e dal conferimento di insindacabili poteri ispettivi e di acquisizione. In particolare:
- le attività poste in essere dall’OdV non devono essere sindacate da alcun altro organismo o struttura aziendale;
- l’OdV deve avere libero accesso presso tutte le funzioni della società – senza necessità di alcun consenso preventivo – onde ottenere ogni informazione o dato ritenuto necessario per lo svolgimento dei compiti previsti dal decreto 231;
- l’OdV può avvalersi, sotto la sua diretta sorveglianza e responsabilità, dell’ausilio di tutte le strutture della società, ovvero di consulenti esterni.
Al fine di garantire la continuità di azione, l’OdV, come si vedrà anche nel prosieguo del presente Modello, deve essere altresì destinatario di specifici flussi informativi che gli permettano di vigilare costantemente sul funzionamento e sull’osservanza dei modelli e di valutare la necessità di eventuali aggiornamenti. Secondo quanto precisato dalla dottrina e dalle stesse indicazioni contenute nelle Linee Guida di Confindustria, i flussi informativi dovrebbero avere ad oggetto (i) le risultanze periodiche delle attività di controllo poste in essere dalle funzioni aziendali a rischio reato (ii) le atipicità riscontrate nell’ambito delle informazioni disponibili (iii) eventuali segnalazioni dei singoli dipendenti che devono essere trasmesse ed acquisite con modalità tali da garantire la riservatezza della fonte e, in ogni caso, l’immunità da potenziali conseguenze negative nell’ambito del rapporto di lavoro con l’azienda. La “piattaforma cognitiva” alimentata dagli “obblighi di informazione” costituisce dunque un’imprescindibile requisito di operatività.
4.2. L’Organismo di Vigilanza istituito da Società Prodotti Antibiotici S.p.A.
In ottemperanza a quanto stabilito dalle disposizioni richiamate nel paragrafo precedente e tenuto conto delle caratteristiche della propria struttura organizzativa, Società Prodotti Antibiotici S.p.A. ha scelto di istituire un organismo collegiale a composizione mista, formato da due membri esterni e da un membro interno. Tale decisione è motivata dalla necessità di associare soggetti in grado di fornire un apporto qualificato in ordine ai profili tecnico-giuridici del peculiare sistema 231 ad un soggetto che, appartenendo alla società, disponga di un’immediata ed approfondita conoscenza della struttura aziendale e delle dinamiche organizzativo-gestionali della stessa.
L’individuazione e la nomina dei componenti è demandata al Consiglio di Amministrazione, che dovrà selezionare i candidati sulla base delle caratteristiche di professionalità ed indipendenza richieste a livello normativo e giurisprudenziale, garantendo che il membro interno non partecipi a decisioni ed attività operative. Al fine di garantire i requisiti di indipendenza e di autonomia, a partire dalla delibera di nomina e per tutta la durata della carica, i componenti dell’Organismo di Vigilanza di SPA non devono:
- rivestire incarichi esecutivi o delegati nel Consiglio di Amministrazione o in rappresentanza della Società;
- svolgere funzioni gestionali o amministrative;
- intrattenere significativi e consolidati rapporti d’affari con la Società, con società da essa controllate o ad essa collegate – ad esclusione del rapporto di lavoro subordinato e l’appartenenza al Collegio Sindacale – nonché con i consiglieri di amministrazione che siano muniti di deleghe;
- essere componenti del nucleo familiare degli Amministratori della società ovvero di soggetti che risultino titolari di partecipazioni azionarie tali da garantire agli stessi di influenzare le decisioni della società., dovendosi intendere per nucleo familiare quello costituito dal coniuge non separato legalmente, dai parenti ed affini entro il quarto grado;
- risultare titolari direttamente o indirettamente di partecipazioni nel capitale della Società.
Al fine di adempiere ai propri compiti, l’Organismo di Vigilanza potrà eventualmente avvalersi anche del supporto di altre funzioni aziendali di SPA, soprattutto di quelle che, a vario titolo, sono coinvolte in attività di audit, compliance e controllo.
L’OdV della Società è investito delle seguenti funzioni:
- valutare l’idoneità e l’efficace attuazione del Modello di Organizzazione e Gestione;
- vigilare sulla sussistenza e persistenza nel tempo dei requisiti di efficienza ed efficacia del Modello, anche in termini di rispondenza tra le modalità operative adottate in concreto dai destinatari del Modello stesso e le SOP formalmente richiamate nello stesso;
- rilevare eventuali violazioni che dovessero emergere tenuto conto anche delle segnalazioni ricevute e volgere un’istruttoria sulle stesse;
- formulare proposte all’Amministratore per gli eventuali aggiornamenti e adeguamenti del presente Modello Organizzativo, da realizzarsi mediante le modifiche o integrazioni che dovessero rendersi necessarie in conseguenza di violazioni significative delle prescrizioni del presente Modello Organizzativo e/o di modifiche dell’assetto aziendale societario, ovvero di modifiche legislative;
- fornire gli opportuni chiarimenti in relazione alle disposizioni contenute nel Codice Etico e nel Modello Organizzativo;
- definire e garantire, attraverso il coordinamento con il Settore Risorse Umane e con le ulteriori funzioni competenti, l’attuazione dei programmi per la diffusione del Modello Organizzativo e la formazione dei dipendenti con differente grado di approfondimento in relazione al diverso livello di coinvolgimento del personale nelle aree sensibili;
- assicurare la corretta implementazione di canali di segnalazione attraverso cui coloro che vengano a conoscenza di comportamenti non conformi alle previsioni del Codice Etico e/o del Modello Organizzativo, possano riferire all’Organismo di Vigilanza. Fermo restando che, per legge, almeno uno di essi dovrà essere telematico, tutti i canali dovranno essere strutturati in modo da garantire la riservatezza circa l’identità del soggetto segnalante;
- predisporre una relazione informativa, con cadenza semestrale, in ordine alle attività di verifica e controllo compiute nel periodo preso in considerazione, da fornire all’Amministratore e, in copia, al collegio sindacale;
- effettuare le segnalazioni previste dalla recente normativa in tema di riciclaggio (art. 52, comma 2, D. Lgs. 231/2007).
Per poter assolvere con efficienza alle proprie funzioni – ivi compresa quella di aggiornare i contenuti del Modello Organizzativo in relazione a modifiche legislative o di assetto organizzativo della Società – Società Prodotti Antibiotici S.p.A. assicura un un’adeguata autonomia e una continuità d’azione all’Organismo di Vigilanza. A tal fine:
- l’Amministratore Delegato di Società Prodotti Antibiotici S.p.A. mette a disposizione dell’Organismo di Vigilanza tutte le risorse economiche e finanziarie di cui lo stesso necessiti per adempiere correttamente i compiti di cui all’art. 6 D.Lgs. 231/01, attribuendo un budget annuale. Laddove si renda necessaria un’attività che eccede l’importo stabilito a titolo di budget, l’OdV trasmette all’Amministratore Delegato una richiesta adeguatamente motivata, illustrando la tipologia di attività da svolgere e le esigenze che giustificano la spese. In caso di particolari situazioni d’urgenza che non consentano di attendere le decisioni dell’AD e che richiedano una risposta immediata, l’OdV è autorizzato a deliberare autonomamente, salvo l’obbligo di tempestiva comunicazione allo stesso organo di amministrazione;
- i componenti esterni dell’Organismo di Vigilanza dovranno essere retribuiti per l’attività di vigilanza svolta ai sensi dell’art. 6 del D.Lgs. 231/01. La remunerazione è costituita da un importo fisso annuo, che non dipende dai risultati economico/produttivi della Società. Per quanto riguarda il membro interno, l’Amministratore Delegato valuta l’attribuzione di un compenso ulteriore rispetto alla retribuzione annua già percepita in qualità di dipendente;
- l’OdV è dotato di ampi poteri ispettivi. A titolo esemplificativo e non esaustivo, lo stesso potrà: effettuare visite a qualsiasi ufficio della Società, accedere a qualsiasi archivio (cartaceo o telematico), banca dati e documento della Società, ottenere chiarimenti dai responsabili delle Direzioni aziendali. Le attività poste in essere dall’OdV non possono in alcun modo essere sindacate e/o contestate da alcuna funzione aziendale;
- fermo restando che la cadenza e le modalità di svolgimento delle riunioni sono oggetto di specifica trattazione all’interno del Regolamento adottato dallo stesso Organismo di Vigilanza, l’OdV dovrà riunirsi con cadenza trimestralmente;
- annualmente l’Organismo di Vigilanza trasmette al Consiglio di Amministrazione e al Collegio Sindacale una relazione sull’attuazione del Modello indicando l’attività svolta, le risultanze emerse e i suggerimenti in merito agli eventuali interventi correttivi e/o di aggiornamento da adottare. A questo proposito, l’Organismo può essere convocato dal Consiglio di Amministrazione e dal Collegio Sindacale in ogni circostanza in cui sia ritenuto necessario o opportuno per il corretto svolgimento delle funzioni di cui all’art. 6 del D.Lgs. 231/01.
L’OdV svolge in ogni caso le proprie funzioni nel pieno rispetto della legge, dei regolamenti, delle prescrizioni contenute nel presente Modello Organizzativo.
4.3. Il regolamento dell’OdV: rinvio.
Nell’ambito di quanto previsto dal Modello Organizzativo, l’Organismo di Vigilanza disciplina il proprio funzionamento per il tramite di un regolamento adottato a maggioranza assoluta dei propri componenti, al quale si rimanda integralmente. Tale documento stabilisce, tra le altre cose:
- la cause di ineleggibilità, incompatibilità e decadenza dei membri;
- le dimissioni e/o rinuncia all’incarico;
- la durata del mandato;
- le modalità operative delle riunioni e delle deliberazioni assunte nell’ambito delle stesse;
- i presidi adottati per garantire la piena tracciabilità delle attività svolte dall’Organismo di Vigilanza e la conservazione della documentazione esaminata e/o approvata dallo stesso.
- I FLUSSI INFORMATIVI ED I CANALI DI SEGNALAZIONE.
Uno dei requisiti essenziali per assicurare la continuità d’azione dell’Organismo di Vigilanza e l’efficacia di un sistema di gestione del rischio che prevenga o minimizzi il pericolo di commissione dei reati presupposto, è la predisposizione a livello aziendale di un sistema di flussi informativi che coinvolga l’OdV e tutte le Direzioni e/o funzioni della società. La previsione di flussi in entrata ed in uscita consente di dare attuazione “ad una gestione integrata” dei rischi che, come riconosciuto dalle Linee Guida di Confindustria, “si fonda anche su specifici e continui meccanismi di coordinamento e collaborazione tra i principali soggetti aziendali interessati tra i quali, a titolo esemplificativo, il Dirigente preposto, la funzione compliance, l’internal Audit, il Datore di Lavoro, il responsabile AML (per le imprese che ne sono tenute), il Collegio Sindacale (…) e l’OdV”.[18]
In questo senso, si possono distinguere:
- 5.1. le informazioni, dati e comunicazioni diretti all’OdV (c.d. flussi informativi in entrata);
- 5.2. le informazioni, dati e comunicazioni, trasmessi dall’OdV al vertice aziendale (c.d. flussi informativi in uscita).
5.1. I flussi informativi in entrata.
In linea con quanto affermato dalla giurisprudenza, i flussi informativi in entrata sono anzitutto costituiti dal complesso di informazioni, dati e comunicazioni che devono esser trasmessi da ciascun Responsabile di Direzione/Divisione o dagli ulteriori Organi di controllo all’OdV al fine di fornire “indicatori idonei a segnalare l’esistenza e l’insorgenza di situazioni di criticità generale e/o particolare, così da consentire all’Organismo stesso ed eventualmente agli altri coinvolti un monitoraggio continuo basato sull’analisi di potenziali red flag”.[19]
Tali flussi possono consistere o in report periodici inoltrati con una determinata cadenza – che descrivono, tra le altre cose, le eventuali anomalie o irregolarità riscontrate – o in rapporti specifici trasmessi in occasione di eventi rilevanti.[20] Nel primo caso, si parla di flussi in forma strutturata, nel secondo di flussi “ad evento”.
Tra i flussi informativi rientrano anche i dati e le informazioni raccolte dal QA al fine di dimostrare l’adeguatezza e l’efficacia del sistema di gestione della qualità implementato con specifico riguardo alla Divisione BIOSPA, qualora gli stessi identifichino “opportunità di miglioramento” connesse a rischi rilevanti ai sensi e per gli effetti del D.Lgs. 231/01. In questo senso, è portata a conoscenza dell’Organismo di Vigilanza la relazione riepilogativa che compendia tali dati o informazioni.[21] Tra gli ulteriori flussi informativi in entrata, particolare importanza rivestono:
- quelli in materia di salute e sicurezza sul lavoro, ad opera del Delegato ex art. 16 D.Lgs. 81/08, dell’RSPP, del Comitato Covid;
- quelli trasmessi dalla funzione preposta agli audit e l’OdV sulle risultanze delle rispettive attività di verifica che abbiano una rilevanza comune ai fini della normativa sulla responsabilità amministrativa degli Enti dipendente da reato.
Debbono considerarsi come flussi informativi “in entrata” anche le segnalazioni trasmesse dai dipendenti attraverso i canali implementati da Società Prodotti Antibiotici S.p.A. che, alla luce delle modifiche apportate all’art. 6 del D.Lgs. 231/01 dalla normativa in tema di whistleblowing, saranno oggetto di specifica ed approfondita trattazione.
5.2. I flussi informativi in uscita.
Per contro, i flussi informativi in uscita sono costituiti dall’insieme di informazioni che devono essere trasmesse dall’OdV al Consiglio di Amministrazione o all’Amministratore Delegato nonché al Collegio Sindacale,[22] concernenti il verbale delle attività di verifica e controllo svolte e le proposte migliorative sullo stato di attuazione del presente Modello Organizzativo. Tali comunicazioni devono essere accurate, chiare, concise, costruttive, complete e tempestive e devono, tra l’altro, contenere: (i) l’esito delle attività svolte, (ii) i fatti di particolare significatività, (iii) le notizie di eventuali violazioni del presente Modello Organizzativo, (iv) le informazioni in ordine all’irrogazione di sanzioni disciplinari conseguenti al procedimento di accertamento di violazione del Modello Organizzativo, come comunicate dai flussi informativi e/ verificate dall’OdV, ed, infine, (iv) l’avviso di mutamenti legislativi in materia di responsabilità amministrativa da reato degli enti, che comportano il costante aggiornamento del Modello.
L’OdV relaziona per iscritto, con cadenza annuale al Consiglio di Amministrazione sull’attività compiuta nel periodo e sull’esito della stessa, fornendo altresì un’anticipazione sulle linee generali di intervento per il periodo successivo. La relazione annuale avrà in particolare ad oggetto:
- l’attività svolta dall’OdV;
- le eventuali problematiche o criticità che si siano evidenziate nel corso dell’attività di vigilanza;
- le azioni correttive, necessarie o eventuali, da apportare al fine di assicurare l’efficacia e l’effettività del Modello, nonché lo stato di attuazione delle azioni correttive deliberate dal Consiglio di Amministrazione o dall’Amministratore Delegato;
- l’eventuale mancata o carente collaborazione da parte delle funzioni aziendali nell’espletamento dei propri compiti di verifica;
- qualsiasi informazione ritenuta utile ai fini dell’assunzione di determinazioni urgenti da parte degli organi deputati.
In ogni caso, l’OdV può rivolgersi al Consiglio di Amministrazione o all’Amministratore Delegato ogni qualvolta lo ritenga opportuno ai fini dell’efficace ed efficiente adempimento dei compiti ad esso assegnati. Gli incontri devono essere verbalizzati e le copie dei verbali devono essere conservate presso gli uffici dell’OdV.
5.3. Le segnalazioni all’OdV (whistleblowing).
L’Organismo di Vigilanza deve essere tempestivamente informato di condotte o eventi che potrebbero integrare una violazione e/o elusione del Modello o delle SOP in esso richiamate: a tal fine, Società Prodotti Antibiotici S.p.A. ha implementato un sistema di segnalazione che consente a tutti i dipendenti e/o collaboratori esterni di SPA di segnalare fatti e/o comportamenti illeciti o indebiti di cui siano venuti a conoscenza nell’esercizio delle proprie funzioni.
Come detto, possono e debbono essere segnalate tutte le condotte che, indipendentemente dalla illiceità penale, costituiscano una violazione delle disposizioni contenute nel Codice Etico, nel Modello di Organizzazione e Gestione o nelle standard operative procedures. Le segnalazioni debbono essere circostanziate e, qualora possibile, debbono indicare atti, documenti e/o ulteriori elementi in grado di corroborare o confermare quanto denunciato. Al contrario, non possono invece essere oggetto di segnalazione:
- rimostranze di carattere personale del segnalante;
- richieste che attengono alla disciplina del rapporto di lavoro o ai rapporti col superiore gerarchico o colleghi;
- valutazioni sull’operato professionale di colleghi non integranti violazioni della normativa;
- offese personali o giudizi morali volti ad offendere o screditare l’onore e/o il decoro personale e/o professionale della persona o delle persone a cui i fatti segnalati sono ascritti.
Quale organo destinatario delle segnalazioni e deputato alla loro istruzione e gestione è stato individuato l’Organismo di Vigilanza, che potrà essere contattato attraverso i due seguenti canali:
- a mezzo posta all’indirizzo: Organismo di Vigilanza di Società SPA – Società Prodotti Antibiotici S.p.A. ;
- a mezzo mail alla casella di posta dell’OdV ([email protected]).
Tale soluzione è coerente con le più recenti indicazioni delle linee guida emesse da Confindustria che, nel premettere come le scelte debbono essere calibrate sulle caratteristiche dimensionali ed organizzative dell’impresa, evidenziano che il destinatario delle segnalazioni può essere identificato anche con il predetto Organo:[23] soluzione, questa, del tutto “coerente con i compiti ad esso spettanti, nonché con gli obblighi di informazione nei suoi confronti previsti dal decreto 231”.
L’informazione ricevuta sarà trattata nel rispetto della normativa sulla protezione dei dati personali di cui al D. Lgs. 196/03 così come modificato dal D.Lgs. 10 agosto 2018, n. 101 e verrà conservata in forma cartacea o informatica.
L’Odv provvederà a mantenere massimo riserbo attorno alla identità del segnalante, fatti salvi gli obblighi di legge e la tutela dei diritti della Società o delle persone accusate in mala fede. A tal fine, i componenti dell’OdV sono obbligati a non rivelare all’esterno alcuna informazione o notizia appresa nell’esercizio delle proprie funzioni, salvo gli obblighi di denuncia o di comunicazione previsti dalla legge.
Tutte le segnalazioni ritenute rilevanti e debitamente circostanziate e/o motivate verranno prese in considerazione ed esaminate, in modo da predisporre le azioni opportune. Al fine di valutare come procedere, l’Organismo di Vigilanza potrà eventualmente ascoltare il responsabile della segnalazione o il responsabile della presunta violazione. Nel caso in cui l’OdV decidesse di non dar seguito alla segnalazione mediante indagini dovranno essere riferiti e documentati i motivi.
I segnalanti in buona fede saranno tutelati da qualsiasi forma di ritorsione, discriminazione o penalizzazione nei loro confronti e verranno protetti da atti quali:
- il demansionamento;
- la sospensione;
- il licenziamento (sia collettivo che individuale);
- altre misure organizzative aventi effetti negativi sulle condizioni di lavoro.
Qualora vengano assunte decisioni in tal senso, è previsto l’immediato reintegro del lavoratore segnalante e/o l’annullamento di ogni atto discriminatorio o ritorsivo.
In caso di segnalazioni palesemente ingiuriose, diffamatorie o calunniose – ove le stesse riportino informazioni false rese al fine di offendere volontariamente l’altrui reputazione – l’Organismo di Vigilanza trasmette gli atti al Responsabile del Settore Risorse Umane al fine di valutare l’avvio di eventuali procedimenti disciplinari nei confronti del soggetto segnalante.
- IL SISTEMA DISCIPLINARE ADOTTATO DA SOCIETA’ PRODOTTI ANTIBIOTICI S.P.A.
6.1. Premessa e principi generali del sistema disciplinare adottato da Società Prodotti Antibiotici S.p.A.
Altro- elemento particolarmente significativo per l’efficace attuazione di un Modello di Organizzazione e Gestione è costituito dalla predisposizione di sanzioni da applicare ai soggetti che violino le disposizioni contenute nello stesso o nei documenti in esso richiamati.
Al riguardo, l’art. 6 del D.Lgs. 231/01 stabilisce infatti che il Modello Organizzativo deve essere assicurato da “un sistema disciplinare idoneo a sanzionare il mancato rispetto delle misure indicate nel modello” commesse sia dai soggetti in posizione apicale che dai soggetti sottoposti all’altrui direzione o coordinamento, in assenza del quale non può essere riconosciuta efficacia esimente al sistema di gestione del rischio adottato dalla società (si veda, tra le tante, la sentenza emessa dal Tribunale di Milano in data 20 settembre 2004).
Il rispetto delle prescrizioni contenute nel Modello Organizzativo, nel Codice Etico e nelle SOP costituisce pertanto un dovere di tutti i dipendenti e dei soggetti che rivestono cariche sociali (compresi i componenti dell’Organismo di Vigilanza) e, dall’altro nonché un obbligo gravante sui soggetti terzi che entrano in contatto con la Società nell’esecuzione dei rapporti contrattuali con la stessa.
Importante evidenziare che l’adozione di provvedimenti sanzionatori prescinde dalla commissione di un reato e dalla pendenza di un procedimento penale davanti all’autorità Giudiziaria competente. Ed invero, anche qualora le condotte non integrino una delle fattispecie previste dal D.Lgs. 231/01, le violazioni dei predetti documenti sono infatti astrattamente idonee a ledere il rapporto fiduciario instauratosi tra la Società oltre che l’immagine della Società medesima. Tale soluzione è conforme alle Linee Guida delle Associazioni di Categoria – alla stregua delle quali il sistema disciplinare “si affianca a quello esterno (penale o amministrativo), volto a sanzionare il trasgressore del Modello organizzativo indipendentemente dal fatto che, da quella violazione, sia scaturita la commissione di un reato”.[24] Le violazioni sanzionabili possono essere suddivise in quattro categorie secondo un ordine di gravità crescente:
- violazioni non connesse ad attività sensibili;
- violazioni connesse ad attività sensibili;
- violazioni idonee ad integrare uno dei reati presupposto previsti dal D.Lgs. 231/01 ed a comportare, per l’effetto, la responsabilità amministrativa dell’ente;
- violazioni finalizzate alla commissione di uno dei reati presupposto.
Fermo restando che l’Organismo di Vigilanza provvede a segnalare all’organo dirigente (o alle competenti funzioni e/o responsabili aziendali) ogni violazione di cui sia venuto a conoscenza, per l’accertamento e la contestazione delle infrazioni restano validi i poteri già conferiti al management aziendale ed eventualmente al Consiglio di Amministrazione/Amministratore Delegato, che dovranno comunque mantenere informato l’Organismo di Vigilanza di ogni procedimento disciplinare che sia stato attivato e dei provvedimenti adottati all’esito dello stesso.
L’irrogazione delle sanzioni disciplinari avviene nel rispetto delle procedure di cui all’art. 7 L. 30 maggio 1970 n. 300 nonché in accordo ai principi di conoscenza e/o conoscibilità, proporzionalità, progressività e tempestività.[25] In particolare:
- presupposto essenziale per esercitare la potestà punitiva è che la norma violata sia conosciuta o conoscibile da parte dei destinatari. A questo proposito, al fine di favorire la piena “diffusione di quanto stabilito dal Decreto e dal Modello adottato”, Società Prodotti Antibiotici S.p.A. ha previsto diversi strumenti. In particolare, (a) nell’ “intranet aziendale” è disponibile una copia telematica del Modello di Organizzazione e Gestione e del Codice Etico adottati del Consiglio di Amministrazione nonché di tutte le standard operative procedures che regolamentano i processi aziendali; (b) come si dirà nel prosieguo, sia a favore dei soggetti in posizione apicali sia di quelli sottoposti alla direzione ed al coordinamento di questi ultimi sono previsti corsi di formazione obbligatori corredati da un test finale di valutazione e di comprensione.
- conformemente a quanto stabilito dalla Corte Costituzionale, “il tipo e l’entità delle sanzioni specifiche” sono applicati in proporzione alla gravità delle infrazioni e in considerazione di una serie di elementi espressamente stabiliti. Nello specifico, occorrerà valutare:
- (i) l’intenzionalità del comportamento o il grado di negligenza, imprudenza o imperizia, con riguardo anche alla prevedibilità dell’evento;
- (ii) la condotta complessiva del lavoratore, con particolare riguardo alla sussistenza o meno di precedenti disciplinari o di violazioni commesse dal medesimo;
- (iii) le mansioni del lavoratore;
- (iv) la posizione funzionale delle persone coinvolte nei fatti costituenti la mancanza;
- (v) le altre particolari circostanze che accompagnino la violazione disciplinare.
- sempre riprendendo la chiara sentenza della Corte Costituzionale,[26] le sanzioni devono essere “graduate in ragione della gravità delle violazioni accertate spaziando da misure conservative, per le infrazioni più tenui, a provvedimenti idonei a recidere il rapporto tra l’agente e l’ente, nel caso di violazioni più gravi”;[27]
- l’irrogazione della sanzione disciplinare deve poi, per quanto possibile, essere “ispirata ai principi di tempestività” (requisito sempre ripreso dalla citata sentenza della Corte Costituzionale che parla di “contestazione dell’addebito tempestiva e specifica”);
- infine, deve essere rispettato il principio del contraddittorio, “assicurando il coinvolgimento del soggetto interessato: formulata la contestazione dell’addebito, tempestiva e specifica, occorre dargli la possibilità di addurre giustificazioni a difesa del suo comportamento”.[28]
6.2. Le diverse parti del sistema disciplinare.
Il sistema disciplinare risulta in particolare suddiviso in quattro parti:
6.2.1. la prima relativa alle sanzioni irrogabili ai dipendenti in posizione subordinata che non ricoprono ruoli apicali;
6.2.2 la seconda concernente le violazioni commesse da parte dei soggetti in posizione apicale o di coloro che ricoprono cariche sociali;
6.2.3 la terza, avente ad oggetto le violazioni poste in essere da soggetti terzi che collaborano con SPA – Società Prodotti Antibiotici S.p.A.;
6.2.4 la quarta, riguardante il procedimento disciplinare.
6.2.1. Le sanzioni applicabili ai dipendenti che non ricoprono ruoli apicali.
L’osservanza delle disposizioni e delle regole comportamentali previste dal Modello di Organizzazione e Gestione da parte dei dipendenti di Società Prodotti Antibiotici S.p.A. costituisce adempimento degli obblighi previsti dall’art. 2104, comma 2, c.c., di cui il Modello rappresenta parte sostanziale ed integrante.
Le sanzioni irrogabili agli stessi, in conformità all’art. 7 della L. 20.5.1970 n. 300 (Statuto dei Lavoratori),[29] per le accertate violazioni del Modello Organizzativo, sono:
- il biasimo verbale, nei casi delle violazioni più lievi alle prescrizioni del Modello Organizzativo (ad esempio soggetto che non osservi alcuni passaggi delle SOP concernenti i processi non sensibili, ometta di inviare all’OdV i flussi informativi periodici, non svolga una verifica alla quale è deputato);
- il biasimo scritto, nei casi di violazioni meno lievi di quelle sanzionabili con il biasimo verbale, ma meno gravi di quelle per le quali sia prevista la multa (recidiva nella violazione delle SOP aventi ad oggetto attività non sensibili, violazione una tantum di procedure e/o disposizioni relative a processi sensibili);
- la multa in misura non eccedente l’importo di 4 ore della normale retribuzione di cui all’art. 185 del C.C.N.L., nel caso di violazioni alle prescrizioni del Modello Organizzativo e delle SOP adottate in relazione a processi non sensibili che denotino negligenza da parte del dipendente e che siano tali da esporre l’integrità dei beni e/o della reputazione aziendale ad una situazione di oggettivo pericolo;
- la sospensione dalla retribuzione e dal servizio per un massimo di giorni 10, nel caso di violazioni alle prescrizioni del Modello Organizzativo e delle SOP adottate in relazione a processi sensibili che arrechino, anche potenzialmente, danno alla Società od al Gruppo cui essa appartiene. La sospensione è altresì disposta nei confronti dei soggetti che pongano in essere atti discriminatori e/o ritorsivi nei confronti di coloro che abbiano provveduto ad inviare segnalazioni all’OdV così come nei confronti di chi abbia inoltrato segnalazioni false o calunniose con dolo o colpa grave.
- Il licenziamento con preavviso in caso di reiterate violazioni (per oltre la terza volta nel biennio) commesse nell’ambito di processi aziendali sensibili o di comportamenti diretti in modo diretto e univoco alla commissione di una delle fattispecie previste e punite dagli artt. 24 ss. del D.Lgs. 231/01. Il licenziamento è altresì disposta nei confronti dei soggetti che: (a) dissuadano i dipendenti dal segnalare condotte illecite o poste in essere in violazione del Modello di Organizzazione e Gestione o delle procedure; (b) pongano reiteratamente in essere atti discriminatori e/o ritorsivi nei confronti di coloro che abbiano provveduto ad inviare segnalazioni all’OdV (c) inoltrino plurime segnalazioni false o calunniose con dolo o colpa grave.
- licenziamento senza preavviso nel caso di comportamento non conforme che integri gli estremi di uno dei reati presupposto e che sia tale da determinare la concreta applicazione a carico della società delle misure previste dal D.Lgs. 231/01 o che rappresenti la terza violazione commessa in relazione ad attività sensibili nell’arco di un anno solare, tale da far venire radicalmente meno la fiducia della società nei confronti del lavoratore e da causare un grave nocumento alla stessa. Il licenziamento senza preavviso è altresì disposto nei confronti di chi ponga in essere condotte fraudolente dolosamente preordinate ad aggirare i presidi implementati dalla società e ad indurre in errore gli organi di controllo. A titolo esemplificativo e non esaustivo:
- falsificazione della documentazione delle operazioni compiute nelle ispezioni;
- distruzione, occultamento o alterazione della documentazione aziendale;
- falsificazione delle relazioni e/o informazioni trasmesse al CdA o all’OdV;
- falsa comunicazione al CdA o all’OdV, alle scadenze stabilite, dell’elenco delle attività di consulenza gestite in deroga ai principi standard;
- doloso ostacolo alle altrui funzioni di controllo o impedimento di accesso a documenti aziendali a soggetti aventi titolo.
6.2.2. Le sanzioni applicabili ai soggetti in posizione apicale ed ai soggetti che ricoprono cariche sociali.
(a) Le sanzioni applicabili ai soggetti in posizione apicale.
Qualora la violazione venga posta in essere da parte di dirigenti o da soggetti che, per quanto non inquadrati come tali, svolgano funzioni di “direzione e coordinamento”, Società Prodotti Antibiotici S.p.A. adotta la misura ritenuta più idonea in conformità a quanto previsto dal CCNL applicabile. A tal proposito, i dipendenti in posizione apicale di SPA – Società Prodotti Antibiotici S.p.A. potranno essere sanzionati, a titolo esemplificativo e non esaustivo:
- per le violazioni già descritte nel paragrafo precedente (cui si rimanda integralmente);
- per le specifiche violazioni in materia di sicurezza del lavoro e di tutela della salute secondo le attribuzioni, competenze e responsabilità eventualmente conferite o delegate al singolo soggetto dal D.Lgs. 81/08:
- per l’omessa trasmissione dei flussi informativi periodici all’Organismo di Vigilanza o per il mancato inoltro di segnalazioni aventi ad oggetto condotte illecite e/o violazioni di cui gli stessi siano venuti a conoscenza nell’esercizio delle proprie funzioni;
- per condotte ritorsive e/o discriminatorie ai danni di soggetti che abbiano inviato una segnalazione all’Organismo di Vigilanza o per la violazione del principio di riservatezza in ordine all’identità del soggetto segnalante;
- per altre violazioni non rientranti tra quelle sopra elencate, ma aventi, per le loro caratteristiche ed in relazione al caso concreto, analoga gravità.
Qualora l’accertata violazione da parte del soggetto in posizione apicale, non sia lieve, ma non abbia gravità tale da comportare la adozione del licenziamento, essa, in relazione alla entità della violazione ed alle circostanze che l’accompagnano:
- sarà considerata in sede di valutazione annuale delle prestazioni quale elemento negativo ai fini del raggiungimento degli obiettivi individuali prefissati e/o della spettanza, o determinazione della misura, della retribuzione variabile eventualmente prevista dal contratto individuale, dalla contrattazione collettiva o da regolamenti e usi aziendali;
- potrà comportare la revoca, totale o parziale, delle eventuali procure o deleghe di funzioni, con perdita del relativo eventuale specifico compenso.
Qualora la accertata violazione da parte del soggetto in posizione apicale sia di gravità tale da far venire meno il vicolo fiduciario e da non consentire quindi la prosecuzione del rapporto di lavoro, verrà adottato il provvedimento del licenziamento con preavviso, ai sensi dell’art. 35, co. 5 ss., del vigente c.c.n.l. applicabile al rapporto di lavoro del Dirigente (terziario, distribuzione e servizi).
Nel caso invece in cui l’accertata predetta violazione, in relazione al caso concreto, per la sua gravità o reiterazione sia tale, oltre che a ledere irreparabilmente il vincolo fiduciario, da non consentire la prosecuzione neppure provvisoria del rapporto di lavoro, verrà adottato il provvedimento del licenziamento per giusta causa ex art. 2119 c.c.
(b) Le sanzioni applicabili ai soggetti che ricoprono cariche sociali.
Se la violazione del Modello di Organizzazione e Gestione, del Codice Etico o delle SOP è attribuibile ad uno dei componenti degli organi amministrativi e/o di controllo della società, l’Organismo di Vigilanza, anche in via disgiunta, deve tempestivamente informare il CdA, il Collegio Sindacale ed il Responsabile delle Risorse Umane. I soggetti che ricoprono cariche sociali di SPA potranno essere sanzionati:
- per le violazioni già descritte nei paragrafi precedenti;
- per il mancato aggiornamento e/o modifica del Modello di Organizzazione e Gestione, del Codice Etico e delle SOP, pur a fronte di motivata richiesta da parte dell’Organismo di Vigilanza;
- per la mancata eliminazione delle violazioni del Modello Organizzativo;
- per condotte ritorsive e/o discriminatorie ai danni di soggetti che abbiano inviato una segnalazione all’Organismo di Vigilanza o per la violazione del principio di riservatezza in ordine all’identità del soggetto segnalante;
- per il mancato adempimento, per negligenza o imperizia, degli obblighi di direzione o vigilanza di cui all’art. 7, comma 1, D.Lgs. 231/01;
- per altre violazioni non rientranti tra quelle sopra elencate, ma aventi, per le loro caratteristiche ed in relazione al caso concreto, analoga gravità.
Le sanzioni irrogabili ai soggetti che ricoprono cariche sociali possono essere, oltre a quelle già menzionate:
- illa perdita parziale o totale della eventuale retribuzione variabile (bonus, compensi legati ad obiettivi e simili);
- la sanzione pecuniaria di importo da determinarsi tra il 10% ed il 50% del compenso fisso annuale;
- la revoca parziale delle eventuali procure o deleghe di funzioni, con perdita del relativo eventuale specifico compenso;
- la revoca dell’incarico, con perdita dell’eventuale compenso.
Qualora il soggetto sia incorso in una violazione di gravità tale da imporre la revoca parziale o totale delle procure o deleghe di funzioni o dello stesso incarico, la Società potrà disporne la sospensione cautelare con effetto immediato. Nel caso in cui alla sospensione segua la revoca, quest’ultima avrà effetto dal giorno in cui ha avuto inizio la sospensione cautelare.
6.2.3. Le sanzioni applicabili ai soggetti e/o società terze che collaborano con Società Prodotti Antibiotici S.p.A.
Oltre a prevedere sanzioni in capo ai dipendenti di Società Prodotti Antibiotici S.p.A. o a coloro che ricoprano una carica sociale, il codice disciplinare prevede che anche i terzi che collaborano a vario titolo con la Società possano essere sanzionati per le violazioni del Codice Etico, del Modello di Organizzazione e Gestione o delle procedure e/o istruzioni operative in essi richiamate. La soluzione è conforme alle più recenti linee guida adottate da Confindustria che, sul punto, precisano come “si possono ipotizzare sanzioni quali la diffida al puntuale rispetto del modello, l’applicazione di una penale o la risoluzione del contratto che lega l’impresa al terzo, a seconda della gravità della violazione contestata”. A questo proposito “occorre inserire nel contratto apposite clausole, volte a prevedere la dichiarazione della controparte di astenersi dal porre in essere comportamenti che possano integrare una fattispecie di reato contemplata dal D. Lgs. 231/2001, nonché l’impegno a prendere visione delle misure definite dall’ente (ad es. modello, codice etico), al fine di promuovere anche l’eventuale definizione di ulteriori e più efficaci strumenti di controllo”.[30]
. Nel caso di violazioni commesse da terzi estranei alla Società e salvo specifiche statuizioni contrattuali, le sanzioni potranno essere:
- la perdita del diritto a sconti e/o a condizioni contrattuali di particolare favore previsti nei contratti stipulati tra le parti;
- la cancellazione temporanea dall’albo dei fornitori/consulenti della Società o del Gruppo;
- la cessazione del rapporto con il terzo e/o la cancellazione dello stesso dall’albo dei fornitori/consulenti della Società e/o del Gruppo.
6.2.4. Brevi cenni sul procedimento disciplinare.
Ferma restando la diversità di sanzioni applicabili, il procedimento disciplinare per le violazioni del Modello di Organizzazione e Gestione, del Codice Etico e delle Standard Operative Procedures è il medesimo per tutti i dipendenti di Società Prodotti Antibiotici S.p.A.
Ad ogni notizia di violazione, verrà promossa un’azione disciplinare finalizzata all’accertamento dell’effettiva sussistenza della violazione stessa, formulando nei confronti del soggetto coinvolto un addebito specifico e garantendo un congruo termine per addurre elementi a difesa. In questo senso, Società Prodotti Antibiotici S.p.A. assicura il rispetto delle disposizioni e delle garanzie previste dall’art. 7 dello Statuto dei Lavoratori. In particolare:
- non può essere adottato alcun provvedimento disciplinare senza aver preventivamente contestato al dipendente le condotte poste in essere in violazione delle vigenti disposizioni di legge o della normativa interna;
- per le violazioni che possano comportare un provvedimento più grave del biasimo verbale, SPA è tenuta sempre a trasmettere e/o consegnare una contestazione scritta che contenga la descrizione degli addebiti;
- deve essere garantito un termine per consentire al dipendente di raccogliere e produrre elementi a sua difesa, prima del quale non è consentita l’emissione di alcun provvedimento disciplinare;
- il provvedimento disciplinare o l’eventuale ulteriore decisione a definizione del procedimento disciplinare deve essere emessa entro un termine specifico (in particolare entro 16 giorni dalla data della contestazione);
- qualora la violazione sia di gravità tale da poter condurre al licenziamento, il dipendente può essere sospeso cautelativamente fino al momento della definizione del procedimento disciplinare;
- il provvedimento con il quale si commina una sanzione disciplinare deve essere adeguatamente motivato e deve indicare le ragioni in fatto ed in diritto poste alla base dello stesso;
- i provvedimenti disciplinari potranno essere impugnati dal lavoratore nelle opportune sedi (sindacale o giudiziaria) in ottemperanza alla normativa vigente.
L’Organismo di Vigilanza dovrà essere tempestivamente informato delle contestazioni avanzate nei confronti di dipendenti della Società, venendo aggiornato sull’evoluzione e sull’esito del procedimento. Sulla base delle circostanze segnalate, l’OdV dovrà peraltro procedere a valutare l’efficacia e l’idoneità delle procedure e/o delle istruzioni operative aventi ad oggetto l’ambito di attività nel quale è stata commessa la violazione contestata. In questo senso, laddove ne ravvisi i presupposti e l’opportunità, potrà al Consiglio di Amministrazione ed all’Amministratore Delegato l’integrazione, modifica ed implementazione delle SOP adottate internamente.
In caso di violazioni commesse da soggetti terzi (consulenti, partner commerciali etc.), l’ufficio che gestisce i rapporti con questi ultimi, in coordinamento con del Responsabile della Direzione Risorse Umane e con le ulteriori funzioni aziendali eventualmente identificate:
- contesterà per iscritto al terzo le violazioni;
- invierà quanto pervenuto al proprio Responsabile o ad eventuali altri Direttori/Responsabili, che potranno trasmettere eventuali osservazioni;
- valuterà le osservazioni dei predetti soggetti prima di adottare le misure più opportune tra quelle previste nel paragrafo, 5.2.3. tenendo altresì conto delle caratteristiche del contratto e/o della relativa tipologia contrattuale.
- L’APPROVAZIONE, LA MODIFICA E L’INTEGRAZIONE DEL MODELLO DI ORGANIZZAZIONE E GESTIONE.
Conformemente a quanto stabilito dall’art. 6, comma primo, lett. a) del D.Lgs. 231/01 – che qualifica il Modello di Organizzazione e Gestione come un atto di emanazione dell’Organo dirigente – il presente documento è approvato dal Consiglio di Amministrazione di Società Prodotti Antibiotici S.p.A., che dovrà altresì formalmente provvedere ad approvare tutte le successive modifiche e integrazioni.
Le deliberazioni in ordine alla modifica del Modello sono assunte su proposta dell’Organismo di Vigilanza, che provvede periodicamente alla verifica dell’idoneità ed adeguatezza del sistema di gestione del rischio implementato dalla società, individuando gli interventi da realizzare. In questo senso, il Modello di Organizzazione e Gestione, dovrà essere tempestivamente integrato a cura dell’OdV:
- in occasione di interventi normativi e/o di significativi arresti giurisprudenziali che interessino la disciplina prevista dal D. Lgs. 231/01;
- a fronte di mutamenti nell’assetto interno della Società o nelle modalità di svolgimento delle attività d’impresa;
- laddove vengano commesse gravi violazioni del Modello Organizzativo, del Codice Etico e/o delle SOP che – a prescindere dalla successiva attivazione di un procedimento penale – ne mettano in discussione l’idoneità o l’efficacia.
Nel procedere a tali modifiche, l’OdV– nei limiti del budget attribuito – potrà inoltre avvalersi di professionisti terzi.
Se le modifiche legate ad interventi normativi, all’identificazione di nuove attività sensibili, alla commissione di reati presupposto o al riscontro di gravi carenze e/o lacune debbono sempre essere oggetto di un’apposita delibera del C.d.A., le variazioni meramente formali o descrittive potranno essere autonomamente apportato dallo stesso Organismo di Vigilanza. Con la predetta espressione, si fa riferimento ad elementi o informazioni che si possono trarre da atti deliberati dal Consiglio di Amministrazione o dalle competenti funzioni aziendali (come, ad esempio, eventuali ridefinizioni dell’organigramma o nuove procedure).
Il Modello di Organizzazione e Gestione sarà in ogni caso sottoposto ad un procedimento di revisione periodica con cadenza biennale da disporsi attraverso un’apposita delibera del Consiglio di Amministrazione.
- LA DIFFUSIONE DEL MODELLO DI ORGANIZZAZIONE E GESTIONE E LA FORMAZIONE DEL PERSONALE.
Affinché il Modello di Organizzazione e Gestione possa essere efficacemente attuato nell’ambito dell’azienda e non rimanga un presidio meramente formale, è essenziale che i principi e le disposizioni in esso contenute siano perfettamente conosciuti dai dipendenti e dai soggetti che – pur non essendo formalmente tali – operano (anche occasionalmente e non continuativamente) per il conseguimento degli obiettivi sociali. D’altronde, come evidenziato nel Manuale della Qualità adottato nell’ambito della Divisione BIOSPA, il livello di qualificazione e di addestramento del personale “costituisce per l’organizzazione un patrimonio prezioso, oltre che una garanzia di credibilità e professionalità, e pertanto risulta opportuno curarlo e seguirlo con particolare impegno e dedizione”. Per questo, è essenziale assicurare che i dipendenti siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”. [31]
Ai fini di una capillare diffusione del Codice Etico e del Modello di Organizzazione e Gestione:
- a tutti i dipendenti – siano essi componenti degli organi amministrativi e/o di controllo, soggetti in posizione apicale o sottoposti all’altrui direzione o coordinamento – sarà data comunicazione iniziale circa l’adozione degli stessi, nelle forme ritenute più appropriate (ad es. attraverso avvisi in bacheca, tramite intranet, etc.);
- verranno fornite le necessarie indicazioni per avere accesso ad una copia aggiornata del Modello Organizzativo e dei documenti in esso richiamati;
- ai nuovi assunti sarà data comunicazione dell’avvenuta adozione del Codice Etico e del Modello di Organizzazione e Gestione all’atto dell’assunzione, spiegandone caratteristiche e finalità e facendo sottoscrivere al soggetto una sintetica informativa per presa visione;
- le comunicazioni al personale effettuate via intranet e relative ad eventuali modifiche del Modello Organizzativo o delle procedure e/o istruzioni operative in esso richiamate saranno trasmesse con comunicazioni telematiche che – oltre a garantire sia la sicurezza d’accesso al sistema, sia la riservatezza delle informazioni – recheranno un avviso di lettura per essere certi della corretta ricezione;
- il Direttore o il soggetto la cui attività comporti rapporti con soggetti terzi (fornitori, particolare clientela, collaboratori), informeranno i collaboratori ed i terzi sull’avvenuta adozione del Modello Organizzativo da parte della Società. In questo senso, la società valuterà l’inserimento di apposite clausole contrattuali che sanzionino condotte poste in essere in violazione dei principi e delle disposizioni contenute nel Modello Organizzativo o nel Codice Etico.
- Il Responsabile della Direzione Risorse Umane provvederà, inoltre, ad assicurare la conoscenza o conoscibilità del correlato aggiornamento del codice disciplinare previsto dal c.c.n.l (così come richiamato nel paragrafo che precede).
Al di là di tali iniziative, come evidenziato dalle Linee Guida di Confindustria “deve essere sviluppato un adeguato programma di formazione modulato in funzione dei livelli dei destinatari” che “deve illustrare le ragioni di opportunità – oltre che giuridiche .- che ispirano le regole e la loro portata concreta”.[32] In questo senso, Società Prodotti Antibiotici S.p.A. promuove ed agevole la formazione di tutto il personale aziendale (compresi anche i soggetti che operano nell’ambito dell’informazione scientifica) rispetto ai contenuti ed ai principi del Modello e del Codice Etico, organizzando corsi e/o attività di training caratterizzate da un grado di approfondimento diversificato a seconda della posizione ricoperta dai dipendenti e dalla maggiore o minore esposizione al rischio.
In questo senso, il Responsabile della Direzione Risorse Umane – di concerto con l’Organismo di Vigilanza e con il QA – definisce la cadenza degli incontri di formazione finalizzati alla sensibilizzazione del personale, potendo avvalersi, laddove necessario, dell’ausilio di un professionista terzo esperto di responsabilità amministrativa degli Enti dipendente da reato. Ferme restando le differenze ed i diversi gradi di approfondimento, nel corso degli incontri dovranno essere trattati:
- i principi fondamentali alla base del D.Lgs. 231/01 e le conseguenze derivanti in capo alla società dall’eventuale commissione dei reati presupposto da parte di soggetti apicali o subordinati che agiscano nell’interesse o a vantaggio della stessa;
- la struttura del Modello di Organizzazione e Gestione adottato da SPA e la centralità dello stesso nel sistema di “autonormazione” in grado di provare l’estraneità dell’ente rispetto all’illecito;
- i processi sensibili che, alla luce delle caratteristiche di SPA e dell’attività aziendale, presentano un maggiore rischio di commissione dei reati presupposto.
Così come per le ulteriori attività di formazione disposte da Società Prodotti Antibiotici a favore dei propri dipendenti, anche i training aventi ad oggetto il Modello Organizzativo ed il Codice Etico sono obbligatori e prevedono la compilazione di un questionario o di un test di valutazione finale che attesti la frequentazione del corso e la piena comprensione dei contenuti illustrati. Qualora si ravvisi la mancata partecipazione di un soggetto che avrebbe dovuto frequentare il corso e/o l’assenza di attestazione che certifichi il superamento degli eventuali test di apprendimento, il Responsabile della Direzione Risorse Umane, di concerto con il Direttore e/o Responsabile di volta in volta interessato, provvede a riprogrammare il training o ad assumere le opportune iniziative concernenti il lavoratore non adeguatamente formato.
Con riferimento ai Responsabili delle Direzioni che si occupano di gestire le attività maggiormente sensibili alla commissione di reati presupposto, la società potrà valutare l’opportunità di trasmettere periodicamente questionari da trasmettere per via telematica, in modo da valutare periodicamente il livello di conoscenza dei principi che fondano il “sistema 231”.
NOTE
[1] Secondo l’impostazione tradizionale, elaborata con riferimento ai delitti dolosi, l’interesse ha un’indole soggettiva. Si riferisce alla sfera volitiva della persona fisica che agisce ed è valutabile al momento della condotta: la persona fisica non deve aver agito contro l’impresa. Se ha commesso il reato nel suo interesse personale, affinché l’ente sia responsabile è necessario che tale interesse sia almeno in parte coincidente con quello dell’impresa (cfr. anche Cass., V Sez. pen., sent. n. 40380 del 2012). Al riguardo, si segnala il recente orientamento della Cassazione che sembra evidenziare la nozione di interesse anche in chiave oggettiva, valorizzando la componente finalistica della condotta (Cass., II Sez. pen., sent. n. 295/2018; Cass., IV Sez. pen., sent. n. n. 3731/2020).
Per contro, il vantaggio si caratterizza come complesso dei benefici – soprattutto di carattere patrimoniale – tratti dal reato, che può valutarsi successivamente alla commissione di quest’ultimo (cfr. anche Cass., II Sez. pen., sent. n. 295/2018), anche in termini di risparmio di spesa (cfr. anche Cass., IV Sez. pen., sent. n. 31210/2016, Cass., IV Sez. pen., sent. n. n. 3731/2020).
Sul punto, si rimanda alle linee guida di Confindustria così come aggiornate al giugno 2021 (pp.6-7).
[2] Pagg. 10-11 delle citate Linee Guida.
[3] Come evidenziato da Confindustria, “il legislatore ha seguito un approccio sinergico in tema di sistemi di minimizzazione e gestione dei rischi per la salute e la sicurezza dei lavoratori, intrecciando la disciplina prevenzionistica del decreto 81 con quella della responsabilità degli Enti”.
[4] Ufficio Indagini preliminari Milano, 8 gennaio 2010, Foro ambrosiano 2010, 3, 350 (nota di: FUSCO; CAMERA)
[5] Si rimanda a pag. 39 delle Linee guida per la costruzione dei Modelli di Organizzazione, Gestione e Controllo, parte generale (così come aggiornate al giugno 2021).
[6] Vedi nota precedente.
[7] Nel caso di società di capitali, gli obblighi concernenti l’igiene e la sicurezza del lavoro gravano su tutti i componenti del Consiglio di amministrazione. La Corte di Cassazione ha infatti evidenziato che “la delega di gestione, in proposito conferita ad uno o più amministratori, se specifica e comprensiva di poteri di deliberazione e spesa, può solo ridurre la portata della posizione di garanzia attribuita agli ulteriori componenti del Consiglio, ma non escluderla interamente, poiché non possono comunque essere trasferiti i doveri di controllo sul generale andamento della gestione e di intervento, soprattutto nel caso di mancato esercizio della delega” [Cassazione penale sez. IV, 11 dicembre 2007, n. 6280].
[8] Secondo la norma, il “datore di lavoro” è il “il soggetto titolare del rapporto di lavoro con il lavoratore o, comunque, il soggetto che, secondo il tipo e l’assetto dell’organizzazione nel cui ambito il lavoratore presta la propria attivita’, ha la responsabilita’ dell’organizzazione stessa o dell’unita’ produttiva in quanto esercita i poteri decisionali e di spesa”.
[9] Addirittura, la Corte di Cassazione, in una recente sentenza, ha rilevato che “la mancanza di deleghe di funzioni, nei termini sopra indicati, è fatto che di per sé prova la mancanza di un efficace modello organizzativo adeguato a prevenire la consumazione del reato da parte dei vertici societari” (Cass. pen., sez. III, 12 gennaio 2017 n. 9132)
[10] I principi di controllo riportati nel presente paragrafo rispondono a quelli indicati nelle Linee Guida di Confindustria, parte generale: pagg. 58-59.
[11] Vedi pag. 41 delle Linee Guida di Confindustria così come aggiornate nel giugno 2021.
[12] Pag. 51 delle linee guida di Confindustria.
[13] P. 78 delle Linee Guida per la costruzione dei Modelli di Organizzazione, Gestione e Controllo (aggiornati al giugno 2021).
[14] La giurisprudenza ha infatti evidenziato che, per essere efficiente e funzionale “l’organismo di controllo non dovrà avere compiti operativi che, facendolo partecipe di decisioni dell’attività dell’ente, potrebbero pregiudicare la serenità di giudizio al momento delle verifiche” (G.i.p. Tribunale Roma, 4 aprile 2003).
[15] Pag. 78 delle Linee Guida elaborate da Confidustria.
[16] Pag. 79 delle Linee Guida elaborate da Confidustria.
[17] Vedi nota precedente.
[18] Pagg. 42 e 43 delle Linee Guida di Confindustria per la costruzione di Modelli di Organizzazione, Gestione e Controllo, parte generale (versione aggiornata a giugno 2021) .
[19] Pag. 43 delle predette Linee Guida.
[20] Secondo quanto precisato dalla Linee Guida di Confindustria, le informazioni da trasmettere all’Odv potranno riguardare, ad esempio:
- le decisioni relative alla richiesta, erogazione e utilizzo di finanziamenti pubblici;
- le richieste di assistenza legale inoltrate dai dirigenti e/o dai dipendenti nei confronti dei quali la Magistratura procede per i reati previsti dalla richiamata normativa;
- i provvedimenti e/o notizie provenienti da organi di polizia giudiziaria, o da qualsiasi altra autorità, dai quali si evinca lo svolgimento di indagini, anche nei confronti di ignoti, per i reati di cui al decreto 231;
- le commissioni di inchiesta o relazioni interne dalle quali emergano responsabilità per le ipotesi di reato di cui al decreto 231;
- le notizie relative alla effettiva attuazione, a tutti i livelli aziendali, del modello organizzativo, con evidenza dei procedimenti disciplinari svolti e delle eventuali sanzioni irrogate ovvero dei provvedimenti di archiviazione di tali procedimenti con le relative motivazioni;
- gli esiti dei controlli – preventivi e successivi – che sono stati effettuati nel periodo di riferimento, sugli affidamenti a operatori del mercato, a seguito di gare a livello nazionale ed europeo, ovvero a trattativa privata;
- gli esiti del monitoraggio e del controllo già effettuato nel periodo di riferimento, sulle commesse acquisite da enti pubblici o soggetti che svolgano funzioni di pubblica utilità.
(Linee Guida di Confindustria per la costruzione dei Modelli di Organizzazione, Gestione e Controllo, parte generale. P. 90).
[21] Si rimanda alle pagg. 33-34 del Manuale della Qualità adottato in relazione alla Divisione BIOSPA.
[22] Secondo quanto precisato dalle Linee Guida di Confindustria, “con riferimento ai flussi informativi tra gli organi di controllo, l’OdV è destinatario di flussi ad evento da parte del Collegio Sindacale, nel caso esso rilevi carenze e violazioni che presentino rilevanza sotto il profilo del Modello Organizzativo 231, nonché di ogni fatto o anomalia riscontrati che rientrino nell’ambito dei processi valutati come sensibili per la commissione dei reati presupposto (p. 90 delle richiamate Linee Guida aggiornate al giugno 2021).
[23] Secondo le linee guida di Confindustria, a titolo esemplificativo, il destinatario potrebbe essere il seguente:
- l’Organismo di Vigilanza ovvero un altro soggetto, comitato, struttura specificamente individuato;
- il responsabile della funzione compliance;
- un comitato rappresentato da soggetti appartenenti a varie funzioni (ad esempio legale, internal audit, compliance, HR);
- un ente o soggetto esterno dotato di comprovata professionalità, che si occupi di gestire la prima fase di ricezione delle segnalazioni in coordinamento con l’ente;
- il datore di lavoro nelle PMI.
(cfr. pag. 60 delle Linee Guida di Confindustria così come aggiornate nel giugno 2021).
[24] Si rimanda sia alle Linee Guida elaborate da Confindustria che alle indicazioni contenute nel documento elaborato dal Consiglio Nazionale dei Dottori Commercialisti e degli Esperti Contabili.
In particolare: “un sistema disciplinare volto a sanzionare comportamenti già di per sé costituenti reato finirebbe per duplicare inutilmente le sanzioni poste dall’ordinamento statale (pena per la persona fisica e sanzione ex decreto 231 per l’ente). Invece, ha senso prevedere un apparato disciplinare se questo opera come presidio interno all’impresa, che si aggiunge e previene l’applicazione di sanzioni “esterne” da parte dello Stato” (p. 71 delle Linee Guida elaborate da Confindustria per la costruzione dei modelli di organizzazione, gestione e controllo” (aggiornate al giugno 2021).
[25] Vedi nota precedente.
[26] Cfr. nota 27 che fa riferimento alla sentenza n. 20/95 della Corte Costituzionale. Sebbene questi principi siano enunciati espressamente solo in relazione al lavoro subordinato (art. 2106 c.c.; art. 7 l. 300/1970, recante il cd. Statuto dei Lavoratori), la giurisprudenza costituzionale ne ha sancito l’applicabilità nello svolgimento di qualsiasi rapporto di lavoro, anche autonomo o professionale.
[27] Linee Guida di Confindustria, p. 71.
[28] Linee Guida di Confindustria, p. 71.
[29] Ed invero, come precisato dalle Linee Guida di Confindustria: “per quanto riguarda i lavoratori subordinati, è necessario coordinare le previsioni del Decreto 231 con il tessuto normativo di fonte legislativa, giurisprudenziale e contrattuale che caratterizza il potere disciplinare del datore di lavoro, a partire dall’art. 7 dello Statuto dei Lavoratori, da cui deriva il principio di tipicità sia delle violazioni che delle sanzioni”.
[30] P. 74 delle Linee Guida richiamate.
[31] Vedi pagg. 21-22 del Manuale della Qualità adottato da BIOSPA.
[32] Vedi pag. 53 delle Linee Guida di Confindustria per la costruzione dei Modelli di Organizzazione, Gestione e Controllo (versione giugno 2021).
PARTE SPECIALE N. 1
Reati contro la Pubblica Amministrazione, reati di corruzione tra privati ed istigazione alla corruzione tra privati ed associazione a delinquere (artt. 24, 24ter, 25 e 25ter, comma 1, lett. s bis)
SOMMARIO:
0.PREMESSA
1. REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N.1
2. LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE E LE REGOLE DI COMPORTAMENTO DA ADOTTARE
2.1 L’acquisto di beni e servizi e, in generale, la gestione dei fornitori.
2.2. I rapporti con la Pubblica Amministrazione e con le Autorità di Vigilanza in occasione di istanze, richieste di autorizzazione, effettuazione di comunicazioni e/o segnalazioni, ispezioni e procedimenti giudiziari.
2.3. Le attività di informazione scientifica, l’utilizzo di materiale informativo e promozionale e la distribuzione di prodotti gratuiti.
2.4. Le attività gestite dalla Direzione Marketing e l’organizzazione/sponsorizzazione di eventi.
2.5. La partecipazione a gare pubbliche o a procedure disciplinate dalle disposizioni del Codice sugli Appalti e le vendite a soggetti pubblici.
2.6. Le attività di vendita a soggetti privati (Strutture ospedaliere, farmacie e grossisti) ed i rapporti con clienti e/o partner commerciali.
2.7. La gestione economica, finanziaria e contabile della società.
2.8. La gestione del personale-
3. I FLUSSI INFORMATIVI E LE SEGNALAZIONI VERSO L’ORGANISMO DI VIGILANZA
0. PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti negli artt. 24, 24ter, 25 e 25ter, comma 1, lett. s bis) del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto sopra menzionati.
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 1
Iniziando dall’elencazione normativa, gli artt. 24 e 25 del D.Lgs. 231/01 richiamano le seguenti fattispecie di reato commesse in danno della Pubblica Amministrazione:
- Peculato e peculato mediante profitto dell’errore altrui (artt. 314 e 316 p.), che possono rappresentare il presupposto della responsabilità amministrativa dell’ente solamente laddove il fatto offenda gli interessi finanziari dell’Unione Europea;
- Malversazione a danno dello Stato (art. 316-bis p.);
- Indebita percezione di erogazioni a danno dello Stato (art. 316-ter c.p.);
- Truffa in danno dello Stato o di altro ente pubblico o delle Comunità Europee (art. 640, comma 2, n. 1, c.p.);
- Truffa aggravata per il conseguimento di erogazioni pubbliche (art. 640bis c.p.);
- Frode informatica in danno dello Stato o di altro ente pubblico (art. 640ter p.);
- Corruzione per l’esercizio della funzione (artt. 318 e 320 c.p.);
- Corruzione per un atto contrario ai doveri di ufficio (art. 319 c.p.);
- Corruzione in atti giudiziari (art. 319ter c.p.);
- Corruzione (propria, impropria o in atti giudiziari) posta in essere da una persona incaricata di pubblico servizio (art. 320 c.p.);
- Concussione (art. 317 c.p.);
- Induzione indebita a dare o promettere altra utilità (art. 319 quater c.p.);
- Pene previste per il corruttore in relazione alle fattispecie elencate supra (art. 321 c.p.);
- Peculato, concussione, induzione indebita a dare o promettere utilità, corruzione e istigazione alla corruzione di membri degli organi delle Comunità Europee e di funzionari delle Comunità Europee e di Stati Esteri; (art. 322bis p.);
- Abuso di ufficio (art. 323 c.p.);
- Traffico di influenze illecite (art. 346bisp.);
- Frode nelle pubbliche forniture (art. 356 c.p.);
- Frode in agricoltura a danno del Fondo europeo agricolo (art. 2 L. 898/1986).
Oltre a tali delitti, la presente parte speciale ha ad oggetto anche gli illeciti di cui all’art. 25, comma primo, lett. sbis) del D.Lgs. 231/01 che, benché formalmente ricompresi tra i reati societari, rappresentano il corrispondente privatistico delle fattispecie corruttive di cui agli artt. 318 ss. c.p. Si tratta in particolare:
- della corruzione tra privati (art. 2635 c.c.);
- dell’istigazione alla corruzione tra privati (art. 2635bis c.).
Da ultimo, la sostanziale coincidenza dei processi sensibili impone di trattare all’interno della presente parte speciale anche il delitto di associazione a delinquere di cui all’art. 416 (commi 1-5) che, come evidenziato nel corso delle attività di mappatura del rischio, rappresenta l’unico reato presupposto tra quelli contemplati dall’art. 25ter a presentare un astratto (per quanto risibile) rischio di commissione nell’ambito delle attività aziendali di SPA.
2. LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE E LE REGOLE DI COMPORTAMENTO DA ADOTTARE.
Quanto alle macroaree di attività aziendale nell’ambito delle quali potrebbero astrattamente essere commessi i reati presupposto elencati nel precedente paragrafo, le stesse sono:
2.1. I rapporti con la Pubblica Amministrazione e con le Autorità Regolatorie e/o di Vigilanza in occasione di istanze, richieste di autorizzazione, effettuazione di comunicazioni/segnalazioni, ispezioni e procedimenti giudiziari.
2.2. l’acquisto di beni e servizi e, in generale, la gestione dei fornitori;
2.3. Le attività di informazione scientifica, l’utilizzo di materiale informativo e promozionale e la distribuzione di prodotti gratuiti.
2.4. Le attività della Direzione marketing e l’organizzazione/sponsorizzazione di eventi.
2.5. La partecipazione a gare pubbliche o a procedure disciplinate dalle disposizioni del Codice sugli Appalti.
2.6. Le attività di vendita a soggetti privati (Strutture ospedaliere o farmacie) ed i rapporti con clienti e/o partner commerciali.
2.7. La gestione economica, finanziaria e contabile della società.
2.8. La gestione del personale.
Di seguito si provvederà ad approfondire ognuna delle macro-aree elencate, specificando, per ciascuna di esse, le SOP adottate da Società Prodotti Antibiotici S.p.A. nonché gli specifici standard di condotta da rispettare al fine di prevenire o minimizzare il rischio di commissione dei reati presupposto.
Al di là di quanto si dirà nei successivi paragrafi e sotto un profilo generale, occorre evidenziare che la gestione dei rischi connessi ai predetti processi aziendali è altresì affidata a standard di controllo e/o a principi di carattere trasversale che si fondano:
- sulla segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- sulla stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- sul rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- sulla documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- sullo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- sull’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- sulla formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[1]
Principi che, oltre a risultare dal Codice Etico e dal Manuale della Qualità adottato in relazione alla Divisione BIOSPA, sono altresì ricavabili dalle seguenti SOP, che riguardano la gestione complessiva dell’azienda e sono applicabili a tutte le Direzioni e/o Divisioni aziendali:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
2.1. I rapporti con la Pubblica Amministrazione e con le Autorità Regolatorie e/o di Vigilanza in occasione di istanze, richieste di autorizzazione, effettuazione di comunicazioni/segnalazioni, ispezioni e procedimenti giudiziari.
Secondo la dottrina e le principali Associazioni di Categoria, in relazione alle società farmaceutiche devono essere considerate “altamente critiche le aree che comportano una relazione con la Pubblica Amministrazione attraverso i soggetti qualificati come pubblici ufficiali o incaricati di pubblico servizio: Il Ministero della Salute, le aziende sanitarie ed ospedaliere, gli enti pubblici territoriali, i medici ospedalieri ed i farmacisti”.[2] Considerata la delicatezza dei prodotti commercializzati e l’esigenza di conciliare il business con la più stringente tutela della salute e della persona, le società farmaceutiche operano infatti in un contesto estremamente normato, interfacciandosi in modo continuo, tra gli altri, con AIFA (Agenzia Italiana del Farmaco) e con il Ministero della Salute, che esercitano una continua attività di verifica e controllo su molteplici aspetti del business aziendale (dai foglietti illustrativi, alla concessione dell’AIC..)
Prima di entrare nel merito dei (numerosi) processi sensibili che caratterizzano la presente macroarea, occorre tuttavia compiere una breve premessa teorica avente ad oggetto il significato da attribuire alle espressioni “Pubblica Amministrazione”, “Pubblico Ufficiale” ed “Incaricato di Pubblico Servizio”, che ricorrono pressochè costantemente nelle fattispecie di reato oggetto della presente parte speciale.
Quanto al concetto di “Pubblica Amministrazione”, agli effetti della legge penale viene comunemente considerato come “Ente della pubblica amministrazione” qualsiasi persona giuridica che abbia in cura interessi pubblici e che svolga attività legislativa, giurisdizionale o amministrativa in forza di norme di diritto pubblico e di atti autoritativi. Sebbene non esista nel codice penale una definizione di pubblica amministrazione, in base a quanto stabilito nella Relazione Ministeriale al codice stesso ed in relazione ai reati in esso previsti, sono ritenuti appartenere alla pubblica amministrazione quegli enti che svolgano “tutte le attività dello Stato e degli altri enti pubblici”.
Con l’espressione “pubblico ufficiale” deve intendersi chiunque, a prescindere da rapporti di dipendenza o di altro tipo con lo Stato o con un ente pubblico, esercita (o concorre ad esercitare) una pubblica funzione legislativa, giudiziaria o amministrativa, termine, questo, con cui si fa riferimento ogni attività disciplinata da norme di diritto pubblico e da atti autoritativi e caratterizzata dalla formazione e dalla manifestazione della volontà della pubblica amministrazione o dal suo svolgersi per mezzo di poteri autoritativi o certificativi.[3] In altre parole, è definita pubblica la funzione amministrativa disciplinata da “norme di diritto pubblico”, ossia da quelle norme volte al perseguimento di uno scopo pubblico ed alla tutela di un interesse pubblico e, come tali, contrapposte alle norme di diritto privato.
Quanto, infine, alla nozione di Incaricato di Pubblico Servizio, la stessa si applica a chiunque, a qualsiasi titolo, presti un pubblico servizio, ovvero un’attività che, anche in assenza di un contratto e/o incarico di natura pubblicistica e senza alcun potere tipico della PA, è disciplinata nelle stesse forme della pubblica funzione (con esclusione dello svolgimento di semplici mansioni di ordine e della prestazione di opera meramente materiale).
Tanto premesso a livello definitorio, in relazione a tale specifica macro area debbono ritenersi sensibili le seguenti attività:
- gestione dei rapporti con le Istituzioni o con Organismi di Vigilanza preposti a garantire lo svolgimento di attività regolate dalla legge o con i funzionari di Enti competenti in materia di adempimenti fiscali, societari (Agenzia delle Entrate, Camere di Commercio, Autorità Garante per la concorrenza e per il mercato);
- gestione di adempimenti, verifiche ed ispezioni in materia contributiva, giuslavoristica o in tema di salute e sicurezza sul lavoro e/o di ambiente;
- gestione dei rapporti di con soggetti appartenenti ad Enti pubblici di rilevanza nazionale, regionale e locale, deputati alla regolamentazione dei settori di interesse della società, tra cui il Ministero della Salute;
- attività connesse alla presentazione delle domande per l’ottenimento e/o modifica dell’AIC (autorizzazione all’immissione in commercio) o, comunque, alla commercializzazione di prodotti medicinali;
- attività di farmacovigilanza o comunque aventi ad oggetto la tracciabilità/ richiamo e distruzione dei farmaci o dei prodotti commercializzati;
- gestione dei rapporti con AIFA;
- gestione dei rapporti con Autorità Regolatorie Estere;
- gestione dei rapporti con l’Autorità Giudiziaria e dei contenziosi che vedono direttamente o indirettamente coinvolta SPA o un proprio dipendente;
Al fine di regolamentare tali processi aziendali, Società Prodotti Antibiotici S.p.A. ha implementato ed adottato diverse procedure specifiche finalizzate a disciplinare processi aziendali che prevedono – direttamente o indirettamente – contatti con le Autorità pubbliche deputate a regolare il funzionamento del settore farmaceutico. In particolare:
- IT.03.01 Tracciabilità del farmaco: tracciati SFR e MOV;
- CQ.02.01 Gestione stampati nel sistema Farmastampati;
- 0S.01.07 Materiale informativo e promozionale.
Fermo restando che tali documenti, per quanto incidentalmente, contribuiscono a fornire indicazioni sui comportamenti da adottare al fine di prevenire o minimizzare il rischio di commissione dei reati presupposto oggetto della presente parte speciale, Società Prodotti Antibiotici S.p.A. ha poi adottato una specifica SOP avente ad oggetto i rapporti con i Pubblici Ufficiali o gli incaricati di Pubblico Servizio.
Al di là delle standard operative procedures sopra menzionate, occorre altresì evidenziare che Società Prodotti Antibiotici S.p.A. ottiene annualmente la certificazione prevista dal Codice Deontologico di Farmindustria, che – essendo finalizzata ad attestare il pieno rispetto dagli obblighi di trasparenza e pubblicazione imposti dal D. Lgs. 219/06 e dalla medesima associazione di categoria – rappresenta un altro (imprescindibile) presidio funzionale a prevenire o minimizzare il pericolo di commissione dei reati presupposto di cui agli artt. 24 e 25 del D.Lgs. 231/01.
Al fine di evitare che i rapporti con le pubbliche amministrazioni o con le autorità regolatorie o di vigilanza offrano l’occasione di commettere i predetti illeciti e rimandando per il resto a quanto stabilito all’interno delle procedure sopra richiamate, è necessario:
- individuare in modo puntuale i soggetti (interni o esterni) che sono autorizzati a rappresentare l’azienda in tutti gli incontri con i pubblici ufficiali o con gli incaricati di pubblico servizio o firmare dichiarazioni e/o documentazioni ufficiali, conferendo tale potere attraverso apposita delega e/o procura;
- dare adeguata pubblicità alle deleghe o procure così conferite;
- fornire direttive chiare, precise e puntuali in ordine alla condotta da adottare nei contatti formali ed informali intrattenuti con enti pubblici, istituzioni, autorità di vigilanza;
- garantire, per quanto ragionevolmente possibile ed opportuno, la tracciabilità delle comunicazioni inviate o ricevute, favorendo l’implementazione di un sistema che consenta di ricostruire i flussi informativi intercorsi con pubblici ufficiali o incaricati di pubblico servizio;
- identificare i soggetti incaricati di presenziare a ispezioni e/o verifiche condotte da autorità pubbliche nonché a fornire informazioni o dati alle stesse;
- assicurare, per quanto possibile, la presenza di almeno due persone durante gli incontri, ispezioni o colloqui con pubblici ufficiali o con incaricati di pubblico servizio;
- evitare di porre in essere qualsivoglia comportamento che sia di ostacolo all’esercizio delle funzioni da parte dei pubblici ufficiali o degli incaricati di pubblico servizio, soprattutto in sede di ispezione e/o di sopralluoghi (espressa opposizione, rifiuti pretestuosi, comportamenti ostruzionistici o di mancata collaborazione, quali ritardi nelle comunicazioni o nella messa a disposizione di documenti);
- consegnare tempestivamente la documentazione eventualmente richiesta nel corso di verifiche/ispezioni o in sede di chiarimenti, assicurandosi che quanto fornito sia integrale e non presenti modifiche, omissioni, tagli o manipolazioni;
- evitare di fornire, redigere o consegnare ai pubblici ufficiali e/o agli incaricati di un pubblico servizio appartenenti alla Pubblica Amministrazione, agli Enti Pubblici e/o ai soggetti ad essi assimilati dello Stato Italiano, delle Comunità Europee e degli Stati esteri dichiarazioni, dati o documenti in genere aventi contenuti inesatti, errati, incompleti, lacunosi e/o falsi, al fine di ottenere certificazioni, permessi, autorizzazioni e/o licenze di qualsivoglia genere o specie, o conseguire erogazioni pubbliche, contributi o finanziamenti agevolati;
- monitorare periodicamente la persistenza delle condizioni/requisiti in virtù dei quali è stata concessa l’autorizzazione o licenza, comunicando tempestivamente alle Autorità o agli organi competenti ogni variazione o cambiamento;
- adottare sistemi che consentano di monitorare gli adempimenti connessi alle licenze o autorizzazioni ottenute (come, ad esempio, rinnovi) o alle scadenze fiscali o tributarie;
- favorire, anche attraverso consulenti terzi, la tempestiva trasmissione delle dichiarazioni fiscali, previdenziali e tributarie attraverso la posta elettronica certificata o gli altri canali a ciò dedicati;
- limitare l’accesso ai sistemi informatici o telematici della Pubblica Amministrazione o agli strumenti telematici (account pec) attraverso cui vengono trasmesse comunicazioni ufficiali;
- vietare la consegna di omaggi o benefit a pubblici ufficiali o a soggetti incaricati di pubblico servizio, dovendosi intendere come “omaggi o benefit” un bene materiale non di modico o minimale valore che comporti un “vantaggio materiale o morale, patrimoniale o non patrimoniale, che abbia valore per il pubblico agente”;
- specificare i limiti economici entro i quali l’omaggio è da considerarsi di valore modesto e/o minimale;
- assicurare che le comunicazioni/segnalazioni/atti inviati o depositati avanti all’Autorità Giudiziaria o ad organi che agiscono su delega di quest’ultima siano sottoscritti da soggetti muniti degli idonei poteri o appositamente incaricati, nonché trasmesse con modalità tali da garantirne la documentabilità;
- archiviare la copia dei documenti ufficiali diretti a Giudici, a membri del Collegio Arbitrale o a Periti d’ufficio chiamati a giudicare sul contenzioso di interesse della Società, nonché all’Autorità Giudiziaria (Pubblico Ministero, Polizia, Carabinieri, ecc.);
- comunicare periodicamente all’Amministratore Delegato (e all’OdV) l’elenco e lo stato dei contenziosi in corso che vedano coinvolta la società e/o i soggetti alle dipendenze della stessa;
- verificare che i professionisti eventualmente nominati per l’assistenza giudiziale o stragiudiziale della società siano dotati della necessaria professionalità e competenza, controllando la coerenza e congruità dei compensi;
- segnalare tempestivamente e senza ritardo, al proprio responsabile gerarchico o ad altre funzioni aziendali, eventuali comportamenti posti in essere da persone operanti nell’ambito della controparte pubblica, rivolti a ottenere favori, elargizioni illecite di denaro o altre utilità, anche nei confronti di terzi.
Con particolare riguardo agli standard di comportamento da adottare in relazione ai rapporti con il Ministero della Salute, con AIFA o, comunque, nell’ambito di tutte le attività direttamente o indirettamente ricomprese nella farmacovigilanza, nell’ottenimento/modifica dell’AIC o nella negoziazione dei prezzi, occorre:
- assicurare la segregazioni di funzioni tra chi predispone la documentazione relativa alle richieste di autorizzazione all’immissione in commercio, chi la approva e chi procede al pagamento degli importi;
- monitorare in modo stringente la completezza, esaustività ed accuratezza della documentazione da depositare presso AIFA/Ministero della Salute per l’ottenimento dell’AIC, favorendo un controllo preventivo a cura delle funzioni competenti (Direzione Scientifica, Regolatorio etc.);
- assicurare la completezza e correttezza dei dati inseriti nelle richieste e/o istanze finalizzate alla registrazione di determinati prodotti (ad es. reagenti in vitro) presso il Ministero della Salute;
- garantire la condivisione interna e la validazione formale delle strategie di prezzo;
- identificare i canali di comunicazione/trasmissione della documentazione ad AIFA o al Ministero della Salute;
- conferire un’apposita procura/delega al dipendente o al soggetto terzo responsabile della consegna della documentazione presso AIFA;
- assicurare la formalizzazione degli incontri con il Ministero della Salute/AIFA nonché la documentabilità dei flussi informativi intercorsi tra la società e la stessa;
- nominare formalmente il Responsabile della Farmacovigilanza della società, comunicando tempestivamente il suo nominativo ad AIFA e consentendo solo a quest’ultimo l’accesso alla Rete Nazionale di Farmacovigilanza mediante user ID e password;
- organizzare corsi di formazione aventi specificamente ad oggetto la materia della farmacovigilanza, fornendo tutte le indicazioni necessarie per la corretta gestione degli adempimenti in materia di segnalazione di eventi avversi;
- implementare canali che consentano a tutto il personale della società o a terzi che collaborano con la stessa di comunicare ogni segnalazione avversa di cui si venga a conoscenza.
2.2. L’acquisto di beni o servizi e la gestione dei rapporti con i fornitori.
Per quanto concerne l’acquisto dei beni o servizi e, in generale, l’attività di gestione dei fornitori, le attività sensibili sono legate:
- alla qualifica ed alla selezione dei fornitori;
- alla predisposizione ed approvazione delle richieste di acquisto;
- alla valutazione dei preventivi e/o offerte ricevute;
- alla gestione delle trattative;
- all’emissione dell’ordine di acquisto;
- all’esecuzione dei contratti.
Al fine di regolamentare tali processi aziendali e di predisporre un sistema di gestione caratterizzato da una stringente regolamentazione delle attività, Società Prodotti Antibiotici S.p.A., – oltre al Modello di Organizzazione e Gestione nonché al Codice Etico – ha adottato le seguenti procedure:
- QA.SQ.16.04 verifiche ispettive interne;
- QA.CQ.15.01, PGN74, relative alla selezione ed alla qualifica dei fornitori;
- PGN742 concernente gli ordini ai fornitori;
- LOG.02.01 gestione acquisti, scorte, carenze prodotti finiti.
Anche alla luce di quanto contenuto nei predetti documenti, occorre:
- per quanto possibile e ragionevole, svolgere un’attività di rigorosa selezione dei fornitori, verificando che gli stessi siano in possesso dei requisiti minimi richiesti per la tipologia di fornitura;
- prevedere periodiche attività ispettive e/o audit esterni per verificare in capo a determinati fornitori (materie prime, principi attivi, prodotti finiti etc.) la sussistenza dei requisiti di legge o delle certificazioni eventualmente richieste;
- correlare il tipo e l’estensione del controllo eseguito sui fornitori agli effetti che il prodotto acquistato può avere sul prodotto finale ed alla normativa applicabile;
- inserire i fornitori autorizzati in un apposito elenco, oggetto di periodico aggiornamento ad opera delle funzioni competenti;
- comunicare in modo tempestivo eventuali modifiche dell’elenco dei fornitori;
- definire i criteri di acquisto in modo chiaro e trasparente, anche attraverso la predisposizione di un piano di acquisti annuale;
- condurre un’adeguata attività selettiva fra diversi offerenti ed effettuare una scelta basata su un’obiettiva comparazione delle offerte e coerente con i criteri di acquisto preventivamente individuati;
- assicurare che la corrispondenza intercorsa da/verso i soggetti terzi con cui SPA intrattiene un rapporto commerciale sia sempre documentata o documentabile;
- utilizzare listini prezzi e/o di ulteriore documentazione contrattuale che predefinisca il valore della merce o del servizio acquistato;
- verificare, prima dell’emissione dell’ordine formale di acquisto, che le richieste di acquisto (RdA) o i c.d. “buoni fabbisogno” (BF), rispondano ad un’effettiva esigenza di SPA, siano caratterizzati da un prezzo congruo nonché coerenti con i budget stabiliti per centri di costo;
- assicurare che l’ordine di acquisto venga approvato da parte delle figure aziendali dotate dei necessari poteri (conformemente allo carica rivestita o ad eventuali deleghe e/o procure conferite) e che vengano svolti controlli sulla corretta valorizzazione, completezza ed accuratezza degli ordini di acquisto;
- prevedere che l’acquisto di beni e/o servizi in deroga a quanto stabilito con riguardo alle richieste di acquisto (o BF), alle verifiche da porre in essere ed all’emissione dei relativi ordini sia limitato ad ipotesi specificamente individuate all’interno della normativa aziendale (ad es. acquisti di beni o servizi nell’ambito di contratti di fornitura o, ancora, fatture allegate alle note spese degli Informatori Scientifici del Farmaco e degli Area Manager);
- verificare la corrispondenza tra il bene/servizio ricevuto e quanto previsto nell’ordine di acquisto prima di autorizzare il pagamento della prestazione;
- monitorare ed accertare la corretta esecuzione del contratto;
- segnalare alle funzioni aziendali competenti – ed eventualmente anche all’Organismo di Vigilanza attraverso i canali a ciò dedicati – le criticità riscontrate in ordine all’approvazione dell’ordine di acquisto e/o alla corretta esecuzione del contratto;
- definire le condizioni di urgenza in relazione a cui si può una fornitura può essere decisa in deroga ai normali passaggi decisionali o autorizzativi, prevedendo adeguati strumenti di verifica, monitoraggio o approvazione ex post;
- formalizzare il processo di acquisti e vendite infragruppo, assicurando l’applicazione di normali valori mercato ed il rispetto delle catene autorizzative e decisionali previste per gli acquisti da fornitori terzi;
- garantire la conservazione e la corretta archiviazione di tutta la documentazione (proposte, preventivi, contratti) legata all’acquisto di beni o servizi da parte di Società Prodotti Antibiotici S.p.A.;
- inserire nei contratti con i con i fornitori un’apposita clausola che regoli le conseguenze della commissione (o tentativo di commissione) da parte degli stessi dei reati di cui al D. Lgs. 231/2001 (es. clausole risolutive espresse o penali);
- inserire clausole che stabiliscano la risoluzione automatica del contratto qualora, in costanza di rapporto, vengano emessi provvedimenti giudiziali definitivi che accertino il coinvolgimento della società o dei propri soci, amministratori o dirigenti nelle condotte criminose di cui agli artt. 416, 416bis, 416ter, 630 c.p. o nel delitto di cui all’art. 74 D.P.R. 309/90.
2.3. Le attività di informazione scientifica, l’utilizzo di materiale informativo e promozionale e la distribuzione di prodotti gratuiti.
Un’altra macro-area particolarmente sensibile al rischio di commissione dei reati oggetto della presente parte speciale è quella legata alle attività di informazione scientifica svolte territorialmente dagli ISF e dagli Area Manager che, come detto, operano a livello territoriale e costituiscono circa due terzi del personale dipendete di Società Prodotti Antibiotici S.p.A. Nello svolgimento delle loro funzioni, i predetti soggetti, pur senza svolgere alcuna attività promozionale o commerciale in senso proprio, si rapportano infatti quotidianamente con operatori e strutture sanitarie pubbliche o private convenzionate, favorendo le conoscenze delle caratteristiche terapeutico/scientifiche dei farmaci e proponendo alla società l’organizzazione di corsi/eventi cui possono partecipare ed essere invitati soggetti qualificati o qualificabili come pubblici ufficiali o come incaricati di pubblico servizio. Tale circostanza – com’è ovvio – aumenta le potenziali occasioni di commissione dei reati indicati negli artt. 24 e 25 del D.Lgs. 231/01, tant’è che la dottrina, nell’identificare le aree maggiormente sensibili per quanto concerne le attività farmaceutiche, ha affermato che “l’attività di informazione scientifica rivolta al medico ed al farmacista costituisce nelle aziende farmaceutiche, una delle maggiori criticità da monitorare per prevenire la commissione dei reati di corruzione e truffa ai danni dello stato ai sensi del D.Lgs. 231/01”.
Al fine di recepire i (numerosi) principi normativi e deontologici concernenti la figura dell’informatore scientifico del farmaco, Società Prodotti Antibiotici S.p.A. – oltre ad approvare SOP di carattere trasversale applicabili a tutti i processi aziendali – ha adottato le seguenti standard operative procedures:
- DC/IS/01.04 “informatori scientifici”;
- SSC/IS/002.01 “materiale ad uso interno per addestramento ISF”;
- DV.01.07 “campioni gratuiti”;
- SSC.IS.01.07 “materiale informativo e promozionale”;
- SSC.IS.03.06 “materiale informativo di consultazione scientifica odi lavoro e materiale promozionale non specificamente attinente il medicinale”;
- 01.01. “gestione di richieste di informazione scientifica”;
- MKT.IS.05.01 “iniziative di relazione professionale”;
Anche alla luce di quanto previsto da tali documenti, è quindi necessario attenersi alle seguenti regole di condotta:
- in fase di assunzione e selezione degli ISF, verificare il possesso, da parte di questi ultimi, di tutti i requisiti previsti dalla normativa di riferimento;
- nominare, ai sensi del un Responsabile del Servizio Scientifico e comunicarne il nominativo ad AIFA;
- garantire, anche per il tramite del Responsabile del Servizio Scientifico, un’adeguata formazione agli ISF ed ai relativi Area Manager, avente ad oggetto da un lato le caratteristiche medico/terapeutiche dei farmaci commercializzati e, dall’altro i principi fondamentali posti alla base del Codice Etico, del Codice Deontologico di Farmindustria e del presente Modello di Organizzazione e Gestione;
- vietare agli Informatori Scientifici del Farmaco di esercitare professioni sanitarie/parasanitarie o aventi attinenza con l’utilizzazione del farmaco così come ulteriori attività di lavoro subordinato;
- provvedere ad una dettagliata e puntuale reportistica avente ad oggetto le visite e/o gli incontri effettuati dagli Informatori Scientifici del Farmaco per ciascun medico o operatore sanitario;
- rispettare scrupolosamente gli obblighi di comunicazione previsti nei confronti di AIFA circa il numero di sanitari visitati dagli ISF negli anni precedenti, adottando un atteggiamento trasparente e non omettendo alcuna informazione;
- formalizzare il processo finalizzato all’approvazione del materiale informativo, prevedendo il coinvolgimento del Responsabile del Servizio Scientifico, dell’ufficio Regolatorio e la tempestiva trasmissione ad AIFA;
- verificare che gli Informatori Scientifici del Farmaco utilizzino solamente materiale informativo debitamente approvato da AIFA;
- consegnare agli operatori sanitari materiale promozionale di valore trascurabile, come da normative vigenti che sia stato preventivamente acquistato dall’azienda a livello centrale;
- assicurare la tracciabilità e la registrazione dei campioni gratuiti ricevuti, consegnandoli agli operatori sanitari nelle quantità e nei limiti stabiliti dalle procedure interne e dal D.Lgs. 219/06;
- prevedere la trasmissione periodica, da parte degli ISF, dell’inventario dei campioni gratuiti dagli stessi detenuti, così da assicurare una corretta gestione degli stessi;
- evitare che le iniziative di relazione professionale siano autonomamente organizzate o decise dagli ISF o dai propri Area Manager, assicurando un costante flusso informativo con la funzione aziendali che è responsabile delle “iniziative di relazione professionale”, deputata a valutarne la conformità rispetto a quanto previsto dalla normativa e dalle linee guida;
- garantire la presenza, nell’ambito delle iniziative di relazione professionale, di almeno un soggetto inquadrabile nel personale direttivo aziendale, escludendo i soggetti che abbiano un ruolo operativo territoriale;
- assicurare il rispetto dei principi di proporzionalità, continenza e non ripetitività delle iniziative di relazione professionale, prevedendo un numero massimo di partecipanti nonché dei tetti massimi di spesa per ciascuno di essi;
- implementare presidi e/o controlli finalizzati a verificare il rispetto dei principi di comportamento (quali periodi di affiancamento);
- rispettare scrupolosamente la normativa di settore e i principi contenuti nel Codice Deontologico di Farmindustria per quanto concerne la gestione di gadget e/o campioni gratuiti.
2.4. Le attività di marketing e, in particolare, l’organizzazione/sponsorizzazione di eventi e la gestione degli inviti.
Oltre all’attività di informazione scientifica (scevra, come detto, di risvolti commerciali) anche i processi aziendali gestiti dalla Direzione Marketing presentano non trascurabili profili di delicatezza e comportano un concreto rischio di commissione delle fattispecie oggetto della presente parte speciale. In particolare, le attività “sensibili” che caratterizzano tale macroarea sono le seguenti:
- la preventiva individuazione di un apposito budget da dedicare agli eventi o da destinare a borse di studio, consulenze scientifiche o studi clinici ed osservazionali;
- la pianificazione degli eventi;
- la gestione organizzativa dell’evento e degli inviti;
- la rendicontazione e trasparenza dei trasferimenti di valore;
- la selezione/gestione dei provider e delle segreterie organizzative;
- la scelta circa i relatori/moderatori;
- la gestione dei rimborsi spese dei partecipanti;
- l’attribuzione di borse di studio;
- la selezione di consulenti e la verifica circa i requisiti degli stessi;
- il controllo circa l’effettiva prestazione delle attività oggetto di consulenza o della borsa di studio;
- la gestione dei rapporti con Società Scientifiche, Associazioni Mediche ed associazioni dei pazienti.
Al fine di descrivere le procedure adottate dalla società e le regole di condotta da porre in essere al fine di prevenire o minimizzare il rischio di commissione dei reati presupposto contemplati negli artt. 24, 25 e 25ter (comma 1, lett. s) e s) bis), verranno partitamente analizzate:
(a) l’organizzazione e la sponsorizzazione di eventi;
(b) le consulenze medico-scientifiche e le borse di studio;
(c) i rapporti con le Società Scientifiche/Associazioni Mediche nonché con le Associazioni di pazienti.
(a) Iniziando dall’organizzazione/sponsorizzazione di eventi, occorre preliminarmente precisare che con l’espressione “eventi” si intende un’ampia categoria concettuale che ricomprende al suo interno una pluralità di definizioni utilizzate all’interno della normativa di settore nonché del Codice Deontologico di Farmindustria, ovvero: gli investigators meetings, gli eventi congressuali, i convegni, i simposi satellite, le visite ai laboratori, l’organizzazione di corsi di formazione e tutti gli ulteriori eventi organizzati al fine di presentare i propri prodotti o servizi.
Al di là di quanto detto in relazione alle standard operative procedures “trasversali” (per il cui elenco fa sempre riferimento a quanto evidenziato nel paragrafo 2.1. della presente parte speciale) tutti i predetti processi aziendali risultano puntualmente disciplinati dalle seguenti SOP:
- AMM.IS.02.02 Trasparenza dei trasferimenti di valore;
- DG/IS/02.04. “convegni, congressi, corsi di aggiornamento e visite ai laboratori aziendali”;
- DS.IS.01.02 “organizzazione Investigators meeting”.
In questo senso, rimandando per il resto a tali documenti nonché al Codice Etico adottato da Società Prodotti Antibiotici S.p.A., ai destinatari del presente Modello di Organizzazione e Gestione è fatto obbligo di:
- predeterminare un budget annuale dedicato agli eventi e provvedere al costante monitoraggio dello stesso;
- garantire una separazione di funzioni tra la funzione proponente e quella preposta ad autorizzare l’organizzazione e/o sponsorizzazione dell’evento medesimo, formalizzando un iter decisionale ed organizzativo fondato sulla chiara identificazione dei soggetti coinvolti;
- verificare, anche attraverso l’ausilio della Direzione Scientifica ed il Responsabile del Servizio Scientifico, il contenuto delle iniziative proposte, accertando se lo stesso sia scientificamente qualificante e sia rispondente alla tipologia dei prodotti commercializzati dalla società;
- disciplinare il processo di selezione delle agenzie eventualmente scelte per l’organizzazione degli eventi;
- controllare la coerenza tra le tematiche oggetto dell’iniziativa e la competenza/specializzazione dei medici che, su invito della società, partecipano alla stessa;
- laddove il personale sanitario da invitare appartenga ad Enti pubblici o a strutture private convenzionate, trasmettere un invito non nominativo, lasciando alla struttura la scelta circa il soggetto da indicare;
- monitorare i soggetti invitati agli eventi sponsorizzati/organizzati dalla società al fine di evitare che la medesima persona venga invitata oltre i limiti stabiliti dalla normativa e dai principi del codice deontologico, predisponendo a tal fine un apposito registro dove vengono inseriti tutti i dati concernenti gli inviti ed i nominativi dei soggetti invitati;
- rispettare le regole e i limiti stabiliti a livello normativo e deontologico con riguardo all’ospitalità, alla durata massima, alla sedi ed alle categorie di spese ammissibili;
- trasmettere, ad AIFA, laddove necessario e previsto, la domanda di autorizzazione preventiva dell’iniziativa sponsorizzata/organizzata dalla società, inserendo sugli appositi portali le spese consuntivate connesse all’evento;
- distribuire unicamente gadget di valore trascurabile ed attinenti le professioni di medico o farmacista;
- documentare e debitamente archiviare tutti i costi sostenuti in relazione all’evento, verificandone la proporzionalità e coerenza prima di autorizzarne il pagamento o rimborso;
- pubblicare, in forma individuale o aggregata, tutti i trasferimenti di valore concernenti l’iscrizione, le spese di viaggio e l’ospitalità (ad esclusione delle spese minimali) degli operatori sanitari invitati;
- pubblicare e/o rendere accessibili/verificabili gli ulteriori trasferimenti di valore legati agli eventi organizzati o sponsorizzati;
- definire in modo chiaro, puntuale e non fraintendibile l’oggetto degli investigators meeting così da evitare che tali riunioni vengano strumentalizzate per fini promozionali;
- coinvolgere un numero di partecipanti proporzionato rispetto a quello dei centri di sperimentazione coinvolti;
- assicurare che siano preventivamente definiti i limiti concernenti i pasti, l’ospitalità, la durata ed il luogo degli investigator meetings;
- attivare gli investigator meetings solo al fine di produrre protocolli di studio da depositare presso il Comitato Etico Locale;
- garantire la piena tracciabilità e documentabilità di tutta la documentazione concernente gli eventi organizzati o sponsorizzati (dai moduli di partecipazione, alle autorizzazioni interne fino ad arrivare alla domanda presentata presso AIFA).
(b) Quanto alle ulteriori attività gestite dalla Direzione Marketing e da considerarsi “sensibili” ai sensi della presente parte speciale, vanno poi menzionate le consulenze medico-scientifiche e le borse di studio. In ordine a tali attività – regolamentate dalla SOP MKT/RIS/01.05 (cui si rimanda integralmente) – è necessario:
- predeterminare un budget avente ad oggetto le borse di studio;
- formalizzare il processo autorizzativo per il conferimento di incarichi consulenziale;
- verificare che il consulente possieda la qualifica e l’esperienza necessaria per fornire il servizio richiesto;
- concordare un compenso che rispetti criteri di economicità e sia congruo ed adeguato rispetto al servizio reso o da rendere;
- assicurare la piena documentabilità dell’attività svolta dal consulente;
- attribuire borse di studio che abbiano ad oggetto un progetto di rilevante interesse scientifico con specifici e misurabili obiettivi;
- verificare che le borse di studio abbiano carattere non abituale e non siano ripetute con la stessa unità operativa o dipartimento prima che sia trascorso un determinato periodo temporale;
- garantire la conservazione e l’archiviazione di tutta la documentazione avente ad oggetto le borse di studio o le consulenze medico-scientifiche;
- inserire nei contratti con i consulenti un’apposita clausola che regoli le conseguenze della commissione (o tentativo di commissione) da parte degli stessi dei reati di cui al D. Lgs. 231/2001 (es. clausole risolutive espresse o penali);
- dare adeguata pubblicazione ai trasferimenti di valore legati al riconoscimento di borse di studio o al compenso per consulenze.
(c) tra i processi aziendali gestiti dalla Direzione Marketing rilevano infine i rapporti con le Società Scientifiche/Associazioni Mediche nonché con le Associazioni di pazienti, nell’ambito dei quali possono essere promossi studi clinici o osservazionali. Fermo restando che in ordine a tali aspetti, SPA ha adottato due procedure specifiche alle quali si rimanda integralmente (ovvero la MKT/IS/02.04 nonché la MKT/IS/0.4.02), occorre rispettare le seguenti regole di condotta:
- predeterminare un budget avente ad oggetto i trasferimenti di valore realizzati – a vario titolo – a favore delle Associazioni mediche o dei pazienti e delle società scientifiche;
- gli enti selezionati per le collaborazioni/sponsorizzazioni/contributi devono essere di provata affidabilità e noti a livello nazionale dovendosi, in caso contrario, raccogliere idonea documentazione attestante la struttura, la missione e le caratteristiche dell’associazione e/o società (statuto, atto costitutivo etc.);
- le sponsorizzazioni, i contributi e gli ulteriori trasferimenti di valore a favore di associazioni mediche e/o di pazienti o delle società scientifiche, devono essere privi di finalità promozionali o commerciali;
- deve essere garantita la trasparenza di tutti i trasferimenti di valore effettuati nei confronti di associazioni di pazienti, provvedendo ogni anno alla pubblicazione di una lista delle associazioni supportate nell’anno precedente e specificando il valore economico dei contributi nonché le finalità dello stesso;
- le attività di cui alle diverse fasi del processo devono essere svolte da soggetti differenti chiaramente identificabili e devono essere supportate da un meccanismo di maker e checker, con una diversificazione tra il soggetto proponente ed il soggetto chiamato a compiere la verifica documentale e, eventualmente, ad autorizzare la sponsorizzazione, il contributo o la collaborazione;
- è necessario ricevere un riscontro circa le attività intraprese dall’associazione e/o ente dopo l’erogazione del contributo;
- gli studi clinici devono essere avviati solo a seguito della ricezione del parere positivo del Comitato Etico interessato ed eventualmente dell’Autorità competente;
- la documentazione prodotta alle autorità regolatorie per l’autorizzazione alla conduzione dello studio clinico deve essere accurata e completa;
- i centri di ricerca eventualmente coinvolti devono essere selezionati così da assicurare la fattibilità degli studi nella specifica area clinico/terapeutica;
- prima di disporre il pagamento, è necessario provvedere a verificare la completezza e correttezza delle fatture ricevute dagli enti incaricati della conduzione degli studi clinici;
- l’esito degli studi clinici deve essere formalizzato a livello interno e notificato all’AIFA.
2.5. La partecipazione a gare pubbliche o a procedure disciplinate dalle disposizioni del codice sugli appalti e le vendite effettuate a soggetti pubblici.
Secondo quanto riferito nel corso delle interviste realizzate per l’attività di mappatura del rischio, è emerso che Società Prodotti Antibiotici S.p.A. – soprattutto per il tramite della divisione aziendale BIOSPA – partecipa a gare o altre procedure pubbliche indette ai sensi del D.Lgs. 50/16 (anche denominato “Codice Appalti”), essendo dotata di un ufficio preposto a gestire tutte le attività direttamente o indirettamente connesse alle stesse. Allo stesso modo, quando consentito dalla normativa, la società partecipa a vendite dirette su richiesta di soggetti pubblici. Tale ambito – com’è ovvio – si caratterizza per una molteplicità di processi aziendali che, comportando il contatto con pubblici ufficiali e la produzione di documentazione atta ad influenzarne e/o orientarne le scelte, presentano molteplici rischi di commissione dei reati presupposto disciplinati dagli artt. 24 e 25 del D.Lgs. 231/01. In particolare, volendo riepilogare le attività “sensibili” aventi ad oggetto tale macroarea, si tratta:
- della definizione delle politiche commerciali e dell’individuazione delle gare e/o procedure cui partecipare;
- della gestione dei contratti con il RUP;
- della predisposizione della documentazione di gara;
- della partecipazione alla gara;
- dell’aggiudicazione e dell’eventuale stipula dei contratti nonché dell’esecuzione degli stessi.
In relazione a tali attività, oggetto della Procedura Generale PGN722 adottata in relazione alla Divisione BIOSPA, i destinatari del presente Modello di Organizzazione e Gestione dovranno:
- selezionare gli agenti di zona deputati alla segnalazione di gare e/o procedure pubbliche o al controllo del capitolato tra soggetti dotati della necessaria professionalità e competenza;
- coinvolgere diverse funzioni aziendali (ciascuna per la propria area di competenza) nella fase di studio del bando di gara e capitolato nonché nella preparazione della documentazione finalizzata ad attestare la sussistenza dei requisiti generali e speciali in capo all’azienda o ai soggetti che l’amministrano o ne detengono il capitale sociale;
- verificare la completezza ed accuratezza della documentazione di gara nonché la coerenza della documentazione di gara rispetto al bando ed al capitolato, controllando altresì la correttezza dei prezzi offerti e/o applicati;
- assicurare che la documentazione prodotta in sede di gara o di vendita diretta sia sottoscritta nel rispetto dei poteri conferiti dal Consiglio di Amministrazione o delle procure eventualmente concesse;
- identificare in modo preventivo le eventuali migliorie di prezzo o le forme di scontistica che possono essere concesse ed i soggetti che sono coinvolti nella catena decisionale o autorizzativa;
- verificare che eventuali forme di scontistica legate al raggiungimento di determinati obiettivi economici e/o ulteriori target siano erogate o concesse al verificarsi delle condizioni preventivamente stabilite;
- coinvolgere una pluralità di soggetti che si rapportino con il Responsabile Unico del Procedimento (di seguito anche semplicemente “RUP”) nominato dalla Stazione Appaltante;
- fornire evidenza scritta in relazione a tutte le eventuali modifiche apportate a seguito di trattative e/o contatti intercorsi con il RUP o con un ulteriori soggetti appartenenti alla stazione appaltante/ente pubblico;
- evitare di offrire, anche per il tramite degli agenti di zona, gadget, omaggi, benefit o utilità (anche se di modico o minimale valore) al RUP o ad altri soggetti appartenenti alla Stazione Appaltante e di persuadere/indurre i pubblici ufficiali ad orientare la propria scelta;
- garantire la piena tracciabilità e documentabilità delle comunicazioni trasmesse e/o ricevute dalla Stazione Appaltante e provvedere debitamente all’archiviazione delle stesse;
- individuare uno o più soggetti responsabili della regolare esecuzione dei contratti di fornitura stipulati in virtù dell’aggiudicazione di una gara o di un’altra procedura indetta ai sensi e per gli effetti del Codice degli Appalti, attribuendo agli stessi il compito di monitorare il rispetto delle tempistiche di allestimento/consegna dei prodotti forniti;
- favorire l’utilizzo delle piattaforme digitali implementate dagli enti pubblici (appartenenti o non appartenenti al SSN) per agevolare la trasmissione di ordini di beni e/o servizi , di conferme d’ordine e di documenti di vendita.
2.6. Le attività di vendita a soggetti privati (strutture ospedaliere, grossisti o farmacie) ed i rapporti con clienti e/o partner commerciali.
L’inserimento nella presente parte speciale delle fattispecie di corruzione tra privati ed istigazione alla corruzione tra privati, determina la necessità di soffermarsi sulle attività concernenti le vendite effettuate da Società Prodotti Antibiotici S.p.A. a favore di ospedali privati, di farmacie/parafarmacie e/o di grossisti, in quanto la gestione dei rapporti commerciali con tali soggetti determina il pericolo che i dipendenti di SPA pongano in essere condotte inquadrabili nel paradigma normativo di cui agli artt. 2635 e 2635bis c.c. In particolare, l’offerta/promessa/dazione di denaro o altra utilità non dovuti per compiere o per omettere un atto in violazione degli obblighi inerenti al loro ufficio o degli obblighi di fedeltà o un’istigazione in tal senso, potrebbe aversi:
- nella definizione delle politiche commerciali;
- nella gestione delle trattative e nell’eventuale concessione di eterogenee forme di scontistica;
- nella stipula ed esecuzione dei contratti.
Pur non essendo oggetto di una specifica standard operative procedure, la regolamentazione di tali attività è affidata ad una pluralità di SOP connotate da una valenza trasversale e da principi applicabili anche alle predette aree di rischio. In particolare, oltre alle standard operative procedures trasversali riepilogate nel paragrafo 2.1., si fa riferimento alle SOP:
- AMM-IS-01-04 “comodati d’uso, donazioni e atti di liberalità”;
- AMM.IS.02.02. “trasparenza dei trasferimenti di valore”;
- MKT.IS.05.01 “iniziative di relazioni professionali”;
- MKT/RIS/01.05 “consulenze scientifiche e borse di studio”.
Conformemente a quanto previsto in tali policies, è fatto obbligo:
- di improntare i rapporti con i clienti e con i partner commerciali alla massima correttezza e trasparenza, garantendo la piena tracciabilità e documentabilità delle comunicazioni o dei rapporti intercorsi con gli stessi;
- di rispettare la catena decisionale ed autorizzativa legata alla predisposizione dell’offerta e/o proposta commerciale, all’invio della stessa al cliente ed alla concessione di eventuali forme di scontistica;
- di verificare la congruità del prezzo offerto rispetto ai riferimenti di mercato, tenuto conto dell’oggetto del contratto e delle quantità;
- di non concedere sconti o condizioni contrattuali agevolate che non rientrino nei poteri/facoltà conferite in virtù dello specifico ruolo rivestito a livello aziendale o attraverso apposita procura;
- di garantire la formalizzazione e l’invio dell’offerta contenente i prezzi e gli sconti eventualmente applicati, provvedendo ad archiviare tutta la documentazione prodotta nel corso dell’attività di gestione commerciale;
- favorire l’utilizzo di piattaforme o portali digitali finalizzati a facilitare il processo di gestione degli ordini e/o la digitalizzazione dei documenti direttamente o indirettamente collegati al ciclo dell’ordine;
- di non promettere o consegnare denaro o di altri benefici (in qualsiasi forma o di qualsiasi entità) agli Amministratori, Direttori Generali, dirigenti preposti alla redazione dei documenti contabili societari, i sindaci, liquidatori o soggetti che svolgono incarichi direttivi all’interno di società clienti o partner;
- di adottare regole predefinite per il conferimento di incarichi, tra cui quelli a titolo di “intermediazione” – o consulenze a soggetti terzi, ispirandosi a criteri di legalità, trasparenza, condivisione funzionale, inerenza e giustificabilità.
- di organizzare eventuali iniziative di relazione professionali che siano sobrie e caratterizzate da ripetitività, rispondendo ad effettivi interessi o esigenze dell’azienda;
- di non ammettere donazioni/erogazioni liberali a favore di clienti e/o partner commerciali, garantendo la stringente applicazione della standard operative procedure adottata a livello interno;
- di realizzare trasferimenti di valore nel pieno rispetto di quanto stabilito dalla normativa e dai principi deontologici di Farmindustria;
- di assicurare la piena trasparenza a tutti i trasferimenti di valore, provvedendo alla pubblicazione, sul sito aziendale o attraverso altre modalità, di uno specifico report avente ad oggetto tutte le predette operazioni;
- di assicurare il monitoraggio della regolare esecuzione del contratto in termini di quantità, qualità e di tempistiche di allestimento e consegna ai clienti;
- di tenere un comportamento corretto, nel pieno rispetto delle norme di legge e delle procedure eventualmente stabilite, nei confronti dei soggetti incaricati delle certificazioni periodiche previste dai sistemi di qualità o di gestione della salute o sicurezza sul lavoro allorché tali soggetti siano organizzati in strutture societarie di diritto privato e non rivestano la qualifica di pubblico ufficiale o incaricato di pubblico servizio.
2.7. La gestione economica, finanziaria e contabile della società.
Con riguardo, invece, alle specifiche condotte da porre in essere in relazione alle aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, giova evidenziare che Società Prodotti Antibiotici S.p.A. ha adottato due specifiche Standard Operative Procedure aventi ad oggetto la gestione economica e contabile della società, ovvero la SOP AMM.04.01 (concernente la gestione fatturazione dei clienti) e la SOP AMM.03.01 (relativa alla gestione del ciclo passivo). Tali documenti, letti unitamente all’organigramma ed al sistema di procure e/o deleghe di funzioni implementato a livello aziendale, consentono di ricostruire compiutamente i presidi posti in essere a livello di gestione economico/finanziaria. Oltre a tali SOP – che costituiscono un allegato del presente Modello di Organizzazione e Gestione ed alla quale si rimanda integralmente – i processi “sensibili” ricompresi in questa macroarea sono indirettamente disciplinati anche da ulteriori procedure quali:
AFC_2013_ 1 “note di credito” (in attesa di revisione: abbiamo la SOP revisionata?);
AMM-IS-01-04 “comodati d’uso, donazioni e atti di liberalità”;
AMM.IS.02.02. “trasparenza dei trasferimenti di valore”;
MKT/RIS/01.05 “consulenze scientifiche e borse di studio”.
Fermo restando che le regole di comportamento da adottare in questo ambito saranno debitamente e compiutamente approfondite all’interno di altre parti speciali – come quella concernente i reati tributari o quella avente ad oggetto le fattispecie di ricettazione, riciclaggio, impiego di denaro o altra utilità, autoriciclaggio– in questa sede è sufficiente osservare che ai destinatari del presente Modello di Organizzazione e Gestionali è fatto obbligo di rispettare le seguenti regole di condotta:
- le risorse destinate a determinate attività (promozione/sponsorizzazione di eventi, donazioni/erogazioni o adempimenti in materia di salute e sicurezza sul lavoro) sono individuate ex ante attraverso una specifica delibera del CdA o attraverso una decisione dell’Amministratore Delegato che istituisca un apposito budget, prevedendo adeguate autorizzazioni in caso di superamento del budget previamente stabilito;
- il CdA stabilisce un sistema di procure per i pagamenti fondato sulla definizione di soglie quantitative di spesa coerenti con le competenze gestionali e con le responsabilità organizzative, provvedendone a darne adeguata pubblicità, in primis attraverso il Registro delle Imprese;
- occorre garantire, anche per il tramite di flussi informativi, il costante allineamento fra poteri, procure e deleghe operative e profili autorizzativi e debbono essere rispettati i livelli autorizzativi sia per la richiesta di pagamento che per la disposizione, che sono articolati in funzione dell’importo;
- i soggetti che operano nelle fasi di richiesta della disposizione di pagamento, effettuazione del pagamento, controllo/riconciliazioni a consuntivo debbono essere distinti;
- tutte le operazioni che comportano l’utilizzazione o l’impiego di risorse economiche o finanziarie devono avere una causale espressa ed essere giustificate dalla produzione di idonea documentazione stabilendo (a titolo esemplificativo, che agli ordini di bonifico devono essere allegate le fatture di riferimento ed eventuale ulteriore documentazione giustificativa);
- sono adottati gestionali che assicurano l’automatica creazione di fatture attive e passive a fronte dell’inserimento della documentazione concernente l’operazione effettuata o la prestazione ricevuta nonché di scaricare o ricevere le fatture passive emesse dai fornitori e che sono idonei ad interfacciarsi e/o rapportarsi con i portali predisposti dall’Agenzia delle Entrate;
- prima di procedere all’invio al Sistema di Interscambio delle fatture attive in formato XML, devono essere effettuati controlli sui documenti fiscali provvisori creati a partire dalla documentazione inserita a gestionale;
- il sistema di trasmissione ed interscambio, deve essere costantemente monitorato accertando la sussistenza di eventuali rifiuti circa la documentazione caricata ed adottando tempestivamente le opportune azioni correttive;
- è vietato effettuare pagamenti a soggetti diversi dalla controparte contrattuale;
- al di là di casi eccezionali, tutti i pagamenti e/o trasferimenti di valore debbono essere effettuati attraverso strumenti di pagamento che assicurino la piena tracciabilità e documentabilità dell’operazione;
- nessun pagamento può essere effettuato dalla Società in contanti se non conformità ai limite di legge e nel pieno rispetto delle procedure adottate a livello interno;
- le casse in contanti eventualmente istituite presso le Direzioni/Divisioni aziendali devono essere contraddistinte da un limite massimo e possono essere utilizzate per realizzare pagamenti di importo minimo, dovendosi in ogni caso garantire la piena tracciabilità e rendicontazione delle operazioni compiute;
- il rimborso delle spese sostenute dai dipendenti può avvenire solo a fronte della produzione di idonea documentazione comprovante l’operazione di cui si chiede il rimborso;
- la documentazione concernente i rimborsi e le note spese deve essere valutata dalle competenti funzioni aziendali al fine di verificare la congruità e l’idoneità degli importi di cui si chiede la corresponsione, oltre che il rispetto della normativa applicabile e dei principi deontologici stabiliti da Farmindustria;
- gli importi eventualmente riconosciuti a titolo di contributo, finanziamento, mutuo agevolato o comunque erogati a favore di Società Prodotti Antibiotici S.p.A. al fine di realizzare attività di pubblico interesse debbono essere spesi coerentemente alle finalità per cui sono stati attribuiti:
- un incarico consulenziale o di una borsa di studio possono essere concessi solo a fronte di e controlli funzionali a verificare: (a) la competenza e professionalità del soggetto che riceve l’incarico o la borsa di studio; (b) che l’importo risponda a criteri di economicità e sia coerente con i valori di mercato; (c) che l’attività oggetto di incarico o della borsa di studio sia effettivamente posta in essere e possa essere documentata;
- i trasferimenti di valore nei confronti di operatori sanitari pubblici o appartenenti a strutture private convenzionate devono essere realizzati rispettando le procedure interne e i principi del Codice Deontologico di Farmindustria, garantendo la non ripetitività degli inviti e la piena trasparenza degli stessi;
- le donazioni devono essere ammesse ed autorizzate solamente a fronte: (a) di una preliminare verifica circa l’ammissibilità della stessa e l’affidabilità dell’ente/struttura richiedente; (b) lo stringente rispetto della catena decisionale ed autorizzativa indicata nella SOP adottata a livello interno e la piena tracciabilità delle decisioni; (c) l’utilizzo di modulistica standard da cui si evinca in modo chiaro l’importo oggetto di donazione e/o erogazione (d) la conservazione e l’archiviazione della documentazione concernente le erogazioni ed i pagamenti effettuati.
2.8. La gestione del personale.
Un’ultima macro-area in cui sussistono potenziali rischi di commissione dei reati presupposto oggetto della presente parte speciale è rappresentata dalle attività a vario titolo connesse alla gestione del personale presente in azienda, che deve considerarsi “sensibile” ai fini del presente documento con riguardo:
- all’assunzione di risorse;
- alla verifica in ordine al possesso di determinati requisiti;
- alla gestione del sistema premiante;
- alla gestione delle carte di credito o degli altri strumenti di p
In relazione a tali attività vanno osservate le seguenti regole di condotta:
- l’assunzione di una risorsa deve sempre avvenire a fronte dell’esistenza di un budget predeterminato deliberato dall’Amministratore Delegato o dal C.d.A.
- il candidato deve essere valutato sulla base di criteri oggettivi e trasparenti (es. laurea/diploma, conoscenze lingue straniere, precedenti esperienze professionali);
- anche in relazione al ruolo ed alle mansioni che il candidato dovrà svolgere, al candidato dovrà essere richiesta la consegna del certificato dei carichi pendenti e del casellario giudiziale,;
- al neoassunto deve essere consegnata copia – integrale o riassuntiva – del Codice Etico adottato da Società Prodotti Antibiotici p.A. e lo stesso dovrà sottoscrivere un modulo a titolo di presa visione del predetto documento;
- è fatto divieto di assumere ex pubblici ufficiali o incaricati di pubblico servizio nei due anni successivi al compimento di un atto discrezionale da cui sia derivato un vantaggio per la società o che comunque, nel medesimo arco temporale, siano stati coinvolti in procedure o procedimenti all’esito dei quali siano state assunte deliberazioni favorevoli per Società Prodotti Antibiotici S.p.A.
- con specifico riguardo ai componenti del Consiglio di Amministrazione, all’Amministratore Delegato, ai soggetti cui è stata conferita una procura specifica avente ad oggetto l’esercizio di determinati poteri, ai componenti del Collegio Sindacale e dell’Organismo di Vigilanza, occorre procedere ad una verifica periodica di eventuali procedimenti penali e/o provvedimenti giudiziali passati in giudicato;
- gli eventuali piani di incentivazione e/o di benefit devono essere predefiniti;
- i criteri di assegnazione dei premi e benefit devono essere tracciabili e ricostruibili ex post;
- devono essere identificate le spese di cui è ammesso il rimborso, unitamente ai relativi limiti di importo (diversificati a seconda dell’inquadramento lavorativo o professionale);
- è sempre richiesta la produzione di giustificativi o di altri documenti che attestino le spese sostenute, che dovranno essere adeguatamente valutati dai competenti Responsabili di Direzione e dalla Direzione Amministrazione e Finanza ;
- le carte di credito e/o prepagate aziendali – sia ordinarie che aventi ad oggetto l’erogazione di carburante (c.d. “fuel card”) – possono essere assegnate solo ai soggetti che rivestono determinati ruoli e funzioni;
- vanno definiti i limiti e le tipologie di spesa ammesse attraverso l’utilizzo della carta di credito o delle fuel card.
3. I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
[2] Si rimanda all’articolo intitolato “Il D.LGS. 231/2001 e le case farmaceutiche. Alcuni spunti sull’attività di sponsorizzazione e sulla gestione del rapporto con gli informatori scientifici del Farmaco”, M. CARDIA, pubblicato su Rivista231.
[3] La giurisprudenza ha ad esempio avuto modo di attribuire la qualità di pubblico ufficiale ai seguenti soggetti:
- il titolare di una delegazione dell’ACI incaricata della riscossione delle tasse automobilistiche (Cass. Sez. VI, sent. n. 31425 del 2007);
- il capotecnico della Motorizzazione civile addetto all’espletamento delle pratiche di revisione auto veicolare (Cass., Sez. VI, sent. n. 35839/2008);
- i militari in servizio presso le caserme (Cass.,Sez. I, sent. n. 5986/1986), nonché gli appartenenti all’Arma dei Carabinieri, che sono da considerarsi in Servizio permanente e non cessano dalle loro qualità di pubblici ufficiali, anche quando non sono comandati in servizio (Cass., Sez. VI, sent. n. 9691/2003);
- il privato esercente un libero deposito di olii minerali, nell’atto in cui per delega della Pubblica Amministrazione, procede alla formazione del certificato di provenienza Mod. H ter 16 (Cass., Sez. III, sent. n. 3161/1984);
- il direttore di un consorzio di bonifica, poiché l’attività del consorzio è destinata al perseguimento di scopi di pubblico interesse (Cass., Sez. VI, sent. n. 8494/1998);
PARTE SPECIALE N. 2
Delitti informatici e di trattamento illecito di dati nonché delitti in materia di violazione del diritto d’autore (Artt. 24bis e 25novies)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 2
2.LE AREE DI ATTIVITA’ “SENSIBILI” A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 24BIS E 25NOVIES DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI E LE SEGNALAZIONI VERSO L’ORGANISMO DI VIGILANZA
0. PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di individuare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti negli artt. 24bis e 25nonies del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti;
- a descrivere le regole di comportamento generali e specifiche finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto contemplati dalle disposizioni sopraindicate.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 2.
Iniziando dall’art. 24bis del D.Lgs. 231/01, lo stesso indica quali reati presupposto della responsabilità amministrativa dell’ente le seguenti fattispecie:
- Falsità in un documento informatico pubblico o avente efficacia probatoria (art. 491-bis c.p.);
- accesso abusivo a un sistema informatico o telematico (art. 615- ter c.p.);
- detenzione e diffusione abusiva di codici di accesso a sistemi informatici o telematici (art. 615 – quater c.p.);
- diffusione di apparecchiature, dispositivi o programmi informatici diretti a danneggiare o interrompere un sistema informatico o telematico (art. 615 – quinquies c.p.);
- intercettazione, impedimento o interruzione illecita di comunicazioni informatiche o telematiche (art. 617 – quater c.p.);
- installazione di apparecchiature atte a intercettare, impedire o interrompere comunicazioni informatiche o telematiche (art. 617 – quinquies c.p.);
- danneggiamento di informazioni, dati e programmi informatici (art. 635 – bis c.p.);
- danneggiamento di informazioni, dati e programmi informatici utilizzati dallo Stato o da altro Ente Pubblico o comunque di pubblica utilità (art. 635 – ter c.p.);
- danneggiamento di sistemi informatici e telematici (art. 635 – quater c.p.);
- danneggiamento di sistemi informatici e telematici di pubblica utilità (art. 635 – quinquies c.p.);
- frode informatica del soggetto che presta servizi di certificazione di firma elettronica (art. 640 – quinquies c.p.);
- violazione delle norme in materia di Perimetro di sicurezza nazionale cibernetica (art. 1, comma 11, D.L. n. 105 del 21/09/2019).
Quanto all’art. 25novies, i reati presupposto sono invece:
- messa a disposizione del pubblico, in un sistema di reti telematiche, mediante connessioni di qualsiasi genere, di un’opera dell’ingegno protetta, o di parte di essa (art. 171, legge n.633/1941 comma 1 lett. a) bis);
- reato di cui punto precedente commesso su opere altrui non destinate alla pubblicazione qualora ne risulti offeso l’onore o la reputazione (art. 171, legge n.633/1941 comma 3);
- abusiva duplicazione, per trarne profitto, di programmi per elaboratore; importazione, distribuzione, vendita o detenzione a scopo commerciale o imprenditoriale o concessione in locazione di programmi contenuti in supporti non contrassegnati dalla SIAE; predisposizione di mezzi per rimuovere o eludere i dispositivi di protezione di programmi per elaboratori (art. 171-bis legge n.633/1941 comma 1);
- riproduzione, trasferimento su altro supporto, distribuzione, comunicazione, presentazione o dimostrazione in pubblico, del contenuto di una banca dati; estrazione o reimpiego della banca dati; distribuzione, vendita o concessione in locazione di banche di dati (art. 171-bis legge n.633/1941 comma 2)
- abusiva duplicazione, riproduzione, trasmissione o diffusione in pubblico con qualsiasi procedimento, in tutto o in parte, di opere dell’ingegno destinate al circuito televisivo, cinematografico, della vendita o del noleggio di dischi, nastri o supporti analoghi o ogni altro supporto contenente fonogrammi o videogrammi di opere musicali, cinematografiche o audiovisive assimilate o sequenze di immagini in movimento; opere letterarie, drammatiche, scientifiche o didattiche, musicali o drammatico musicali, multimediali, anche se inserite in opere collettive o composite o banche dati; riproduzione, duplicazione, trasmissione o diffusione abusiva, vendita o commercio, cessione a qualsiasi titolo o importazione abusiva di oltre cinquanta copie o esemplari di opere tutelate dal diritto d’autore e da diritti connessi; immissione in un sistema di reti telematiche, mediante connessioni di qualsiasi genere, di un’opera dell’ingegno protetta dal diritto d’autore, o parte di essa (art. 171-ter legge n.633/1941)
- mancata comunicazione alla SIAE dei dati di identificazione dei supporti non soggetti al contrassegno o falsa dichiarazione (art. 171-septies legge n.633/1941)
- fraudolenta produzione, vendita, importazione, promozione, installazione, modifica, utilizzo per uso pubblico e privato di apparati o parti di apparati atti alla decodificazione di trasmissioni audiovisive ad accesso condizionato effettuate via etere, via satellite, via cavo, in forma sia analogica sia digitale (art. 171-octies legge n.633/1941).
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Alla luce delle caratteristiche normative delle predette fattispecie, il rischio di commissione delle stesse si concentra principalmente nelle seguenti aree di attività aziendale:
- gestione dei sistemi informatici e telematici connessi con reti esterne ed utilizzo dispositivi aziendali (personal computer, tablet, telefoni cellulari) attribuiti ai dipendenti per lo svolgimento dell’attività lavorativa;
- acquisizione, installazione ed aggiornamento dei software, programmi e/o applicativi presenti sui PC e sugli altri dispositivi aziendali consegnati ai lavoratori;
- attribuzione della qualifica di amministratore di sistema e, più in generale, gestione delle autorizzazioni ad accedere ai dati ed alle informazioni aziendali;
- gestione dei documenti elettronici o informatici con valore probatorio;
- interlocuzione con sistemi e/o portali telematici implementati dagli Enti Pubblici o dalle Autorità Regolatorie e/o di Vigilanza volte a regolamentare il settore di attività in cui opera Società Prodotti Antibiotici S.p.A.;
- eventuale predisposizione di certificazioni, dichiarazioni sostitutive o documenti informatici da produrre, consegnare, depositare ad AIFA, al Ministero della Salute o ad altri enti pubblici con cui SPA si rapporti nell’ambito delle proprie attività;
- selezione ed assunzione del personale di società concorrenti o di partner commerciali (che potrebbero rivelare o procurarsi password per accedere ai sistemi informatici delle stesse);
- caricamento sul sito di contenuti (pubblicitari o meno) caratterizzati da segni grafici e musicali o da riferimenti ad opere cinematografiche o letterarie drammatiche, scientifiche o didattiche, musicali o drammatico-musicali
- eventuale attività di marketing e di promozione dei prodotti attraversi canali televisivi e telematici;
- messa a disposizione di opere dell’ingegno, programmi, banche dati ed altre opere tutelate dal diritto d’autore nell’ambito degli studi clinici ed osservazionali nonché nell’organizzazione/sponsorizzazione degli eventi;
- attività di marketing,
Prima di entrare nel merito dei presidi e delle regole di condotta che occorre adottare in relazione alle predette attività sensibili, occorre precisare che, per quanto astrattamente ipotizzabili,[1] i reati presupposto contemplati dall’art. 25novies appaiono di difficile realizzazione nell’ambito dei processi aziendali di Società Prodotti Antibiotici S.p.A. Ed invero:
(a) La società non svolge alcuna attività di riproduzione, distribuzione, vendita o commercializzazione, noleggio o importazione di opere dell’ingegno destinate al circuito televisivo/cinematografico;
(b) I materiali promozionali e pubblicitari – oltre ad essere sottoposti ad uno stringente controllo della Direzione Scientifica e del Responsabile del Servizio Scientifico – devono essere preventivamente verificati ed approvati da AIFA;
(c) I contenuti da pubblicare sul sito internet o su eventuali pagine telematiche riconducibili all’azienda devono essere sottoposti allo stringente controllo di una pluralità di funzioni aziendali al fine di assicurare la conformità di quanto pubblicato ai principi contenuti nel Codice Deontologico di Farmindustria nonché alla normativa di settore.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 24BIS E 25NOVIES DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato sull’individuazione di principi generali e trasversali – che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali – e su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[2]
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, ai principi di comportamento specifici da porre in essere in relazione alle singole aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, la società ha adottato la SOP SSC.04.04 (avente ad oggetto la “gestione del sito internet aziendale”) ed ulteriori standard operative procedures che incidono a vario titolo su alcuni aspetti delle predette attività sensibili (come la SOP SSC.IS.01.07 in materia di “materiale informativo e promozionale”, e la SOP SSC.IS.03.06, concernente il “materiale informativo di consultazione scientifica o di lavoro e il materiale promozionale non specificatamente attinente al medicinale”).
I destinatari del presente Modello di Organizzazione e Gestione, ciascuno per la propria area di attribuzione e competenza, dovranno rispettare le seguenti regole di condotta:
- deve essere nominato un Amministratore di Sistema che sia dotato della necessaria competenza, esperienza e professionalità;
- la richiesta di creazione/modifica di un account deve essere effettuata a mezzo mail dal Responsabile del settore IT e deve indicare i dati del nuovo utente nonché la qualifica e le attribuzioni lavorative;
- gli accessi ai supporti informatici sono controllati mediante meccanismi di autenticazione degli utenti;
- le password di accesso ai dispositivi, ai gestionali, alle applicazioni e/o ai sistemi informatici sono strettamente personali e, in quanto tali, non debbono essere comunicate ad altri dipendenti dell’azienda o a soggetti terzi;
- ciascun utente è responsabile di qualsiasi operazione effettuata con la propria utenza e della riservatezza della proprie password, dovendo modificarle periodicamente al fine di evitare l’accesso indebito di altri soggetti;
- l’utilizzo della postazione di lavoro deve essere esclusivamente funzionale allo svolgimento delle attività aziendali o agli scopi autorizzati dalle funzioni aziendali interessate;
- ad ogni dipendente sono attribuiti “profili di accesso” in relazione all’attività svolta;
- ciascun utente deve rispettare i livelli autorizzativi attribuitigli in funzione del ruolo e della funzione svolta, non accedendo a dati e/o informazioni che non sarebbe autorizzato a consultare e/o visionare;
- ogni variazione dei profili di accesso deve essere preventivamente richiesta o autorizzata dall’Amministratore di Sistema identificato da Società Prodotti Antibiotici S.p.A.;
- le principali attività compiute attraverso tutti i dispositivi informatico/telematici in uso presso la società devono essere tracciabili, garantendo che tutti gli interventi aggiuntivi, modificativi o eliminatori siano ricostruibili ex post ed attribuibili ad un utente specifico;
- i prodotti software installati (sia sulle apparecchiature assegnate all’utenza che relativi alle infrastrutture di rete) sono approvati da Società Prodotti Antibiotici S.p.A. o dal fornitore terzo di cui la stessa eventualmente si avvale: gli stessi sono correttamente licenziati nonchè aggiornati e/o rinnovati a cura della società o del fornitore alle debite scadenze;
- occorre periodicamente verificare che le licenze di utilizzo di banche dati siano acquistate ed utilizzate nel rispetto di quanto previsto dalle condizioni contrattuali;
- i soggetti alle dipendenze di Società Prodotti Antibiotici S.p.A. che abbiano a disposizione un dispositivo telematico per lo svolgimento dell’attività aziendale non devono scaricare o installare software non licenziati o comunque non previamente autorizzati dal Responsabile IT, dalla società o dal fornitore terzo di cui la stessa si avvale;
- le installazioni di software sui personal computer o su altri dispositivi telematici aziendali devono essere effettuate solamente da personale tecnico autorizzato;
- è fatto divieto di detenere, intercettare o diffondere abusivamente codici d’accesso o ogni altro mezzo idoneo all’accesso di un sistema protetto da misure di sicurezza;
- in occasione di colloqui finalizzati all’assunzione di personale con un candidato che provenga da una società concorrente, è vietato chiedere informazioni e notizie circa codici di accesso e/o password in uso presso l’azienda di provenienza;
- in occasione di colloqui con un candidato che provenga dalla Pubblica Amministrazione o da un’Autorità Regolatoria o di Vigilanza deputata a disciplinare il settore in cui opera SPA, e, è vietato chiedere informazioni e notizie circa codici di accesso e/o password in uso presso l’ente o l’Autorità di provenienza;
- è vietato utilizzare la strumentazione aziendale (hardware/software) per trasmettere dati, informazioni, programmi finalizzati a distruggere, danneggiare o ostacolare il funzionamento di sistemi informatici o telematici di pubblica utilità;
- è vietato trasferire su risorse pubbliche aziendali dati non destinati alla diffusione, nonché dati d’interesse strategico aziendale;
- è vietato effettuare download, trasmettere, distribuire o possedere materiale a contenuto di natura oltraggiosa e/o discriminatoria per sesso, lingua, religione, razza, origine etnica, opinione e appartenenza sindacale e/o politica;
- allo stesso modo, è vietato effettuare download, trasmettere, distribuire o conservare sul proprio PC o in qualsiasi server aziendale, programmi per elaboratori, banche dati protette ovvero qualsiasi opera protetta dal diritto d’autore e da diritti connessi, incluse opere a contenuto letterario, musicale, multimediale, cinematografico, artistico nonché mettere in atto pratiche di scaricamento dati (file sharing), attraverso lo scambio e la condivisione di qualsivoglia tipologia di file attraverso piattaforme presenti sul web;
- è necessario che ogni utente si conformi alle indicazioni elencate, legate all’utilizzo della Posta Elettronica, che è uno strumento di lavoro. Ne è, pertanto, vietato l’utilizzo, anche occasionale, per fini personali;
- l’utilizzazione della pec aziendale deputata alla trasmissione di comunicazioni/istanze/atti verso la Pubblica Amministrazione o verso Autorità di Vigilanza/Regolatorie è unicamente consentita ai soggetti che siano a ciò espressamente autorizzati;
- i soggetti autorizzati a rappresentare Società Prodotti Antibiotici S.p.A. davanti alla Pubblica Amministrazione nonché alle Autorità Regolatorie e/o di Vigilanza (e pertanto legittimati ad interfacciarsi con eventuali portali telematici messi a disposizione dagli stessi) devono essere chiaramente identificati attraverso l’attribuzione di procure o deleghe;
- i documenti informatici inseriti sui sistemi gestionali in uso presso la Pubblica Amministrazione o le Autorità Regolatorie o di Vigilanza debbono contenere dati ed informazioni non alterate e corrispondenti al vero;
- è vietato utilizzare la firma elettronica certificata altrui o alterare la forma e/o contenuto dei messaggi o documenti inviati attraverso tale procedura;
- devono essere predisposte e mantenute adeguate misure di sicurezza per la protezione dei dati personali e sensibili trattati da Società Prodotti Antibiotici nell’esercizio della sua attività;
- i dati raccolti o trattati da SPA devono essere trattati nel pieno rispetto delle disposizioni emesse dagli Organi di Vigilanza e nel rispetto del Codice in materia di protezione dei dati personali;
- sono previste specifiche soluzioni di disaster recovery che assicurino il recupero dei dati e la normale operatività del sistema anche in soluzioni di emergenza. In questo senso, tutti i dati immessi nei sistemi informatici aziendali vengono archiviati sul server e vengono sottoposti a backup periodici;
- l’eventuale accesso, da parte di soggetti terzi, ai sistemi informatici o gestionali di Società Prodotti Antibiotici S.p.A. nonché ai dati in essi contenuti può essere autorizzato solo dall’Amministratore di Sistema;
- l’infrastruttura informatica di Società Prodotti Antibiotici S.p.A. è dotata di un sistema anti-virus ed antispamming costantemente aggiornato;
- i contratti con soggetti terzi che siano eventualmente chiamati a svolgere attività sugli apparati o sistemi informatici di SPA (outsourcer informatici) debbono contenere apposite clausole di conoscenza dei principi e della normativa di cui al D.Lgs. 231/01;
- in caso di violazioni di tali clausole debbono essere previste sanzioni in capo al fornitore che, nei casi più gravi, possono arrivare sino alla risoluzione del contratto;
- deve essere istituito un canale telematico per inviare segnalazioni circa violazioni – accertate o presunte – del Codice Etico, del Modello di Organizzazione e Gestione nonché delle procedure e/o istruzioni operative aziendali;
- Il materiale promozionale avente ad oggetto medicinali o farmaci commercializzati da SPA deve essere verificato ed approvato da AIFA;
- i contenuti promozionali o pubblicitari pubblicati sul sito o su qualsivoglia pagina telematica riconducibile alla società debbono essere previamente verificati dalle funzioni identificate nella procedura adottata internamente;
- le funzioni aziendali coinvolte nella progettazione delle campagne commerciali e nelle attività di definizione del materiale pubblicitario legate allo sviluppo di nuovi prodotti o al rilancio di prodotti esistenti sono chiamate ad eseguire verifiche e controlli sull’uso di marchi registrati, segni distintivi ovvero di brevetti, modelli e disegni oltre a controlli sulla compliance dei prodotti offerti;
- ogni contratto con agenzie pubblicitaria per la realizzazione di manifesti, video e inserzioni pubblicitari deve essere formalizzato con l’espressa inclusione di clausole finalizzate al rispetto della normativa in materia di diritto d’autore;
- l’utilizzo di video, materiale fotografico o fonografico da utilizzarsi per i messaggi pubblicitari è subordinato al previo rilascio da parte dell’agenzia pubblicitaria dell’attestazione per iscritto dell’avvenuto esaurimento delle pratiche SIAE;
- è vietato l’impiego di beni aziendali (come fotocopiatrici, sito web, copisterie o altro) al fine di porre in essere condotte che violino la tutela dei diritti d’autore, quale che sia il vantaggio perseguito.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Secondo quanto indicato nei “case study” elaborato da Confindustria in occasione dell’ultimo aggiornamento delle linee guida per la costruzione dei Modelli di Organizzazione, Gestione e Controllo “I reati presupposto inseriti nell’art. 25-novies non sono fattispecie di reato di esclusivo interesse delle imprese operanti nello specifico settore software/audiovisivo, ma, al contrario, alcune fattispecie di reato impongono, alla quasi totalità dei soggetti collettivi portatori di interesse economico che intendono contenere i rischi, l’esigenza di porre in essere specifiche misure e protocolli” (p. 109 del case study pubblicato nel giugno 2021 da Confindustria).
[2] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 3
Reati Societari (art. 25ter)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 3
2.LE AREE DI ATTIVITA’ “SENSIBILI” A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25TER DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI E LE SEGNALAZIONI VERSO L’ORGANISMO DI VIGILANZA
0. PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di individuare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti nell’art. 25ter del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti;
- a descrivere le regole di comportamento generali e specifiche finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 3.
Le fattispecie indicate dall’art. 25ter quali presupposto della responsabilità amministrativa dell’ente sono le seguenti:
- false comunicazioni sociali (art. 2621 c.c.) e fatti di lieve entità (art. 2621bis c.c.);
- false comunicazioni sociali delle società quotate (art. 2622 c.c.);
- falso in prospetto (art. 2623 c.c.);
- falsità nelle relazioni o nelle comunicazioni delle società di revisione (art. 2624 c.c.);
- impedito controllo (art. 2625 comma 2 c.c.);
- indebita restituzione dei conferimenti (art. 2626 c.c.);
- illegale ripartizione degli utili e delle riserve (art. 2627 c.c.);
- illecite operazioni sulle azioni o quote sociali o della società controllante (art. 2628 c.c.);
- operazioni in pregiudizio dei creditori (art. 2629 c.c.)
- omessa comunicazione del conflitto d’interessi (art. 2629-bis c.c.);
- interessi degli amministratori (art. 2391, c.1, c.c.);
- formazione fittizia del capitale (art. 2632 c.c.);
- indebita ripartizione dei beni sociali da parte dei liquidatori (art. 2633 c.c.);
- illecita influenza sull’assemblea (art. 2636 c.c.);
- Aggiotaggio (art. 2637 c.c.);
- ostacolo all’esercizio delle funzioni delle autorità pubbliche di vigilanza (art. 2638 comma 1 e 2 c.c.).
Nel predetto elenco, non sono stati riportati i delitti di cui al terzo comma dell’art. 2635 c.c. (corruzione tra privati) e di cui al primo comma dell’art. 2635bis c.c. (Istigazione alla corruzione tra privati), in quanto gli stessi sono stati trattati nella parte speciale n. 1, unitamente alle fattispecie presupposto contemplate negli artt. 24 e 25 del D.Lgs. 231/01.
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Al fine di una corretta individuazione delle aree di attività aziendale che comportano un maggiore rischio di commissione dei reati oggetto della presente parte speciale, occorre premettere che i cd. “reati societari” sono prevalentemente “reati propri”, che, in quanto tali, possono essere commessi solo ed esclusivamente da coloro che ricoprono una determinata qualifica o qualità espressamente indicata dalla norma incriminatrice. Tale qualifica, a seconda delle singole ipotesi di reato è quella di amministratore delegato, direttore generale, dirigente proposti alla redazione dei documenti contabili, sindaco e liquidatore.
Ciò peraltro non esclude che altri soggetti possano concorrere in tali reati (cd. concorso dell’extraneus nel reato proprio, ammesso da dottrina e giurisprudenza ai sensi dell’art. 110 c.p., alla sola condizione che sussista in capo all’extraneus la consapevolezza in ordine alla qualità soggettiva dell’intraneus determinante il titolo di reato applicabile).[1] In linea teorica, potrebbero quindi concorrere nel reato dipendenti di Società Prodotti Antibiotici S.p.A. non aventi le specifiche qualifiche previste dalla legge ed operanti nell’ambito non solo della Direzione Controlling & Finance ma anche della altre Direzioni. Questi ultimi, in particolare, potrebbero ad esempio concorrere nel reato ove trasmettessero alla Direzione Controlling & Finance informazioni errate o false.
Tanto premesso e considerate le caratteristiche normative delle predette fattispecie, il rischio di commissione delle stesse si concentra principalmente nelle seguenti aree di attività aziendale:
- formazione ed approvazione del bilancio;
- processi di fatturazione attiva o passiva;
- operazioni sul capitale sociale;
- acquisto e sottoscrizione di azioni o di quote sociali, anche emesse dalla società controllante e/o da società controllate;
- approvazione dei documenti concernenti le predette operazioni;
- operazioni straordinarie (fusioni o scissioni);
- operazioni infragruppo;
- svolgimento dei consigli di Amministrazione ed assunzione delle relative deliberazioni;
- controlli e verifiche legalmente attribuite ai soci o ad altri organi sociali;
- redazione, approvazione e diffusione di comunicazioni rivolte ad operatori del settore.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25TER DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[2]
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, ai principi di comportamento specifici, Società Prodotti Antibiotici S.p.A. – oltre a predisporre alcune SOP specifiche in tema di fatturazione attiva e passiva (la SOP AMM.04.01 concernente la gestione fatturazione dei clienti e la SOP AMM.03.01 relativa alla gestione del ciclo passivo) – ha adottato uno Statuto che regola in modo puntuale il funzionamento degli organi amministrativi e sociali e, al di là di quanto previsto all’interno di tale documento, si attiene scrupolosamente al rispetto della normativa del codice civile nonché delle disposizioni di legge e/o linee guida nazionali ed internazionali poste a salvaguardia dell’integrità ed effettività del capitale sociale, promuovendo un atteggiamento collaborativo e trasparente nei confronti del mercato e delle Autorità di Vigilanza.
In questo senso, i comportamenti che i destinatari del presente Modello di Organizzazione e Gestione dovranno adottare al fine di ridurre la possibilità di realizzazione dei reati qui considerati verranno trattati attraverso una suddivisione in alcune macro-aree che ricomprendono i processi sensibili individuati nel paragrafo n. 2 della presente Parte Speciale:
Con riguardo a tutte le attività propedeutiche alla corretta formazione del bilancio ed all’approvazione di tale documento, sono previste le seguenti regole di condotta:
- sono adottati gestionali che assicurano l’automatica creazione di fatture attive e passive a fronte dell’inserimento della documentazione concernente l’operazione effettuata o la prestazione ricevuta nonché di scaricare o ricevere le fatture passive emesse dai fornitori e che sono idonei ad interfacciarsi e/o rapportarsi con i portali predisposti dall’Agenzia delle Entrate;
- prima di procedere all’invio al Sistema di Interscambio delle fatture attive in formato XML, devono essere effettuati controlli sui documenti fiscali provvisori creati a partire dalla documentazione inserita a gestionale;
- il sistema di trasmissione ed interscambio, deve essere costantemente monitorato accertando la sussistenza di eventuali rifiuti circa la documentazione caricata ed adottando tempestivamente le opportune azioni correttive;
- l’emissione e la conservazione delle fatture attive e passive è conforme a quanto previsto dalla normativa in tema di fatturazione elettronica,;
- al di là di quanto previsto dalla normativa in tema di fatturazione elettronica, la registrazione di dati e documenti a rilevanza contabile (ad es. fatture, note di credito, note di debito, pagamenti, incassi, etc.) avviene a mezzo di appositi e dedicati sistemi informatici gestiti direttamente da Società Prodotti Antibiotici S.p.A. o da fornitori terzi dei quali la stessa si avvale;
- ogni fattura e nota di credito deve evidenziare in modo completo e comprensibile i prodotti e servizi resi e ogni altro dato obbligatorio e per ogni nota di credito deve esser indicata e registrata la data di pagamento;
- ogni Direzione o Divisione aziendale deve comunicare tempestivamente per iscritto alla Direzione Amministrazione e Finanza i dati riguardanti operazioni che implicano accantonamento in Fondo Rischi;
- le singole Direzioni e/o Divisioni trasmettono alla Direzione Amministrazione, Finanza e Controllo ogni informazione rilevante ai fini della formazione del bilancio, per consentirne il controllo e garantirne, la veridicità, la correttezza, la precisione e la completezza;
- la trasmissione dei dati rilevanti a fini contabili deve avvenire mediante sistema informatico che consenta di tracciare i singoli passaggi e di identificare i soggetti che inseriscono e ricevono i dati;
- il Responsabile della Direzione Amministrazione Finanza e Controllo ed i professionisti terzi eventualmente incaricati della preparazione, redazione e verifica del bilancio societario sono tenuto a garantire l’applicazione dei principi di redazione del bilancio contenuti nel codice civile nonché dei principi contabili internazionali o a verificare il rispetto di tali disposizioni;
- i professionisti cui è affidata la redazione del bilancio e dei documenti connessi (nota integrativa, prospetti di bilancio etc.) devono essere selezionati tra soggetti dotati della necessaria professionalità e competenza;
- deve essere verificata la corrispondenza tra il bilancio da depositare ed i dati estratti dal sistema informatico, al fine di identificare eventuali scostamenti e di risolvere, di conseguenza, eventuali anomalie;
- il CFO trasmette al CdA un documento contenente dati relativi al progetto di bilancio e/o della relazione della società di revisione nonché una bozza del progetto di bilancio prima della relativa riunione del CdA stesso;
- la Direzione Amministrazione Finanza e Controllo mette a disposizione dei componenti del CdA la relazione sul bilancio predisposta dalla società di revisione.
****
Per quanto riguarda le operazioni sul capitale sociale, il regolare funzionamento e andamento della Società nonché dei suoi organi, si richiamano le seguenti regole di condotta:
- eventuali operazioni di ripartizione di utili e/o di restituzione di conferimenti vanno realizzate nel pieno rispetto della normativa contenuta nel codice civile e delle ulteriori disposizioni poste a salvaguardia del capitale sociale nonché delle riserve di legge obbligatorie;
- è vietato sottoscrivere o acquistare quote proprie o procedere ad aumenti di capitale fittizi per il tramite dell’attribuzione di quote per un valore inferiore a quello nominale;
- non è possibile effettuare riduzioni del capitale sociale, fusioni o scissioni in violazione delle disposizioni di legge a tutela dei creditori
- al Collegio Sindacale deve essere comunicata tempestivamente l’eventuale sussistenza di un conflitto di interesse (anche solo potenziale) che abbia ad oggetto il compimento di un’operazione di amministrazione ordinaria o straordinaria;
- debbono essere favoriti gli opportuni accertamenti e verifiche da parte dei soci, del Collegio Sindacale o delle funzioni coinvolte negli audit o nelle attività ispettive svolte a livello interno;
- è necessario mettere a disposizione dei soci e degli altri organi sociali tutta la documentazione sulla gestione della società necessaria ad effettuare le attività di controllo legalmente attribuite agli stessi, senza occultare alcun dato e/o informazione;
- è vietato porre in essere, in occasione di assemblee, atti simulati o fraudolenti, finalizzati ad alterare il regolare procedimento di formazione della volontà assembleare;
- occorre mantenere riservate tutte le informazioni e i documenti acquisiti nello svolgimento delle proprie funzioni, con particolare riguardo ai dati relativi alla gestione economico-finanziaria della società (oltre a custodire accuratamente tutta la documentazione che contenga tali informazioni autorizzando l’accesso solo ai soggetti a ciò abilitati);
- tutte le comunicazioni societarie eventualmente rese a soggetti terzi debbono essere improntate ad uno scrupoloso rispetto dei dati e delle informazioni risultanti dalla documentazione contabile predisposta dalla Direzione Amministrazione e verificata dal Collegio Sindacale.
Con riguardo ai rapporti infragruppo:
- deve essere garantita una chiara segregazione di funzioni tra chi provvede alla predisposizione della documentazione inerente i rapporti infragruppo, chi la verifica e chi l’autorizza;
- tutte le transazioni o operazioni realizzate all’interno del gruppo tra società controllate e controllanti devono essere registrate e perfettamente tracciabili;
- le operazioni infragruppo devono essere coerenti con quelle realizzate con parti o soggetti terzi che operano in condizioni similari;
- occorre provvedere all’archiviazione sistematica dei dati e delle informazioni utilizzate ai fini della predisposizione della documentazione richiesta dalla normativa in tema di transfert pricing;
- le restituzioni dei conferimenti realizzati a favore della società controllata debbono avvenire nel pieno rispetto della normativa vigente.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Ad esempio, benchè la Direzione Finanza e Controllo sia la principale responsabile della formazione del bilancio e la principale detentrice dei saldi contabili di fine anno, numerose sono le operazioni – saldi contabili parziali, fatturazione, rimanenze, etc. – realizzate a monte all’interno di altre Direzioni Generali, Direzioni, Aree o Settori che possono concorrere all’elaborazione di risultanze finali (bilancio finale, nota integrativa e relazione sulla gestione) erronee o false.
Infatti, la conoscenza dei c.d. principi contabili, indispensabile per una compiuta attività di formazione e valutazione del bilancio, di competenza della Direzione Controlling & Finance “non impedisce una errata indicazione di importi di importi nel bilancio o una errata esposizione di fatti nella nota integrativa, se le informazioni sottostanti che debbono pervenire dalle altre funzioni aziendali sono errate per colpa o per dolo” (cfr. Linee guida per la costruzione dei modelli di organizzazione, gestione e controllo ex. D.Lgs. 231/2001, Confindustria, 31 marzo 2008, p. 84).
[2] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 4
Reati contro l’industria ed il commercio e contro la fede pubblica (artt. 25bis e 25bis1)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 4
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 25BIS E 25BIS1 DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA
0. PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti negli artt. 25bis e 25bis 1 del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto oggetto della presente parte speciale.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 4.
Iniziando dall’art. 25 bis1, le fattispecie indicate quali presupposto della responsabilità amministrativa dell’ente sono le seguenti:
- Turbata libertà dell’industria o del commercio (art. 513 c.p.);
- Illecita concorrenza con minaccia o violenza (art.513-bis c.p.);
- Frodi contro le industrie nazionali (art. 514 c.p.);
- Frode nell’esercizio del commercio (art. 515 c.p.);
- Vendita di prodotti industriali con segni mendaci (art. 517 c.p.);
- Fabbricazione e commercio di beni realizzati usurpando titoli di proprietà industriale (art. 517-ter c.p.).
In relazione all’articolo 25 bis del D.Lgs. 231/01, avente ad oggetto i delitti contro la fede pubblica, si elencano di seguito i soli reati ritenuti potenzialmente applicabili con riferimento all’oggetto sociale della società, rimandando per il resto alla già citata appendice normativa. Nello specifico:
- Falsificazione di valori di bollo, introduzione nello Stato, acquisto, detenzione o messa in circolazione di valori di bollo falsificati (art. 459 c.p.);
- Uso di valori di bollo contraffatti o alterati (art. 464 c.p.)
- Contraffazione, alterazione o uso di marchi o segni distintivi ovvero di brevetti, modelli e disegni (art. 473 c.p.);
- Introduzione nello Stato e commercio di prodotti con segni falsi (art. 474 c.p.).
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Alla luce delle caratteristiche normative delle predette fattispecie e della struttura della società, i processi aziendali che presentano un astratto rischio di commissione dei reati sopra elencati sono i seguenti:
- predisposizione dei dossier da sottoporre ad AIFA al fine di ottenere l’autorizzazione all’immissione in commercio di un determinato farmaco o di richiedere modifiche o variazioni all’AIC già ottenute;
- trasmissione di richieste e/o materiali ad AIFA e gestione dei rapporti con la stessa; e/ con il Ministero della Salute;
- predisposizione, aggiornamento e diffusione di cataloghi, brochure, newsletter, pubblicazioni ed ogni altro documento e/o strumento utilizzato a fini promozionali;
- gestione delle vendite a farmacie, grossisti e strutture sanitarie;
- gestione degli artwork;
- monitoraggio del processo produttivo presso terzi, confezionamento ed apposizione del marchio e dei bollini ottici (attività potenzialmente sensibile in virtù di quanto previsto dal decreto 4 agosto 2003 del Ministro dell’economia e delle finanze che, nelll’aggiornare le procedure di produzione dell’Istituto poligrafico e zecca dello Stato (IPZS), ha equiparato il bollino farmaceutico alle carte valori al pari dei francobolli o dei valori bollati);
- attività di monitoraggio e controllo dello stato di conservazione dei farmaci custoditi nei depositi e/o magazzini in uso alla società;
- gestione dei rapporti economico/commerciali con altre realtà operanti nel settore farmaceutico nonché con associazioni mediche, associazioni di pazienti ed associazioni scientifiche;
- assunzione di personale proveniente da società concorrenti o comunque operanti nello stesso settore di Società Prodotti Antibiotici S.p.A.;
- gestione dei marchi registrati e non.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25TER DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[1]
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, alle specifiche condotte da porre in essere in relazione alle aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, la società ha adottato le seguenti SOP:
- QA-03.02 “Difettosità”;
- QA.04.02 “Richiami”;
- QA.CQ.05.03 “Gestione certificati e controcampioni dei lotti di specialità prodotti e rilavorati dai terzisti”;
- QA.CQ.06.01 “Tracciabilità del farmaco: gestione dati dai siti di produzione”;
- QA.CQ.08.01 “Gestione dei bollini ottici”;
- QA.09.02 “Approvazione artworks e materiali di confezionamento stampati”;
- QA.CQ.13.01 “Etichette e foglietti illustrativi in lingua tedesca”;
- DV.01.07 “Campioni gratuiti”;
- IT.IT.03.01 “Tracciabilità del farmaco: tracciati SFR e MOV”;
- RA.CQ.02.01 “Gestione stampati nel sistema Farmastampati”;
- SSC/IS/01.07 “Materiale informativo e promozionale”.
Anche alla luce di quanto stabilito all’interno di tali documenti, i destinatari del presente Modello di Organizzazione e Gestione, ciascuno per la propria area di attribuzione e competenza, dovranno:
- monitorare in modo stringente la completezza, esaustività ed accuratezza della documentazione da depositare presso AIFA/Ministero della Salute per l’ottenimento dell’AIC, favorendo un controllo preventivo a cura delle funzioni competenti (Direzione Scientifica, Regolatorio etc.);
- assicurare la completezza e correttezza dei dati inseriti nelle richieste e/o istanze finalizzate alla registrazione di determinati prodotti (ad es. reagenti in vitro) presso il Ministero della Salute;
- condurre – anche attraverso società terze – verifiche, ispezioni e/o altri controlli in ordine ai fornitori, per conto di Società Prodotti Antibiotici S.p.A., si occupano del processo produttivo dei farmaci così come dell’azienda che si occupa del confezionamento;
- implementare presidi e controlli che consentano di garantire la piena tracciabilità dei lotti di prodotto consegnati presso i depositi;
- al momento della ricezione presso il magazzino fiduciario di ogni lotto di prodotto finito, verificare la completezza ed esaustività della documentazione trasmessa dalla società terza (a titolo esemplificativo e non esaustivo certificato di analisi e dichiarazione di conformità) nonché i controcampioni concernenti ciascun lotto;
- acquistare bollini ottici esclusivamente dall’Istituto Poligrafico e Zecca dello Stato in base alle giacenze di magazzino ed agli ordini di produzione previsti, installando la relativa applicazione web fornita dal predetto Istituto;
- garantire la corretta archiviazione della documentazione inerente l’acquisto dei bollini ottici e conservare i bollini in condizioni idonee all’interno di locali caratterizzati da misure di sicurezza;
- segnalare tempestivamente l’eventuale furto o distruzione di bollini ottici, provvedendone allo smaltimento dei bollini quale rifiuto farmaceutico;
- assicurare la corretta trasmissione di tutti i dati concernenti i bollini ottici al Ministero della Salute, provvedendo a nominare un soggetto deputato alla trasmissione delle informazioni di cui all’art. 3, commi 2, 3 e 4 del Decreto del Ministero della Salute 15 luglio 2004 alla banca dati centrale;
- assicurare che gli artwork o gli ulteriori materiali di confezionamento stampati siano conformi ai testi approvati da AIFA ed alle ulteriori indicazioni provenienti dalla stessa;
- garantire la piena tracciabilità di tutta la documentazione relativa alla predisposizione/autorizzazione dei testi e della bozza finale dell’artwork, che deve essere opportunamente conservata presso la funzione competente;
- adottare idonee ed efficaci misure per assicurare che la documentazione illustrativa avente ad oggetto il medicinale contenga informazioni veritiere, corrette ed aggiornate, stabilendo, a tal fine, una periodica revisione/aggiornamento della stessa;
- pubblicare in Gazzetta Ufficiale, laddove richiesto dalla normativa vigente, le variazioni degli stampati (foglio illustrativo) concernenti i medicinali rispetto cui SPA è titolare di AIC;
- assicurare il corretto adempimento dei flussi informativi nei confronti di Farmastampati, garantendo la trasmissione di tutte le informazioni concernenti le modifiche apportate e la tempestiva indicazione del primo lotto di prodotti medicinali caratterizzato dagli stampati aggiornati;
- coinvolgere il Responsabile del Servizio Scientifico nell’analisi della documenti o del materiale promozionale così da garantire che le informazioni contenute negli stessi siano conformi a quanto presentato ai fini del rilascio dell’autorizzazione all’immissione in commercio o ai suoi aggiornamenti;
- depositare il predetto materiale presso AIFA per l’approvazione;
- non distribuire materiale o documentazione promozionale che non sia stato preventivamente approvato da AIFA o la cui verifica abbia dato esito negativo;
- verificare che il materiale prodotto o stampato sia conforme a quello approvato da AIFA;
- formulare un piano annuale concernente la quantità dei campioni gratuiti necessari alle attività di promozione;
- garantire che i campioni di medicinali siano graficamente identici alla confezione più piccola messa in commercio e siano idonei sotto il profilo terapeutico, specificando eventuali caratteristiche e/o differenze (a livello, ad esempio, di unità posologiche) sull’etichetta;
- assicurare che i campioni gratuiti distribuiti presso gli Informatori Scientifici del Farmaco siano conservati adeguatamente, predisponendo adeguati flussi informativi con gli ISF;
- condurre – anche attraverso consulenti dotati della necessaria competenza ed esperienza – valutazioni di fattibilità tecnico/economica/giuridica in merito alla possibilità di registrare un marchio/denominazione di un prodotto o una metodologia di packaging secondo criteri predeterminati ed oggettivi, verificando che non siano integrate contraffazioni/alterazioni di un marchio, denominazione, disegno o modello già esistente;
- prevedere presidi e controlli atti a monitorare la data di scadenza dei marchi registrati;
- in caso di commercializzazione di prodotti riconducibili a società terze – per i quali SPA abbia l’esclusiva o la concessione di vendita sul territorio nazionale – verificare presso la società che il marchio e/o segno distintivo riportato sui beni distribuiti sia correttamente stato registrato o che, comunque, siano state osservate le norme delle leggi interne, dei regolamenti comunitari e delle convenzioni internazionali sulla tutela della proprietà intellettuale o industriale;
- garantire lo svolgimento di audit o ispezioni presso le società i cui prodotti vengono distribuiti o commercializzati sul mercato nazionale;
- non commercializzare prodotti con nomi, marchi o segni distintivi nazionali o esteri atti a indurre in inganno il compratore sull’origine, provenienza o qualità dell’opera o del prodotto;
- improntare i rapporti con le società concorrenti alla massima correttezza e trasparenza, garantendo la piena tracciabilità e documentabilità delle comunicazioni o dei rapporti eventualmente intercorsi con gli stessi;
- non contattare, direttamente o indirettamente, dipendenti, dirigenti o collaboratori di società concorrenti al fine di ottenere notizie, dati o informazioni che siano da considerarsi riservate o segrete;
- in sede di colloqui finalizzati all’assunzione di soggetti precedentemente impiegati presso società concorrenti o comunque attive nel medesimo settore di SPA, non richiedere (direttamente o indirettamente) informazioni riservate o segrete che abbiano ad oggetto, a titolo esemplificativo e non esaustivo, metodologie produttive, elenchi di clienti e/o fornitori, prezzi o condizioni commerciali, forme o modalità di scontistica;
- non porre in essere condotte che possano determinare discredito in capo ad una società concorrente e/o ai servizi offerti dalla stessa o, alternativamente, appropriarsi dei pregi e delle qualità di un’altra azienda;
- garantire che l’attività di informazione scientifica posta in essere attraverso gli ISF, o gli Area Manager avvenga conformemente a quanto stabilito dalla normativa di settore e dal Codice Deontologico di Farmindustria, senza indebiti confronti e/o paragoni con prodotti commercializzati da altre società farmaceutiche.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 5
Reati di omicidio colposo o lesioni gravi o gravissime commesse con violazione delle norme sulla tutela della salute e sicurezza sul lavoro (Art. 25septies)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 5
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25SEPTIES DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche: un’analisi dei presidi e delle regole di comportamento alla luce della formulazione dell’art. 30 del D.Lgs. 81/08
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA
0. PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti nell’art. 25septies del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto di cui all’art. 25septies del D.Lgs. 231/01.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 5.
I reati presupposto contemplati dall’art. 25septies del D.Lgs. 231/01 sono i seguenti:
- omicidio colposo (art. 589 c.p.) commesso con violazione della normativa a tutela della salute e sicurezza sul lavoro;
- lesioni personali colpose gravi o gravissime (art. 590 c.p.) commesse con violazione della normativa a tutela della salute e sicurezza sul lavoro.
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Dall’esame della documentazione aziendale e dalle circostanze riferite nel corso delle interviste svolte nell’ambito dell’attività di mappatura del rischio, è emerso che Società Prodotti Antibiotici S.p.A. è dotata di sedi deputate esclusivamente allo svolgimento di attività amministrative, essendo priva di propri stabilimenti produttivi e di magazzini deputati allo stoccaggio/trasmissione dei prodotti destinati all’immissione in commercio. In particolare, le attività di produzione dei farmaci per cui SPA è titolare AIC e/o degli ulteriori prodotti nonchè la gestione del magazzino sono state esternalizzate presso società terze. Medesime considerazioni possono esprimersi con riguardo alla specifica Divisione BIOSPA che, ad eccezione dei flussi materiali che riguardano la produzione interna, si serve di un fornitore esterno per le attività di magazzino e spedizioni, ivi incluso il mantenimento in condizioni speciali dei prodotti che lo richiedano.[1]
Tali circostanze determinano – com’è ovvio – una rilevante diminuzione dei rischi connessi alla commissione dei reati presupposto di cui all’art. 25septies, in quanto, come riferito dall’RSPP nel corso delle interviste, gli infortuni sono “prevalentemente costituiti da incidenti occorsi agli Informatori Scientifici del Farmaco mentre si spostano nell’area territoriale loro assegnata. E’ capitato (sebbene raramente) che si verificassero cadute o scivolamenti anche in sede ma si tratta di episodi che possono contarsi sulle dita di una mano”.
Se ciò è vero, è altresì innegabile che l’importanza di prevenire o minimizzare i rischi di commissione dei reati presupposto di cui all’art. 25septies D.Lgs. 231/01 è sensibilmente aumentata a fronte dell’attuale situazione di emergenza epidemiologica e dei rischi connessi allo svolgimento in presenza delle attività aziendali. In questo senso – sul presupposto che l’infezione da Covid-19 contratta in occasione dello svolgimento dell’attività lavorativa è stata equiparata ad un infortunio professionale (art. 42 del D.L. 18/2020 così come successivamente convertito dalla L. 27/2020 e circolare n. 22/2020 INAIL) – è necessario assicurare una rigorosa attuazione di tutti i protocolli sottoscritti tra le parti sociali al fine di garantire la prosecuzione delle attività produttive, individuando organi che verifichino l’implementazione delle misure necessarie.
L’esigenza di assicurare il pieno rispetto delle norme poste a tutela della salute e sicurezza dei lavoratori si lega altresì alla presenza di un laboratorio aziendale all’interno della Divisione BIOSPA che, per quanto limitato, si caratterizza per l’utilizzo di apparecchiature di produzione, strumentazione di controllo, e per la gestione di alcuni composti e/o sostanze artificiali.
Tanto premesso, si elencano di seguito le aree di attività aziendali che possono essere considerate “sensibili” ai sensi e per gli effetti dell’art. 25septies del D.Lgs. 231/01:
- svolgimento delle attività lavorative presso gli uffici e/o locali in uso alla Società in cui siano impiegate una pluralità di persone;
- gestione degli accessi di soggetti terzi;
- approvvigionamento e fornitura di igienizzanti, dispositivi di protezione individuale e/o altri elementi espressamente indicati all’interno dei protocolli sottoscritti tra le parti sociali al fine di prevenire il rischio da contagio;
- sovraesposizione dei dipendenti ai dispositivi telematici in uso agli stessi per lo svolgimento delle attività lavorative:
- gestione del telelavoro e dello smartworking;
- interventi di manutenzione all’interno degli stabili in cui sono collocati gli uffici amministrativi;
- manutenzione delle autovetture aziendali assegnate ai dipendenti;
- visite al laboratorio aziendale;
- manutenzione delle apparecchiature di produzione e della strumentazione di controllo utilizzate nell’ambito del laboratorio di BIOSPA e, in generale, all’interno di tale Divisione;
- attività di sviluppo/ricerca eventualmente svolte all’interno del laboratorio della Divisione BIOSPA, con particolare riguardo all’utilizzo (ed alla relativa conservazione) di sostanze e/o reagenti chimici;
- organizzazione e svolgimento di corsi di formazione in tema di salute e sicurezza sul lavoro.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25SEPTIES DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[2]
3.2. Le regole di comportamento specifiche: un’analisi dei presidi e delle regole di comportamento alla luce della formulazione dell’art. 30 del D.Lgs. 81/08.
Con riguardo ai secondi, è necessario partire dalla disposizione di cui all’art. 30 del D.Lgs. 81/08, che, come noto, rappresenta il parametro di riferimento per valutare l’idoneità ed efficacia del Modello di Organizzazione e Gestione rispetto alla prevenzione dei reati di cui all’art. 25septies del D.Lgs. 231/01.
Tale disposizione, in particolare, prevede che: “1. Il modello di organizzazione e di gestione idoneo ad avere efficacia esimente della responsabilità amministrativa delle persone giuridiche, delle società e delle associazioni anche prive di personalità giuridica di cui al decreto legislativo 8 giugno 2001, n. 231, deve essere adottato ed efficacemente attuato, assicurando un sistema aziendale per l’adempimento di tutti gli obblighi giuridici relativi: a) al rispetto degli standard tecnico-strutturali di legge relativi a attrezzature, impianti, luoghi di lavoro, agenti chimici, fisici e biologici; b) alle attività di valutazione dei rischi e di predisposizione delle misure di prevenzione e protezione conseguenti; c) alle attività di natura organizzativa, quali emergenze, primo soccorso, gestione degli appalti, riunioni periodiche di sicurezza, consultazioni dei rappresentanti dei lavoratori per la sicurezza; d) alle attività di sorveglianza sanitaria; e) alle attività di informazione e formazione dei lavoratori; f) alle attività di vigilanza con riferimento al rispetto delle procedure e delle istruzioni di lavoro in sicurezza da parte dei lavoratori; g) alla acquisizione di documentazioni e certificazioni obbligatorie di legge; h) alle periodiche verifiche dell’applicazione e dell’efficacia delle procedure adottate. 2. Il modello organizzativo e gestionale di cui al comma 1 deve prevedere idonei sistemi di registrazione dell’avvenuta effettuazione delle attività di cui al comma 1. 3. Il modello organizzativo deve in ogni caso prevedere, per quanto richiesto dalla natura e dimensioni dell’organizzazione e dal tipo di attività svolta, un’articolazione di funzioni che assicuri le competenze tecniche e i poteri necessari per la verifica, valutazione, gestione e controllo del rischio, nonché un sistema disciplinare idoneo a sanzionare il mancato rispetto delle misure indicate nel modello. 4. Il modello organizzativo deve altresì prevedere un idoneo sistema di controllo sull’attuazione del medesimo modello e sul mantenimento nel tempo delle condizioni di idoneità delle misure adottate. Il riesame e l’eventuale modifica del modello organizzativo devono essere adottati, quando siano scoperte violazioni significative delle norme relative alla prevenzione degli infortuni e all’igiene sul lavoro, ovvero in occasione di mutamenti nell’organizzazione e nell’attività in relazione al progresso scientifico e tecnologico.”
Alla luce della chiara formulazione normativa e delle lettere di cui la stessa si compone, la descrizione dei presidi implementati a livello societario nonchè delle “regole speciali di condotta” in tema di salute e sicurezza sul lavoro, dovrà brevemente soffermarsi:
3.2.1. sulla struttura organizzativa aziendale prevista in tema di salute e sicurezza sul lavoro;
3.2.2. sui rapporti con gli appaltatori (Art. 30, comma 1, lett. c) del D.LGS. 81/08);
3.2.3. sull’attività di sorveglianza sanitaria (art. 30, comma 1, lett. d) del D.Lgs. 81/08
3.2.4. sulle attività connesse alla formazione ed informazione dei lavoratori (art. 30, comma 1, lett. e) del D.Lgs. 81/08);
3.2.5. sull attività di gestione della documentazione e certificazione obbligatorie per legge (art. 30, comma 1, lett. g) del D.LGS. 81/08);
3.2.6. sul sistema di controllo sulla salute e sicurezza sul lavoro e, quindi sul sistema integrato di Gestione Qualità (SGQ), sulle procedure operative, sul ruolo dell’organismo di vigilanza in materia di salute e sicurezza sul lavoro e sul raccordo con le funzioni di primo controllo (art. 30, comma 1, lett. f)-h) e comma 4 del D.LGS. 81/08);
3.2.7. sul sistema di registrazione delle attività di cui al comma 1 dell’art. 30 (art. 30, comma 2 del D.Lgs. 81/08);
3.2.8. sull’aggiornamento e riesame (art. 30, comma 4 del D.LGS. 81/08).
3.2.1. La struttura organizzativa aziendale prevista in tema di salute e sicurezza sul lavoro: sulla base dell’articolata organizzazione aziendale, la società ha scelto di assicurare il rispetto della normativa in tema di salute e sicurezza sul lavoro attraverso una struttura composita che, accanto alle figure normativamente previste dal D.Lgs. 81/08, ha altresì previsto il conferimento di deleghe di funzioni ai sensi dell’art. 16 del D.Lgs. 81/08. La giurisprudenza ha infatti da tempo sottolineato che la complessità dei processi gestionali ed operativi all’interno di un’impresa di medie o rilevanti dimensioni impone necessariamente, per essere fronteggiata, l’esistenza di una pluralità di figure che, in virtù di valide deleghe o procure, possano intervenire a garantire un presidio dei rischi legati alla commissione di un reato presupposto. In questo senso, rimandando per il resto all’organigramma allegato al presente Modello di Organizzazione e Gestione – si tratta delle seguenti figure:
- datore di lavoro (rappresentato dall’Amministratore Delegato);
- delegato alla Sicurezza ex art. 16 D.Lgs. 81/08;
- dirigenti per la sicurezza (che possono coincidere con le figure sub b) e c));
- Preposti;
- Responsabile del Servizio di Prevenzione e Protezione;
- Responsabile dei Lavoratori per la Sicurezza;
- Medico competente;
- Squadra di Emergenza e squadra di primo soccorso.
3.2.2. I rapporti con gli appaltatori: fermo restando che la selezione degli appaltatori è specificamente regolata dalle Standard Operative Procedures in tema di fornitori, i contratti stipulati con questi ultimi dovranno necessariamente includere clausole che obbligano l’appaltatore o fornitore al rispetto dei principi contenuti nel Codice Etico adottato da Società Prodotti Antibiotici S.p.A. o dal Modello di Organizzazione, Gestione e Controllo.
Per quanto interessa la presente parte speciale, il quadro della disciplina del rapporto con gli appaltatori è completato dalle previsioni del DUVRI (Documento Unico di Valutazione dei Rischi Interferenziali) che è volto a mappare i rischi da interferenza sul luogo di lavoro, incidendo sull’esecuzione del contratto di appalto. In particolare, in caso di affidamento di lavori con contratto di appalto e d’opera, che non riguardino servizi di natura intellettuali, la mera fornitura di materiali o attrezzature e che non siano non superiori ai due giorni (salvo le condizioni previste dall’art. 26 comma 3 bis del D.Lgs. 81/2008) Società Prodotti Antibiotici S.p.A. procede sempre alla stesura del DUVRI. L’amministratore delegato, il soggetto delegato ai sensi dell’art. 16 D.Lgs. 81/08 e/o i Responsabili e il Responsabile del Servizio di Prevenzione e Protezione possono richiedere ai fornitori e/o appaltatori la possibilità di effettuare audit sia presso le loro sedi sia durante lo svolgimento delle loro attività presso le sedi aziendali.
3.2.3. Il medico competente e l’attività di sorveglianza sanitaria: con riguardo a quanto espressamente previsto dall’art. 30 comma 1, lett. d) del D.Lgs. 81/08 – a norma del quale il Modello deve assicurare che siano adempiuti gli obblighi giuridici con riguardo alle attività di sorveglianza sanitaria – Società Prodotti Antibiotici S.p.A. ha nominato un Medico Competente, responsabile delle attività di cui all’art. 25 del D.Lgs. 81/2008. A titolo esemplificativo e non esaustivo, lo stesso:
- collabora con il datore di lavoro e con il servizio di prevenzione e protezione alla valutazione dei rischi, alla predisposizione dell’attuazione delle misure per la tutela della salute e della integrità psico-fisica, all’attività di formazione e informazione nei confronti dei lavoratori, all’organizzazione del servizio di primo soccorso, alla attuazione e valorizzazione di programmi volontari di “promozione della salute”;
- programma ed effettua la sorveglianza sanitaria di cui all’articolo 41 attraverso protocolli sanitari definiti in funzione dei rischi specifici e tenendo in considerazione gli indirizzi scientifici più avanzati;
- istituisce, aggiorna e custodisce, una cartella sanitaria e di rischio per ogni lavoratore sottoposto a sorveglianza sanitaria, e concorda con il datore di lavoro il luogo di custodia;
- informa ogni lavoratore interessato dei risultati della sorveglianza sanitaria;
- visita gli ambienti di lavoro almeno una volta all’anno o a cadenza diversa che stabilisce in base alla valutazione dei rischi.
3.2.4. la formazione ed informazione dei lavoratori: Società Prodotti Antibiotici S.p.A. promuove un’attività di costante e continua formazione, basata, tra gli altri, anche su training in tema di salute e sicurezza dei lavoratori. In questo senso, il Responsabile della Direzione del Personale – di concerto con il Responsabile del Servizio di Prevenzione e Protezione – definisce la cadenza degli incontri di formazione finalizzati alla sensibilizzazione del personale, potendo avvalersi, laddove necessario, dell’ausilio di professionisti terzi.
Tali corsi sono obbligatori e prevedono la compilazione di un questionario o di un test di valutazione finale che attesti la frequentazione del corso e la piena comprensione dei contenuti illustrati.
3.2.5. L’Attività di gestione della documentazione e delle certificazioni obbligatorie per legge: con riguardo, alla gestione della documentazione e certificazioni, si evidenzia che Società Prodotti Antibiotici S.p.A. svolge un monitoraggio puntuale di tutti i dispositivi, le attrezzature e gli strumenti per accertare la loro conformità rispetto ai requisiti legislativi e certificativi ed ha adottato specifiche procedure per la corretta creazione, approvazione ed archiviazione della documentazione.
3.2.6. Il sistema di controllo sulla SSL: il Manuale della Qualità, le procedure operative, il ruolo dell’Organismo di Vigilanza in materia di salute e sicurezza sul lavoro e il raccordo con le funzioni di primo controllo: come visto, l’art. 30 comma 1, lett. f) e h) stabilisce altresì che il Modello deve assicurare che siano adempiuti gli obblighi giuridici con riguardo “alle attività di vigilanza con riferimento al rispetto delle procedure e delle istruzioni di lavoro in sicurezza da parte dei lavoratori” nonché “alle periodiche verifiche dell’applicazione e dell’efficacia delle procedure adottate. Il comma quarto del medesimo articolo prevede inoltre che “il modello organizzativo deve altresì prevedere un idoneo sistema di controllo sull’attuazione del medesimo modello e sul mantenimento nel tempo delle condizioni di idoneità delle misure adottate”.
Preliminarmente, è opportuno evidenziare che, anche nell’ottica di perseguire il miglioramento continuo in ambito di salute e sicurezza sul lavoro e di minimizzare progressivamente i rischi cui possono essere esposti i dipendenti o i terzi,[3] Società Prodotti Antibiotici SPA, con specifico riguardo alla Divisione BIOSPA, si è dotata di un Sistema di Gestione Integrato Qualità, Salute e Sicurezza e Ambiente (QHSE) conforme alle norme UNI EN ISO 9001:2015 ed ha adottato il relativo Manuale della Qualità. Tale documento – al fine di gestire i processi connessi alla predetta Divisione- si basa sulla metodologia “plan-do-check-act”, adottando l’approccio basato sul rischio di processo e/o di prodotto (risked based thinking) quale strumento di prevenzione e/o mitigazione.[4]
Al di là di tale documento, sono state adottate le seguenti procedure operative specifiche:
- PGN710 “Gestione dei rischi correlati a dispositivi medici”;
- PGN751 “Attività di rilavorazione prodotto”;
- PGN751-2 Norme per l’esecuzione di prove, controlli e collaudi”;
- PGN760 Norme generali per la taratura degli strumenti di prova, misurazione e collaudo”;
- PGN760-2 “Regole di attuazione pratica della conferma metrologica degli strumenti di prova, misurazione e collaudo”;
- PGN824 “Gestione dei risultati non conformi dei test di controllo”.
Tanto premesso, si riportano di seguito tutti gli aspetti generali dei presidi di controllo in tema di salute e sicurezza sul lavoro:
- le responsabilità in materia di salute e sicurezza sul lavoro, con particolare riferimento al Datore di Lavoro, ai Delegati individuati ai sensi e per gli effetti dell’art. 16 del D.Lgs. 81/08, all’RSPP, al RLS, ai dirigenti per la sicurezza, ai preposti devono essere formalmente identificate e documentate, attraverso disposizioni organizzative e deleghe specifiche rilasciate da parte dei soggetti competenti e comunicate ai terzi interessati;
- devono essere tempestivamente identificati e valutati dal Datore di Lavoro i rischi per la salute e sicurezza sul lavoro, ivi compresi quelli riguardanti i lavoratori esposti a rischi particolari. Nell’ambito del processo di identificazione e valutazione dei rischi, deve essere tenuta in adeguata considerazione la struttura aziendale, la natura dell’attività, l’ubicazione dei locali e delle aree di lavoro, l’organizzazione del personale, le specifiche sostanze, le attrezzature e gli impianti impiegati nelle attività. La valutazione dei rischi deve essere documentata attraverso l’elaborazione, ai sensi della normativa prevenzionistica vigente, di un “Documento di Valutazione dei Rischi” che contenga quanto prescritto all’Art. 28 del D.Lgs. 81/08. Il DVR deve avere data certa ed essere approvato dal Datore di Lavoro, dall’RSPP e dal Medico Competente, sentito il RLS;
- Il Datore di Lavoro deve promuovere la cooperazione ed il coordinamento per l’attuazione delle misure di prevenzione e protezione dai rischi sul lavoro incidenti sull’attività lavorativa oggetto delle attività di appalto, elaborando un unico documento per la valutazione dei rischi (come anticipato, “DUVRI”), indicante le misure adottate per eliminare le interferenze ed i rischi sulle forniture;
- occorre osservare rigorosamente tutte le leggi e i regolamenti e procedure in materia di sicurezza sul lavoro e sulla tutela dell’igiene e salute sul lavoro che disciplinano l’accesso, il transito e lo svolgimento delle attività lavorative presso i locali in uso alla Società, con particolare riguardo ai protocolli e/o documenti approvati internamente per prevenire i rischi derivanti dal virus Sars-Covid19;
- vanno forniti adeguati dispositivi di protezione individuali ai propri dipendenti, conformi alle normative vigenti e in funzione delle mansioni da quelli svolte (tra cui i DPI e i materiali igienizzanti previsti dalla normativa approvata per fronteggiare l’attuale situazione di emergenza epidemiologica);
- il Servizio Prevenzione e Protezione, unitamente al Comitato Covid (di cui lo stesso fa parte), propone e diffonde adeguate procedure volte alla tutela della sicurezza sul lavoro e alla tutela dell’igiene e salute sul lavoro nonché le indicazioni sulle adeguate misure di prevenzione e protezione da adottare;
- vengano assicurati adeguati flussi informativi tra i soggetti a vario titolo responsabili della salute e sicurezza dei lavoratori ed il Comitato Covid;
- ai fini della gestione delle emergenze, della prevenzione degli incendi e dell’evacuazione dei lavoratori, nonché per il caso di pericolo grave e immediato, devono essere adottate adeguate misure, che garantiscano:
a) lo svolgimento e la documentazione di periodiche prove di esodo ed evacuazione;
b) la definizione e adozione di adeguate misure per il controllo di situazioni di rischio in caso di emergenza, con particolare riferimento all’elaborazione e periodico aggiornamento, a cura del Servizio di Protezione e Prevenzione, del Piano di sicurezza e di gestione dell’emergenza, testato periodicamente;
c) la predisposizione ed il tempestivo aggiornamento, qualora necessario in relazione a variazioni di rischio (ad esempio in relazione a maggiori carichi di incendio, nuove attività con pericolo di incendio, modifiche strutturali, ecc.), del Documento di Valutazione dei rischi di incendio nei luoghi di lavoro, ai sensi del DM 10 marzo 1998, a cura del Servizio di Protezione e Prevenzione. Il documento deve essere approvato dai relativi Datori di Lavoro ed RSPP e custodito presso l’unità produttiva di riferimento;
d) l’identificazione di una squadra di pronto intervento, costituita da un numero adeguato di dipendenti debitamente formati e con specifico addestramento in materia di antincendio, primo soccorso ed evacuazione;
e) l’impiego di attrezzature, impianti e dispositivi adeguati e la dotazione di adeguate misure di primo soccorso;
f) la programmazione delle verifiche e delle manutenzioni relative alle apparecchiature antincendio e la regolare alimentazione del Registro dell’Antincendio, ai sensi del DPR 37/98;
- deve essere tempestivamente ottenuto e conservato il Certificato di Prevenzione Incendi (CPI), rilasciato dal Comando Provinciale dei Vigili del Fuoco in relazione alle attività svolte e ai materiali gestiti, provvedendo al relativo rinnovo qualora in scadenza;
- deve essere predisposto ed aggiornato, a cura del Medico Competente un Piano Sanitario volto sia ad assicurare l’implementazione delle misure necessarie a garantire la tutela della salute e dell’integrità psico-fisica dei lavoratori, sia a fornire una valutazione della situazione sanitaria esistente presso le sedi, sia a programmare l‘effettuazione delle visite mediche;
- nei trasferimenti interni ed esterni, sia con mezzi propri che aziendali, devono essere osservate tutte le necessarie ed opportune precauzioni in materia di salute e sicurezza sul lavoro;
- ove il personale debba accedere a zone che lo espongano a rischi gravi e specifici, deve essere prevista per esso specifica informazione e formazione in merito ai rischi ed alle relative modalità di gestione;
- deve essere garantita la manutenzione ordinaria e straordinaria dei dispositivi di sicurezza aziendale (ad esempio, porte tagliafuoco, lampade di emergenza, estintori, ecc.) nonchè degli ulteriori strumenti necessari per lo svolgimento delle attività lavorative;
- devono essere richiesti e valutati i costi per la salute e sicurezza sul lavoro in occasione dell’attività di selezione dei fornitori (in particolare degli appaltatori e dei fornitori d’opera). Tale voce di spesa deve essere specificamente indicata nel contratto, e deve essere separata dal costo generale dello stesso
- l’assegnazione, la verifica e la gestione degli appalti o degli incarichi a lavoratori autonomi deve essere effettuata controllando l’idoneità tecnico professionale delle imprese appaltatrici nonché il pieno rispetto della normativa di riferimento, di cui all’articolo 26 del D.Lgs. 81/08 e delle procedure interne di sicurezza.
Quanto al sistema di controllo in materia di sicurezza sul lavoro, lo stesso – come peraltro suggerito dalle Linee Guida e dalle best practices – si articola in un doppio livello di monitoraggio. Il primo livello coinvolge tutti i soggetti che operano nell’ambito della struttura organizzativa della Società, essendo previsto:
- l’auto-controllo da parte dei lavoratori, i quali devono sia utilizzare correttamente i dispositivi e le attrezzature di lavoro, i mezzi di trasporto, nonché i dispositivi di sicurezza e di protezione messi a loro disposizione, sia segnalare immediatamente le deficienze di tali mezzi e dispositivi nonché qualsiasi eventuale condizione di pericolo di cui vengano a conoscenza;
- il coinvolgimento diretto dei soggetti aziendali con specifici compiti in materia di SSL (ad esempio, Datore Di Lavoro, Delegato in materia di salute e sicurezza, RSPP), i quali intervengono, tra l’altro, in materia:
(a) di vigilanza e monitoraggio periodici e sistematici sulla osservanza degli obblighi di legge e delle procedure aziendali in materia di SSL;
(b) di segnalazione al datore di lavoro di eventuali deficienze e problematiche;
(c) di individuazione e valutazione dei fattori aziendali di rischio;
(d) di elaborazione delle misure preventive e protettive attuate e richiamate nel Documento di Valutazione dei Rischi, nonché dei sistemi di controllo di tali misure;
(e) di proposizione dei programmi di formazione e addestramento dei lavoratori, nonché di comunicazione e coinvolgimento degli stessi.
Per valutare l’adeguatezza del sistema di gestione integrato e proporre eventuali azioni correttive e/o preventive, la funzione QA, di concerto con l’RSPP programma annualmente audit interni sia “di processo” che in tema di salute e sicurezza sul lavoro.
Il secondo livello di monitoraggio, richiamato espressamente dalle Linee Guida, è svolto anzitutto dall’Organismo di Vigilanza, che, pur non ricoprendo ruoli operativi:
- vigila sull’adeguatezza e sul rispetto del presente Modello di Organizzazione e Gestione, del Codice Etico e di tutte le procedure aziendali che, direttamente o indirettamente, sono funzionali a garantire inclusi il Codice Etico e le procedure aziendali in materia di salute e sicurezza sul lavoro;
- esamina le segnalazioni concernenti eventuali violazioni del Modello e delle procedure dallo stesso richiamate;
- propone al Consiglio di Amministrazione gli aggiornamenti del Modello di Organizzazione e Gestione, del sistema preventivo adottato dalla Società ovvero delle procedure aziendali vigenti, che dovessero rendessero necessarie o opportune in considerazione di eventuali inadeguatezze riscontrate, ovvero a seguito di significative violazioni o di cambiamenti della struttura organizzativa della Società in relazione al progresso scientifico e tecnologico.
Oltre all’OdV, Società Prodotti Antibiotici S.p.A., in conseguenza dell’attuale situazione di emergenza epidemiologica, ha inoltre istituito internamente un Comitato funzionale a monitorare la corretta attuazione delle misure finalizzate a minimizzare o prevenire i rischi derivanti dalla diffusione del virus Sars-Covid19, cui partecipano il Datore di Lavoro, il delegato ex art. 16 D.Lgs. 81/08, l’RSPP, il Medico competente e l’RLS (di seguito anche “Comitato Covid”).
Al fine di consentire all’Organismo di Vigilanza ed al Comitato di svolgere efficacemente il monitoraggio di secondo livello è previsto un apposito raccordo tra le funzioni della struttura organizzativa e tali organi, attraverso i flussi informativi periodici (e non) meglio descritti nella parte generale del presente Modello di Organizzazione e Gestione.
3.2.7. Il sistema di registrazione delle attività di cui al comma 1 dell’art. 30: con riguardo a tutti i processi sensibili, Società Prodotti Antibiotici S.p.A. ha previsto la predisposizione e l’implementazione di apposita modulistica aziendale per dare evidenza del pieno rispetto di quanto previsto all’interno delle SOP adottate internamente.
La registrazione delle attività di aggiornamento dei DVR, DUVRI e PSC (rilevanti ex art. 30 lett. a) e b) è riscontrabile oltre che direttamente nei documenti (archiviati e tenuti a disposizione degli interessati), anche nella successiva attività di monitoraggio e verifica da parte delle competenti funzioni.
Per quanto concerne l’attività di sorveglianza sanitaria (ex lett. d) dell’art. 30), è lo stesso Medico Competente che procede alla registrazione dell’esecuzione delle attività in questione
Le attività di vigilanza di cui alle lettere f) e h) e al comma 4 dell’art. 30 dovranno essere oggetto di registrazione/archiviazione da parte delle competenti funzioni di controllo sia di primo che di secondo livello (Organismo di Vigilanza).
3.2.8 Aggiornamento e riesame: Il comma 4 dell’art. 30 prevede, infine, che il riesame e l’eventuale modifica del modello organizzativo devono essere adottati, quando siano scoperte violazioni significative delle norme relative alla prevenzione degli infortuni e all’igiene sul lavoro, ovvero in occasione di mutamenti nell’organizzazione e nell’attività in relazione al progresso scientifico e tecnologico”. Sul punto, si rinvia a quanto detto nella parte generale con specifico riferimento all’Organismo di Vigilanza.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Al fine di assicurare la corretta prevenzione di contagi legati alla diffusione del virus Sars-Covid19 in ambienti lavorativi e di minimizzare il conseguente rischio di “infortuni” potenzialmente rilevanti ai sensi dell’art. 25septies, è stata altresì prevista l’istituzione di periodici flussi informativi anche tra il Comitato Covid e l’Organismo di Vigilanza.
Il complesso di tali flussi informativi ha come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Si rimanda sul punto a pag. 29 del Manuale della Qualità.
[2] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
[3] Sul presupposto che “il lavoro e ambiente dell’organizzazione è una combinazione di fattori umani e fisici” che influenzano “la motivazione, la soddisfazione, lo sviluppo e le prestazioni del personale, come pure la qualità dei prodotti e dei servizi” il Manuale della Qualità evidenzia che “sono tenuti sotto controllo i seguenti fattori”:
- “condizioni di salute e sicurezza”;
- “metodi di lavoro”;
- “condizioni dell’ambiente di lavoro”.
Si vedano per il resto le pagg. 19 e 20 del documento sopra richiamato.
[4] Si rimanda in questo senso alla tabella contenuta a pag. 4 del Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 6
Reati contro l’amministrazione della giustizia
(Induzione a non rendere dichiarazioni o a rendere dichiarazioni mendaci all’Autorità Giudiziaria e favoreggiamento personale transnazionale art. 25decies e combinato disposto degli artt. 378 c.p. e artt. 3 e 10 della L. 146/06)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 6.
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO OGGETTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEL REATO DI CUI ALL’ART. 25-DECIES DEL D.LGS. 231/01 E DEL FAVOREGGIAMENTO PERSONALE TRANSNAZIONALE
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA
0.PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione del reato presupposto previsto nell’art. 25decies del D.Lgs. 231/01 (sia in ottica nazionale che internazionale) e del delitto previsto dall’art. 378 c.p. (rilevante esclusivamente in un’ottica transnazionale ai sensi degli artt. 3 e 10 Legge 16 marzo 2006 n. 146),[1] definendo i principi di comportamento che tutti i destinatari del Modello debbono rispettare.
In questo senso, si provvederà:
- a fornire una descrizione sintetica dei reati contemplati dalle predette disposizioni;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione degli stessi.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 6.
La fattispecie indicata nell’art. 25decies – rilevante anche in un’ottica transazionale ai sensi del combinato disposto degli artt. artt. 3 e 10 della L. 146/06 – sanziona la condotta di “chiunque, con violenza o minaccia, o con offerta o promessa di denaro o di altra utilità, induce a non rendere dichiarazioni o a rendere dichiarazioni mendaci la persona chiamata a rendere davanti all’autorità giudiziaria dichiarazioni utilizzabili in un procedimento penale, quando questa ha la facoltà di non rispondere”.
Quanto all’art. 378 c.p. – che rileva esclusivamente in un’ottica transazionale – tale disposizione punisce invece chi aiuta taluno a eludere le investigazioni dell’Autorità (comprese quelle svolte da organi della Corte penale internazionale) o a sottrarsi alle ricerche di questa.
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI OGGETTO DELLA PRESENTE PARTE SPECIALE.
Alla luce delle caratteristiche normative delle predette fattispecie e della struttura della società, i processi aziendali che presentano un astratto rischio di commissione del reato sopra elencato sono i seguenti:
- rapporti con le Autorità Giudiziarie o con le ulteriori autorità e/o uffici preposti all’amministrazione della giustizia (anche appartenenti ad altri stati);
- ricezione ed evasione di richieste documentali da parte di Autorità Giudiziarie nazionali o straniere;
- ispezioni, perquisizioni o accessi dell’Autorità Giudiziaria (nazionale o straniera) o di soggetti dalla stessa incaricati o delegati;
- selezione dei professionisti incaricati dell’assistenza e difesa della società o di un suo dipendente;
- gestione dei contenzioni giudiziali e stragiudiziali in cui la società sia coinvolta a vario titolo (in qualità di persona offesa, indagata, imputata, parte attrice, convenuta etc.) o, sebbene non coinvolta formalmente, abbia comunque un interesse diretto;
- gestione dei contenziosi tra la società ed i propri dipendenti;
- rapporti con dipendenti e/o collaboratori chiamati a rendere dichiarazioni nell’ambito di procedimenti penali, civili, amministrativi, tributari che abbiano ad oggetto condotte e/o eventi direttamente o indirettamente connessi all’attività aziendale.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEL REATO DI CUI ALL’ART. 25-DECIES DEL D.LGS. 231/01 E DEL FAVOREGGIAMENTO PERSONALE TRANSNAZIONALE.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[2]
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, alle specifiche condotte da porre in essere in relazione alle aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, i destinatari del presente Modello di Organizzazione e Gestione, ciascuno per la sua area di attribuzione e competenza, dovranno osservare le seguenti regole di condotta:
- i consulenti e/o i professionisti terzi incaricati della difesa e dell’assistenza della società devono essere scelti tra soggetti dotati della necessaria professionalità e competenza;
- il Responsabile del Personale deve comunicare al CdA (e all’OdV), con periodicità definita, l’elenco dei contenziosi in corso che coinvolgono Società Prodotti Antibiotici S.p.A. o uno dei suoi soci, amministratori, dirigenti o dipendenti per condotte poste in essere nell’esercizio delle mansioni lavorative;
- il dipendente al quale vengano contestati, con atto dell’Autorità Giudiziaria o dell’Autorità Amministrativa, fatti relativi ad attività compiute in ambito aziendale che possano coinvolgere la Società e comportarne una responsabilità amministrativa o civile deve darne immediatamente notizia a Società Prodotti Antibiotici S.p.A.;
- è necessario consegnare tempestivamente la documentazione eventualmente richiesta nel corso di verifiche/ispezioni/perquisizioni o in sede di chiarimenti, assicurandosi che quanto fornito sia integrale e non presenti modifiche, omissioni, tagli o manipolazioni;
- è fatto divieto di fornire, redigere o consegnare all’Autorità Giudiziaria o ai soggetti dalla stessa incaricati dichiarazioni, dati o documenti in genere aventi contenuti inesatti, errati, incompleti, lacunosi e/o falsi;
- occorre assicurare un atteggiamento pienamente collaborativo e trasparente nei confronti dell’Autorità Giudiziaria (nazionale o straniera) procedente, non nascondendo alcuna circostanza di cui si sia a conoscenza in relazione ai fatti oggetto di accertamento e rendendo dichiarazioni veritiere;
- è vietato, anche per il tramite di legali e/o professionisti terzi, formulare raccomandazioni e/o suggerimenti circa il comportamento processuale da adottare al dipendente/collaboratore chiamato a rendere dichiarazioni davanti all’Autorità Giudiziaria;
- è vietato offrire denaro o altre utilità (quali promozioni o benefit aziendali) al dipendente/collaboratore che chiamato a rendere dichiarazioni davanti all’Autorità Giudiziaria;
- non possono essere chieste al dipendente informazioni o notizie sul contenuto delle domande rivoltegli dall’Autorità Giudiziaria o dai Pubblici Ufficiali dalla stessa delegata nel corso di audizioni o testimonianze;
- deve essere identificata una specifica funzione aziendale destinataria di eventuali segnalazioni (di pressioni, minacce, ecc.) da parte del soggetto che è coinvolto in un procedimento o che è stato chiamato a deporre avanti l’Autorità Giudiziaria.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Occorre sul punto ricordare che la responsabilità amministrativa degli Enti dipendente dalla commissione di illeciti penali discende non solo dal Decreto Legislativo 231/01 ma anche dall’art. 10 della L. 146/06, che contempla quali reati presupposto alcune fattispecie di illeciti transnazionali. Ai sensi dell’art. 3 del medesimo provvedimento normativo, “si considera reato transnazionale il reato punito con la pena della reclusione non inferiore nel massimo a quattro anni, qualora sia coinvolto un gruppo criminale organizzato, nonché:
- a) sia commesso in più di uno Stato;
- b) ovvero sia commesso in uno Stato, ma una parte sostanziale della sua preparazione, pianificazione, direzione o controllo avvenga in un altro Stato;
- c) ovvero sia commesso in uno Stato, ma in esso sia implicato un gruppo criminale organizzato impegnato in attività criminali in più di uno Stato;
- d) ovvero sia commesso in uno Stato ma abbia effetti sostanziali in un altro Stato”.
[2] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 7
Reati ambientali (Art. 25undecies)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 7
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25SEPTIES DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA
0.PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti nell’art. 25undecies del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto oggetto della presente parte speciale.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 5.
Tra i numerosi reati presupposto contemplati dall’art. 25undecies del D.Lgs. 231/01, le fattispecie che presentano un astratto rischio di commissione nell’ambito dei processi aziendali di Società Prodotti Antibiotici S.p.A. sono le seguenti:
- scarichi di acque reflue industriali ( D.Lgs. 152/2006 Art. 137);
- attività di gestione di rifiuti non autorizzata (D. Lgs n.152/2006, art. 256);
- inquinamento del suolo, del sottosuolo, delle acque superficiali o delle acque sotterranee (D. Lgs n. 152/2006, art. 257);
- traffico illecito di rifiuti (D. Lgs n.152/2006, art. 259);
- violazione degli obblighi di comunicazione, di tenuta dei registri obbligatori e dei formulari (D. Lgs n.152/2006, art. 258);
- attività organizzate per il traffico illecito di rifiuti (art. 452 quaterdecies c.p.).
Per le restanti fattispecie, si rinvia a quanto evidenziato all’interno dell’appendice normativa allegata al presente Modello di Organizzazione e Gestione.
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Dall’esame della documentazione aziendale e dalle circostanze riferite nel corso delle interviste svolte nell’ambito dell’attività di mappatura del rischio, è emerso che Società Prodotti Antibiotici S.p.A. è dotata di sedi deputate quasi esclusivamente allo svolgimento di attività amministrative, essendo priva di propri stabilimenti produttivi e di magazzini deputati allo stoccaggio/trasmissione dei prodotti destinati all’immissione in commercio: in particolare, le attività di produzione dei farmaci per cui SPA è titolare AIC e/o degli ulteriori prodotti nonchè la gestione del magazzino risultano essere state esternalizzate presso società terze. All’interno della Divisione BIOSPA è presente un laboratorio aziendale che, pur producendo reagenti accessori e materie prima per diagnostici in vitro, si caratterizza tuttavia per una funzionalità molto ridotta e, allo stato, impiega solamente due risorse.
Tali circostanze – com’è ovvio – determinano una rilevante diminuzione dei rischi connessi alla commissione dei reati presupposto di cui all’art. 25undecies, limitando i processi aziendali “sensibili” alle seguenti aree di attività:
- ottenimento, modifica e rinnovo delle autorizzazioni ambientali;
- attività condotte all’interno del laboratorio della Divisione BIOSPA, con particolare riguardo alla produzione di reagenti accessori e/o materie prime per diagnostici in vitro;
- gestione, smaltimento dei rifiuti originati dall’ attività di lavorazione svolta all’interno del laboratorio;
- gestione e smaltimento dei rifiuti prodotti dagli uffici amministrativi presenti presso la sede, con particolare riguardo ai rifiuti organici ed inorganici direttamente o indirettamente connessi alle misure implementate per prevenire o minimizzare il rischio da contagio da Covid-19;
- gestione dei rifiuti generati in occasione di attività di manutenzione/ristrutturazione o in occasione di interventi realizzati presso gli uffici aziendali da parte di società terze cui sia appaltato lo svolgimento di determinate attività;
- rapporti con le società terze che si occupano della logistica e delle attività di magazzino per assicurare la corretta gestione dei medicinali non più vendibili (rifiuti) e conferimento a terzi per trasporto e smaltimento.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25SEPTIES DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[1]
3.2. Le regole di comportamento specifiche.
Quanto alle regole di condotta specificamente concernenti le attività sensibili individuate nel paragrafo 2 della presente parte speciale, giova anzitutto evidenziare che, con riguardo alla Divisione BIOSPA, Società Prodotti Antibiotici S.p.A. si è dotata di un Sistema di Gestione Integrato Qualità, Salute e Sicurezza e Ambiente (QHSE) conforme alle norme UNI EN ISO 9001:2015 ed ha adottato il relativo Manuale della Qualità.
Inoltre, per quanto i rischi connessi alla gestione ambientali siano risibili, SPA ha deciso di conferire un’apposita delega in materia di “prevenzione e tutela ambientale” al fine di soddisfare “in maniera più incisiva nella dimensione e complessità del fenomeno aziendale” (Cass. pen., sez. III, n. 1112 del 26 maggio 2004, ric. Carraturo) la protezione di tali beni. Anche perché, “quando l’azienda ha notevoli dimensioni e si articola in varie branche”, è impossibile che un singolo soggetto “abbia il controllo dell’intera attività produttiva”( Cass. pen., sez. III, n. 8538 del 14 settembre 1993, ric. Robba)
Tanto premesso, i destinatari del presente Modello di Organizzazione e Gestione, ognuno secondo le proprie attribuzioni e competenze, avranno l’obbligo di:
- ottenere, modificare o rinnovare le autorizzazioni ambientali eventualmente richieste, affinché l’attività di smaltimento e/o gestione delle acque reflue e/o delle ulteriori sostanze trattate nell’ambito del laboratorio sia conforme prescrizioni normative vigenti;
- definire i programmi dei campionamenti e delle analisi degli scarichi/emissioni in linea con quanto previsto dalle prescrizioni autorizzative e dalla normativa vigente;
- monitorare i dati riguardanti gli scarichi/emissioni, ivi compresi i certificati analitici e i campionamenti effettuati;
- selezionare l’eventuale fornitore (intermediari/trasportatori /smaltitori) deputato alla gestione ed al corretto smaltimento dei rifiuti secondo criteri che garantiscano l’individuazione di soggetti altamente qualificati e che accertino il possesso delle iscrizioni/comunicazioni/ autorizzazioni previste dalla normativa;
- verificare periodicamente la sussistenza delle necessarie autorizzazioni e/o certificazioni in capo al fornitore;
- garantire che le attività di gestione dei medicinali da avviare a smaltimento siano svolte in conformità ai requisiti normativi e autorizzativi vigenti previsti in capo al produttore di rifiuti;
- non trasportare in conto proprio i rifiuti prodotti in assenza dei requisiti previsti dalla normativa;
- tenere un comportamento corretto, trasparente e collaborativo, nel rispetto delle norme di legge e delle procedure aziendali interne, in tutte le attività inerenti l’uso e la gestione della sicurezza ambientale e della raccolta e smaltimento dei rifiuti;
- sul presupposto che i rifiuti prodotti negli ambienti di lavoro della società sono prevalentemente classificabili come urbani, effettuare la raccolta differenziata di alcune tipologie di rifiuti secondo modalità che variano da Comune a Comune in base agli obblighi disposti dalla normativa vigente a livello nazionale (d.lgs.152/06) e locale (disposizioni Regionali e Comunali):
- informare i dipendenti dell’obbligo di attenersi alle disposizioni vigenti in ordine alle modalità di detta raccolta anche attraverso apposita cartellonistica, informative tramite la Intranet aziendale o raccoglitori allo scopo chiaramente identificati e segnalati;
- analizzare le modalità di miscelazione dei rifiuti nonché delle modalità di raccolta, recupero, smaltimento degli stessi;
- Implementare un sistema volto ad ottenere un controllo rigoroso, a mezzo di verifiche periodiche, della miscelazione dei rifiuti;
- garantire la corretta classificazione e codificazione delle varie tipologie di rifiuti prodotti nonché l’esatta attribuzione delle caratteristiche di pericolo nel rispetto della legislazione vigente e della normativa tecnica di settore;
- favorire la raccolta differenziata dei rifiuti delle apparecchiature elettriche ed elettroniche (RAEE) ed assicurare l’assegnazione della relativa gestione e smaltimento a imprese iscritte all’Albo Nazionale Gestori Ambientali;
- istituire presso la sede un registro di carico e scarico rifiuti che è tenuto ed aggiornato a cura del Delegato in materia di prevenzione e protezione ambientale (con l’ausilio di suoi collaboratori) ed è periodicamente vidimato dalla Camera di Commercio competente per territorio conservato per 5 anni dall’ultima registrazione;
- identificare eventualmente le aree adibite al deposito temporaneo di rifiuti;
- disciplinare le attività di gestione dei rifiuti generati presso gli uffici da parte degli appaltatori a cui sono affidate attività di manutenzione e/o interventi presso le sedi aziendali, affinché le stesse siano svolte in conformità ai requisiti normativi e a quanto previsto dalle clausole contrattuali definite;
- conservare ed archiviare debitamente tutta la documentazione amministrativa relativa alla gestione dei rifiuti, assicurando la tracciabilità delle attività svolte.
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 8
Reati di ricettazione, riciclaggio, impiego di denaro, beni o utilità di provenienza illecita, autoriciclaggio e delitti tributari (artt. 25octies e 25quinquiesdecies)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 8
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 25OCTIES E 25QUINQUIESDECIES DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA
0.PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti negli artt. 25octies e 25quinquiesdecies del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni, rimandando, per una compiuta descrizione delle caratteristiche oggettive e soggettive degli illeciti, all’appendice normativa allegata;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto oggetto della presente parte speciale.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 8.
La scelta di predisporre un’unica parte speciale concernente le fattispecie di reato contemplate negli artt. 25octies e 25quinquiesdecies del D.Lgs. 231/01 deriva dallo stretto legame sostanziale che – al di là delle differenze normative in punto di condotta e di bene giuridico tutelato – intercorre tra i delitti contemplati dalla prima disposizione e quelli oggetto della seconda. Gli stessi, infatti, interessando processi aziendali simili o del tutto coincidenti, sono caratterizzati dalla (frequente) sovrapposizione delle aree di rischio e dei processi sensibili, richiedendo identiche regole di comportamento che valgono a prevenire sia gli uni che gli altri.
Non è d’altronde un caso che, all’epoca dell’introduzione del delitto di autoriciclaggio, una parte della dottrina avesse osservato che “i reati tributari previsti dal d.lgs. 74/2000 rientrano nella categoria dei delitti presupposto di riciclaggio”, evidenziando sin da allora la necessità di adottare un “modello volto a prevenire le irregolarità fiscali e, di conseguenza, anche l’autoriciclaggio, scongiurando cioè il rischio che i proventi derivanti dalla commissione dei reati tributari possano essere autoriciclati nello svolgimento dell’attività economica, imprenditoriale o finanziaria delle società”.[1]
Non a caso, all’interno del “case study” elaborato da Confindustria in occasione della pubblicazione della più recente versione delle “linee guida per la costruzione dei modelli di organizzazione, gestione e controllo”, è stato osservato che l’introduzione dei reati tributari nel novero delle fattispecie presupposto non impone l’adozione di nuovi presidi bensì la semplice “revisione del sistema di procedure e protocolli progettato prima dell’entrata in vigore del DL fiscale, per regolamentare quella serie di attività esposte al rischio di costituire la fonte, in termini di strumentalità, per la realizzazione di alcuni reati già rilevanti ai fini 231. Il riferimento è, a titolo di esempio, ai reati di autoriciclaggio e corruzione, che presuppongono la disposizione di una provvista di denaro strumentale alla commissione della condotta illecita”. Tali attività infatti “vanno ora analizzate non più solo come potenzialmente strumentali alla commissione di “altre” fattispecie di delitto, ma coincidenti con condotte ora divenute rilevanti “in sé”.[2]
Tanto premesso in ordine all’opportunità di adottare un approccio “integrato” ed “unitario” nella gestione dei rischi connessi alle fattispecie di reato oggetto della presente parte speciale, i delitti contemplati negli artt. 25octies e 25quinquiesdecies del D.Lgs. 231/01 sono i seguenti:
- ricettazione (art. 648 c.p.);
- riciclaggio (art. 648-bis c.p.);
- impiego di denaro, beni o utilità di provenienza illecita (art. 648-ter c.p.);
- autoriciclaggio (art. 648-ter.1 c.p.);
- dichiarazione fraudolenta mediante uso di fatture o altri documenti per operazioni inesistenti (art. 2, D.Lgs. 74/2000);
- dichiarazione fraudolenta mediante altri artifici (art. 3, D.Lgs. 74/2000);
- emissione di fatture o altri documenti per operazioni inesistenti (art. 8, D. Lgs. 74/2000);
- occultamento o distruzione di documenti contabili (art. 10, D. Lgs. 74/2000);
- sottrazione fraudolenta al pagamento di imposte (art. 11, D. Lgs. 74/2000);
- dichiarazione infedele (art. 4 D.lgs. 74/2000, che rileva ai fini della responsabilità amministrativa dell’ente solo laddove commessa nell’ambito di sistemi fraudolenti transfrontalieri e al fine di evadere l’IVA per un importo complessivo non inferiore a euro 10.000.000)
- omessa dichiarazione (art. 5 D.lgs. 74/2000, che comporta l’insorgenza di una potenziale responsabilità amministrativa dell’ente nelle ipotesi di cui al precedente articolo) ;
- l’indebita compensazione (art. 10 quater D.lgs. 74/2000, per le quali valgono le considerazioni già espresse in relazione agli artt. 4 e 5)
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Alla luce delle caratteristiche normative delle fattispecie elencate nel precedente paragrafo e della struttura della società, i processi aziendali che presentano un astratto rischio di commissione dei reati sopra elencati sono i seguenti:
- selezione e verifica dei fornitori;
- predisposizione delle condizioni contrattuali di vendita e concessioni di eventuali deroghe e/o sconti;
- rapporti con l’Agenzia delle Entrate o con altre Autorità Pubbliche che svolgano qualsivoglia funzione – diretta o indiretta – connessa alla tutela degli interessi erariali dello Stato;
- flussi informativi con consulenti esterni (società o persone fisiche) incaricati di svolgere attività in ambito tributario o fiscale;
- gestione delle scadenze e/o degli adempimenti fiscali/tributari;
- predisposizione, redazione ed invio delle dichiarazioni fiscali sui redditi o sull’imposta sul valore aggiunto;
- processi di fatturazione attiva e passiva;
- gestione dei pagamenti e dei conti correnti intestati alla società;
- attività di gestione della cassa in contanti istituita presso la Direzione Amministrazione e Finanza;
- archiviazione e conservazione di tutta la documentazione contabile;
- utilizzo di strumenti di pagamento (carte di credito) concesse come benefit aziendali;
- verifica ed eventuale rimborso delle note spese prodotte dai dipendenti.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 25OCTIES E 25QUINQUIESDECIES DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività sensibili menzionate nel precedente paragrafo, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[3]
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, alle specifiche condotte da porre in essere in relazione alle aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, giova evidenziare che Società Prodotti Antibiotici S.p.A. ha adottato due specifiche Standard Operative Procedure aventi ad oggetto la gestione economica e contabile della società, ovvero la SOP AMM.04.01 (concernente la gestione fatturazione dei clienti) e la SOP AMM.03.01 (relativa alla gestione del ciclo passivo). Tali documenti, letti unitamente all’organigramma ed al sistema di procure e/o deleghe di funzioni implementato a livello aziendale, consentono di ricostruire compiutamente i presidi posti in essere a livello di gestione economico/finanziaria. Oltre a tali SOP – che costituiscono un allegato del presente Modello di Organizzazione e Gestione ed alla quale si rimanda integralmente – i processi “sensibili” ricompresi in questa macroarea sono indirettamente disciplinati anche da ulteriori procedure quali:
- AFC_2013_ 1 “note di credito” (in attesa di revisione: abbiamo la SOP revisionata?);
- AMM-IS-01-04 “comodati d’uso, donazioni e atti di liberalità”;
- AMM.IS.02.02. “trasparenza dei trasferimenti di valore”;
- MKT/RIS/01.05 “consulenze scientifiche e borse di studio”.
Anche in considerazione di quanto previsto da tali SOP, i destinatari del presente Modello di Organizzazione e Gestione, ciascuno per la propria area di attribuzione e competenza, dovranno:
(a) con riguardo ai rapporti con i fornitori, agli ordini di acquisto ed alla gestione del magazzino (per quanto affidato ad una società terza):
- per quanto possibile e ragionevole, svolgere un’attività di rigorosa selezione dei fornitori, verificando che gli stessi siano in possesso dei requisiti minimi richiesti per la tipologia di fornitura;
- prevedere periodiche attività ispettive e/o audit esterni per verificare in capo a determinati fornitori (materie prime, principi attivi, prodotti finiti etc.) la sussistenza dei requisiti di legge o delle certificazioni eventualmente richieste;
- inserire i fornitori autorizzati in un apposito elenco, oggetto di periodico aggiornamento ad opera delle funzioni competenti e comunicare in modo tempestivo eventuali modifiche dell’elenco dei fornitori;
- definire i criteri di acquisto in modo chiaro e trasparente, anche attraverso la predisposizione di un piano di acquisti annuale;
- condurre un’adeguata attività selettiva fra diversi offerenti ed effettuare una scelta basata su un’obiettiva comparazione delle offerte/preventivi e coerente con i criteri di acquisto preventivamente individuati nonché con il budget a disposizione;
- definire i criteri e le relative modalità di valutazione della congruità del valore economico dell’offerta anche rispetto ai costi del lavoro e della sicurezza prospettabili con riferimento alle prestazioni oggetto del contratto e, qualora questa appaia anormalmente bassa, chiedere giustificazioni scritte o la produzione di documentazione a corredo;
- assicurare che la corrispondenza intercorsa da/verso i soggetti terzi con cui SPA intrattiene un rapporto commerciale sia sempre documentata o documentabile;
- per quanto possibile e ragionevole, utilizzare listini prezzi e/o di ulteriore documentazione contrattuale che predefinisca il valore della merce o del servizio acquistato;
- verificare, prima dell’emissione dell’ordine formale di acquisto, che le richieste di acquisto (RdA) o i c.d. “buoni fabbisogno” (BF), rispondano ad un’effettiva esigenza di SPA, siano caratterizzati da un prezzo congruo nonchè coerenti con i buget stabiliti per centri di costo;
- assicurare che l’ordine di acquisto venga approvato da parte delle figure aziendali dotate dei necessari poteri, conformemente allo carica rivestita o ad eventuali deleghe e/o procure conferite;
- prevedere che l’acquisto di beni e/o servizi in deroga a quanto stabilito con riguardo alle richieste di acquisto (o BF), alle verifiche da porre in essere ed all’emissione dei relativi ordini sia limitato ad ipotesi specificamente individuate all’interno della normativa aziendale (ad es. acquisti di beni o servizi nell’ambito di contratti di fornitura o, ancora, fatture allegate alle note spese degli Informatori Scientifici del Farmaco e degli Area Manager);
- prevedere dei controlli sulla corretta valorizzazione, completezza ed accuratezza degli ordini di acquisto;
- verificare la corrispondenza tra il bene/servizio ricevuto e quanto previsto nell’ordine di acquisto prima di autorizzare il pagamento della prestazione;
- garantire la conservazione e la corretta archiviazione di tutta la documentazione (proposte, preventivi, contratti) legata all’acquisto di beni o servizi da parte di Società Prodotti Antibiotici S.p.A.;
- inserire nei contratti con i con i fornitori un’apposita clausola che regoli le conseguenze della commissione (o tentativo di commissione) da parte degli stessi dei reati di cui al D. Lgs. 231/2001 (es. clausole risolutive espresse o penali);
- assicurare la periodica inventariazione e riconciliazione al fine di assicurare che la giacenza fisica all’interno dei magazzini fisici coincida con la giacenza indicata a sistema;
- non ricevere, detenere e commercializzare beni dei quali sia incerta l’origine/provenienza o che provengano da fornitori non iscritti nell’apposito elenco tenuto presso la società;
- assicurare che ogni movimentazione di magazzino sia adeguatamente riflessa all’interno del bilancio di Società Prodotti Antibiotici S.p.A.
(b) con riguardo alla ricezione degli ordini, alla predisposizione delle condizioni contrattuali di vendita ed alla concessione di eventuali deroghe e/o sconti:
- improntare i rapporti con i clienti e con i partner commerciali alla massima correttezza e trasparenza, garantendo la piena tracciabilità e documentabilità delle comunicazioni o dei rapporti intercorsi con gli stessi;
- rispettare la catena decisionale ed autorizzativa legata alla predisposizione dell’offerta e/o proposta commerciale, all’invio della stessa al cliente ed alla concessione di eventuali forme di scontistica;
- non concedere sconti o condizioni contrattuali agevolate che non rientrino nei poteri/facoltà conferite in virtù dello specifico ruolo rivestito a livello aziendale o attraverso apposita procura;
- garantire la formalizzazione e l’invio dell’offerta contenente i prezzi e gli sconti eventualmente applicati, provvedendo ad archiviare tutta la documentazione prodotta nel corso dell’attività di gestione commerciale;
- favorire – sia con riguardo ai clienti privati che agli enti pubblici, l’utilizzo di piattaforme o portali digitali finalizzati a facilitare il processo di gestione degli ordini e/o la digitalizzazione dei documenti direttamente o indirettamente collegati al ciclo dell’ordine;
- coinvolgere, ove necessario, le competenti funzioni fiscali aziendali o i consulenti esterni, sia in fase di definizione contrattuale, sia in fase di esecuzione, al fine di garantire che le operazioni siano svolte in conformità alla normativa fiscale di riferimento;
- assicurare il monitoraggio periodico circa la corretta esecuzione dei contratti e attestazione circa la corretta esecuzione delle prestazioni rispetto ai requisiti e ai termini definiti negli ordini/contratti di vendita.
(c) con riguardo alla gestione economica, contabile e finanziaria della società:
- individuare ex ante le risorse destinate a determinate attività (c.d. “centri di costo”) attraverso una specifica delibera del CdA o attraverso una decisione dell’Amministratore Delegato che istituisca un apposito budget, prevedendo adeguate autorizzazioni in caso di superamento del budget previamente stabilito;
- stabilire un sistema di procure per i pagamenti fondato sulla definizione di soglie quantitative di spesa coerenti con le competenze gestionali e con le responsabilità organizzative, provvedendone a darne adeguata pubblicità, in primis attraverso il Registro delle Imprese;
- garantire, anche per il tramite di flussi informativi, il costante allineamento fra poteri, procure e deleghe operative e profili autorizzativi nonché il rispetto dei livelli autorizzativi sia per la richiesta di pagamento che per la disposizione;
- distinguere i soggetti che operano nelle fasi di richiesta della disposizione di pagamento, di effettuazione del pagamento e di controllo/riconciliazioni dell’operazione effettuata;
- assicurare che tutte le operazioni che comportano l’utilizzazione o l’impiego di risorse economiche o finanziarie abbiano una causale espressa e siano giustificate dalla produzione di idonea documentazione, stabilendo, a titolo esemplificativo, che agli ordini di bonifico siano allegate le fatture di riferimento ed eventuale ulteriore documentazione;
- regolamentare in modo specifico i casi in cui i pagamenti possono essere disposti e realizzati prima della ricezione del bene e/o del servizio e prima dell’emissione della fattura, richiedendo (quantomeno) la produzione di documentazione attestante il preventivo o l’offerta cui il pagamento è collegato;
- adottare gestionali e/o piattaforme che da un lato assicurino l’automatica creazione di fatture attive a fronte dell’inserimento della documentazione concernente l’operazione effettuata nonché di scaricare o ricevere le fatture passive emesse dai fornitori, e che dall’altro siano idonei ad interfacciarsi e/o rapportarsi con i portali predisposti dall’Agenzia delle Entrate;
- prevedere, prima di procedere all’invio al Sistema di Interscambio delle fatture attive in formato XML, controlli sui documenti fiscali provvisori creati a partire dalla documentazione inserita a gestionale;
- garantire che l’emissione e la conservazione delle fatture attive e passive sia conforme a quanto previsto dalla normativa in tema di fatturazione elettronica, essendo fondata sull’utilizzo di idonei programmi telematici abilitati ad interfacciarsi con l’Agenzia delle Entrate;
- monitorare il sistema di trasmissione ed interscambio, accertando la sussistenza di eventuali rifiuti circa la documentazione caricata ed adottando tempestivamente le opportune azioni correttive;
- rifiutare ogni documento fiscale che non sia dotato di adeguata giustificazione e che non corrisponda ad alcuna prestazione resa e/o ricevuta di Società Prodotti Antibiotici S.p.A.;
- verificare la coerenza tra il soggetto che ha erogato la prestazione (bene / lavoro / servizio), il soggetto indicato nell’ordine/ contratto ed il soggetto che ha emesso la fattura;
- assicurare, anche attraverso società terze, la registrazione di qualsivoglia dato e documento a rilevanza contabile (ad es. fatture, note di credito, note di debito, pagamenti, incassi, etc.), assicurandone la corretta archiviazione e conservazione;
- garantire che l’inserimento, l’elaborazione e la trasmissione dei dati contabili avvenga mediante sistemi informatici che consentano di tracciare i singoli passaggi e di identificare i soggetti che inseriscono e ricevono i dati;
- eseguire controlli in sede di apertura/modifica di anagrafica fornitori/clienti a sistema al fine di assicurare che vi sia sempre piena corrispondenza tra il nome del fornitore/cliente e l’intestazione del conto su cui far pervenire/da cui accettare il pagamento;
- non realizzare pagamenti a soggetti diversi dalla controparte contrattuale, salvo i casi di cessione del credito o gli ulteriori casi espressamente previsti dalla legge;
- vietare l’accettazione/ricezione di pagamenti su conti cifrati;
- effettuare tutti i pagamenti e/o trasferimenti di valore attraverso strumenti di pagamento che assicurino la piena tracciabilità e documentabilità dell’operazione;
- non effettuare pagamenti in contanti se non conformità ai limite di legge e nel pieno rispetto delle procedure adottate a livello interno;
- verificare la completezza, accuratezza e validità delle registrazioni dei pagamenti e delle operazioni di tesoreria, nonché della documentazione da trasmettere agli istituti bancari, sottoscritta dai procuratori competenti;
- controllare le (i) partite sospese a chiusura dei conti transitori(ii) anomalie nei pagamenti (come, ad esempio, nel caso di coordinate bancarie riconducibili a più fornitori, o di disallineamento tra la sede legale della controparte e la sede della banca di appoggio);
- analizzare l’andamento dei saldi contabili rispetto ai dati storici, al fine di individuare eventuali situazioni anomale e successiva analisi degli scostamenti significativi (in termini assoluti e relativi);
- predisporre una periodica riconciliazione bancaria per tutti i conti correnti attivi, prevendo che le riconciliazioni siano riviste e firmate per approvazione dal Responsabile della Direzione Finanza e Controllo;
- verificare in modo puntuale i presupposti per l’emissione di note di credito, anche laddove le stesse rappresentino una particolare forma di scontistica concordata in relazione al raggiungimento di determinate soglie di fatturato;
- individuare l’importo complessivo massimo che delle casse in contanti eventualmente istituite presso le Direzioni/Divisioni aziendali, garantendo che le stesse siano utilizzate per realizzare pagamenti di importo minimo e che, in ogni caso, sia garantita la piena tracciabilità e rendicontazione delle operazioni compiute utilizzando le somme contenute all’interno di queste casse;
- effettuare una riconciliazione periodica delle giacenze della piccola cassa con le risultanze contabili;
- stabilire che il rimborso delle spese sostenute dai dipendenti possa avvenire solo a fronte della produzione di idonea documentazione comprovante l’operazione di cui si chiede il rimborso;
- prevedere che la documentazione concernente i rimborsi e le note spese debba essere valutata dalle competenti funzioni aziendali al fine di verificare la congruità e l’idoneità degli importi di cui si chiede la corresponsione, oltre che il rispetto della normativa applicabile e dei principi deontologici stabiliti da Farmindustria;
- prevedere che il rimborso a favore dei dipendenti avvenga tramite strumenti tracciabili ed in modo trasparente, vietando di effettuare operazioni su conti cifrati o in contanti e/o a soggetti diversi dal personale che ha diritto ad ottenere il rimborso stesso.
- conferire un incarico consulenziale o attribuire una borsa di studio solo a fronte di e controlli funzionali a verificare: (a) la competenza e professionalità del soggetto che riceve l’incarico o la borsa di studio; (b) che l’importo risponda a criteri di economicità e sia coerente con i valori di mercato; (c) che l’attività oggetto di incarico o della borsa di studio sia effettivamente posta in essere e possa essere documentata;
- ammettere le donazioni solamente a fronte: (a) di una preliminare verifica circa l’ammissibilità della stessa e l’affidabilità dell’ente/struttura richiedente; (b) lo stringente rispetto della catena decisionale ed autorizzativa indicata nella SOP adottata a livello interno e la piena tracciabilità delle decisioni; (c) l’utilizzo di modulistica standard da cui si evinca in modo chiaro l’importo oggetto di donazione e/o erogazione (d) la conservazione e l’archiviazione della documentazione concernente le erogazioni ed i pagamenti effettuati.
- realizzare i trasferimenti di valore connessi agli eventi e/o congressi sponsorizzati o organizzati da SPA rispettando le procedure interne e i principi del Codice Deontologico di Farmindustria, garantendo la non ripetitività degli inviti e la piena trasparenza degli stessi (aspetto sul quale si rimanda integralmente alla parte speciale n. 1);
- assicurare la piena trasparenza a tutti i trasferimenti di valore, provvedendo alla pubblicazione, sul sito aziendale o attraverso altre modalità, di uno specifico report avente ad oggetto tutte le predette operazioni;
- non alienare simulatamente o compiere altri atti fraudolenti sui propri o altrui beni al fine di sottrarsi al pagamento delle imposte;
- prevedere modalità di verifica circa la congruenza tra i bonifici effettuati al personale ed i cedolini;
- definire le modalità per la corresponsione degli incentivi in maniera proporzionale al grado di raggiungimento degli obiettivi, verificando la corrispondenza tra gli incentivi erogati rispetto alle performance rendicontate.
(d) con riguardo alla redazione del bilancio ed alle dichiarazioni e/o agli ulteriori adempimenti fiscali:
- conservare ed archiviare i registri, libri obbligatori, fatture, contratti e altri documenti a supporto in maniera idonea e per periodi non inferiori a quelli previsti dalla legge e in modo da rendere possibile ai terzi una puntuale ricostruzione dei redditi / volumi di affari;
- adottare modalità di archiviazione che, per quanto possibile e ragionevole, ne impediscano la distruzione, alterazione, modifica o occultamento o che, in ogni caso, assicurino la tracciabilità delle operazioni compiute e l’identificazione del soggetto che è intervenuto sui dati o sulle informazioni contabili;
- individuare in modo chiaro i soggetti autorizzati a sottoscrivere il bilancio e/o le dichiarazioni fiscali nonché i soggetti cui è demandato il compito di verificare la correttezza del calcolo delle imposte e dei contributi dovuti;
- selezionare gli eventuali professionisti terzi cui è affidata la redazione del bilancio, delle dichiarazioni fiscali e dei documenti connessi (nota integrativa, prospetti di bilancio etc.) tra soggetti dotati della necessaria professionalità e competenza;
- conferire per iscritto gli incarichi aventi ad oggetto la cura degli interessi economici e finanziari della Società, con l’indicazione dei contenuti e delle condizioni economiche pattuite;
- assicurare che le società di consulenza e/o i professionisti terzi eventualmente coinvolti nella predisposizione di dichiarazioni fiscali e del bilancio abbiano a disposizione tutta la documentazione, le informazioni ed i dati necessari per svolgere in modo adeguato i compiti loro attribuiti;
- garantire che la redazione ed approvazione del bilancio avvenga attraverso il coinvolgimento delle Direzioni e/o Divisioni aziendali che intervengono nelle attività di gestione ed archiviazione della contabilità attiva e passiva, prevedendo una pluralità di livelli di controllo e di verifica (sia a livello locale che a livello regionale);
- assicurare l’applicazione dei principi di redazione del bilancio contenuti nel codice civile nonché dei principi contabili internazionali, garantendo la corretta contabilizzazione, delle donazioni, delle borse di studio e degli ulteriori trasferimenti di valore nonchè verificando in modo rigoroso la deducibilità/detraibilità delle stesse nell’ambito delle attività di predisposizione del bilancio o della dichiarazioni fiscali;
- verificare che vengano definite le modalità di gestione di eventuali scritture di rettifica/integrazione/assestamento e del calcolo alla base della determinazione del valore delle stesse;
- trasmettere al CdA un documento contenente dati relativi al progetto di bilancio prima della relativa riunione del CdA stesso;
- adottare gestionali o programmi che consentano di programmare e scadenzare gli adempimenti fiscali e tributari;
- non perseguire finalità di evasione di imposte sui redditi o sul valore aggiunto, o di altre imposte in generale, né nell’interesse o vantaggio della Società né nell’interesse o vantaggio di terzi;
- verificare che, nelle dichiarazioni concernenti le imposte sui redditi o sul valore aggiunto non vengano inseriti elementi passivi fittizi, elementi attivi per un ammontare inferiore a quello effettivo o crediti/ritenute fittizi;
- definire le modalità di autorizzazione (i) del contenuto dei Modelli dichiarativi e di versamento, (ii) dell’invio degli stessi all’Amministrazione finanziaria e (iii) al pagamento delle imposte;
- implementare controlli volti a verificare la tempestiva e corretta liquidazione delle imposte (o delle cartelle esattoriali) rispetto alle scadenze di legge e a quanto riportato nelle dichiarazioni presentate, tenendo conto sia dei versamenti in acconto già effettuati che degli acconti dovuti per l’esercizio in corso;
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Ciò, sebbene le Linee Guida di Confindustria – al fine di evitare un eccessivo ed un non arginabile ampliamento delle ipotesi di responsabilità da reato delle società – avessero suggerito che “il novero dei reati presupposto del delitto di autoriciclaggio” avrebbe dovuto essere “riferito ai soli delitti che già di per sé considerati fondano ai sensi degli artt. 24 ss. d.lg. n. 231 del 2001, la responsabilità da reato della persona giuridica”
[2] Si rimanda alle pagg. 130-131 del documento denominato “Case Study” allegato alla Linee Guida per la costruzione dei modelli di organizzazione, gestione e controllo pubblicate da Confindustria nel giugno del 2021.
[3] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
PARTE SPECIALE N. 9
L’impiego di cittadini di paesi terzi il cui soggiorno è irregolare, l’Intermediazione illecita e sfruttamento del lavoro ed i reati di razzismo e xenofobia (artt. 25quinques, duodecies e terdecies D.Lgs. 231/01)
SOMMARIO:
0.PREMESSA
1.I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 9
2.LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE
3.LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI ALL’ART. 25QUINQUIES, DUOCDECIES E DELL’ART. 25TERDECIES DEL D.LGS. 231/01
3.1. I principi e gli standard di controllo generali
3.2. Le regole di comportamento specifiche
4.I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
0.PREMESSA.
La presente parte speciale, anche utilizzando i risultati dell’attività di risk assesment compiuta prima dell’adozione del presente Modello di Organizzazione e Gestione, ha la finalità di identificare le aree aziendali che presentano un maggiore rischio di commissione dei reati presupposto previsti negli artt. 25quinquies (sebbene con esclusivo riguardo alla fattispecie di cui all’art. 603bis c.p.), duodecies e terdecies del D.Lgs. 231/01, definendo i principi di comportamento che tutti i destinatari del Modello (ciascuno per gli aspetti di propria competenza) debbono rispettare.
In questo senso, si provvederà:
- a fornire un’elencazione sintetica delle fattispecie di reato contemplate dalle predette disposizioni;
- a riepilogare le aree di attività aziendali maggiormente sensibili alla commissione di tali delitti ed a descrivere le regole di comportamento finalizzate a prevenire o minimizzare il pericolo di commissione dei reati presupposto di cui agli artt. 25quinquies, 25duodecies e 25terdecies.
- I REATI PRESUPPOSTO OGGETTO DELLA PARTE SPECIALE N. 9.
Iniziando dall’art. 25quinquies, l’unica fattispecie astrattamente configurabile nell’ambito delle attività aziendali è quella di “intermediazione illecita e sfruttamento del lavoro”, che sanziona chiunque recluta, utilizza o assume manodopera:
(1) “allo scopo di destinarla al lavoro presso terzi in condizioni di sfruttamento, approfittando dello stato di bisogno dei lavoratori”;
(2) “sottoponendo i lavoratori a condizioni di sfruttamento ed approfittando del loro stato di bisogno”.[1]
Quanto all’art. 25duodecies, tale disposizione contempla anzitutto il delitto di cui all’articolo 22 comma 12-bis, del decreto legislativo 25 luglio 1998, n. 286 (di seguito anche T.U. immigrazione), a norma del quale è sanzionato il datore di lavoro che occupa alle proprie dipendenze lavoratori stranieri privi di permessi di soggiorno, ovvero il cui permesso sia scaduto – e per il quale non si sia richiesto il rinnovo – qualora alternativamente:
- i lavoratori occupati siano in numero superiore a tre;
- i lavoratori occupati sono minori in età non lavorativa;
- i lavoratori occupati siano sottoposti a condizioni lavorative di particolare sfruttamento (di cui al terzo comma dell’articolo 603-bis del codice penale, vale a dire, aver commesso il fatto esponendo i lavoratori a situazioni di grave pericolo avuto riguardo alle caratteristiche delle prestazioni da svolgere e delle condizioni di lavoro).
A seguito delle modifiche introdotte attraverso la L. 161/2017 l’art. 25duodecies è stato esteso anche alle fattispecie previste all’art. 12, commi 3, 3-bis, 3-ter e 5 del d.lgs. 286/1998 (Testo unico sull’immigrazione). Per quanto tali reati siano di difficile (se non proprio impossibile) commissione nell’ambito dell’attività aziendale di Società Prodotti Antibiotici S.p.A. ai fini della responsabilità amministrativa degli enti rilevano pertanto anche i delitti di immigrazione clandestina, commessi da chi promuove, dirige, organizza finanzia o effettua il trasporto di stranieri nel territorio dello Stato, nel caso in cui:
- il fatto riguarda l’ingresso o la permanenza di cinque o più persone;
- la persona trasportata è stata esposta a pericolo per la vita;
- la persona trasportata è stata sottoposta a trattamento inumano;
- il fatto è commesso da tre o più persone in concorso,
- gli autori del fatto hanno disponibilità di armi;
- al fine di trarre un ingiusto profitto dalla condizione di illegalità dello straniero favorisce la permanenza di questi nel territorio dello Stato.
Per quanto concerne l’art. 25terdecies, lo stesso ha invece ad oggetto il reato previsto e punito dall’art. 604bis c.p., che sanziona le condotte di partecipazione ad organizzazioni, associazioni, movimenti o gruppi aventi tra i propri scopi l’incitamento alla discriminazione o alla violenza per motivi razziali, etnici, nazionali o religiosi, nonché la propaganda ovvero l’istigazione e l’incitamento, fondati in tutto o in parte sulla negazione, sulla minimizzazione in modo grave o sull’apologia della Shoah o dei crimini di genocidio, dei crimini contro l’umanità e dei crimini di guerra, purchè dal fatto derivi un concreto pericolo di diffusione
- LE AREE DI ATTIVITA’ A RISCHIO DI COMMISSIONE DEI REATI PRESUPPOSTO DELLA PRESENTE PARTE SPECIALE.
Alla luce della struttura della società e delle caratteristiche normative delle fattispecie di cui agli artt. 604bis c.p. e 22, comma 12bis del T.U. Immigrazione (unico illecito che, come detto, che presenta un astratto rischio di commissione tra quelli previsti dall’art. 25duodecies del D.Lgs. 231/01), i processi aziendali sensibili di SPA sono i seguenti:
- attività di selezione e assunzione di dipendenti, collaboratori interni e consulenti esterni;
- gestione del personale dipendente, con particolare riguardo alle condizioni di lavoro ed ai diritti contrattualmente stabiliti a favore degli stessi;
- adempimento di tutti gli obblighi in tema di salute e sicurezza dei lavoratori;
- rapporti con i fornitori.
- LE REGOLE DI COMPORTAMENTO GENERALI E SPECIFICHE DA ADOTTARE AL FINE DI PREVENIRE O MINIMIZZARE IL RISCHIO DI COMMISSIONE DEI REATI DI CUI AGLI ARTT. 25DUODECIES DEL D.LGS. 231/01.
Al fine di prevenire o minimizzare i rischi connessi allo svolgimento delle attività che presentano un astratto rischio di commissione dei reati presupposto oggetto della presente parte speciale, Società Prodotti Antibiotici S.p.A. ha predisposto un sistema di controlli e presidi fondato da un lato sull’individuazione di principi generali e trasversali (che, in quanto tali debbono ritenersi applicabili a tutte i processi aziendali) e dall’altro su specifiche regole di comportamento.
3.1. I principi e gli standard di controllo generali.
Con riguardo ai primi – e rimandando per il resto alla parte generale del presente Modello di Organizzazione e Gestione – tutte le attività aziendali debbono fondarsi su standard specifici di controllo e su principi che, almeno in parte, risultano dalle seguenti Standard Operative Procedures:
- QA.00.02, riguardante la redazione e gestione delle Procedure Operative Standard;
- PGN422, concernente la verifica sull’idoneità ed efficacia dal Manuale della Qualità adottato dalla Divisione BIOSPA;
- QA.IS.01.03 e PGN423, relativa alla gestione dei documenti ed alla tenuta sotto controllo degli stessi;
- PGN424, concernente la tenuta sotto controllo delle registrazioni;
- QA.SQ.12.02, PGN830 e PGN852, aventi ad oggetto la gestione di non conformità e le azioni correttive/azioni preventive;
- QA.SQ.16.04 e PGN822, relative alle verifiche ispettive interne ed agli audit da svolgere all’interno della Divisione BIOSPA;
- QA.IS.17.03 e PG93, concernenti i “Riesami di Direzione”;
- QA.SQ.10.01, avente ad oggetto la gestione dei cambiamenti (change control);
Anche in ottemperanza a quanto previsto da tali documenti e dal Manuale della Qualità sopra richiamato (come detto, adottato solo con riguardo alla Divisione BIOSPA), occorre pertanto garantire:
- la segregazione delle attività e sulla separazione delle funzioni, così che l’autorizzazione di un’azione o di un atto venga accordata da soggetto diverso da quello che compie l’azione o l’atto. La necessità che il controllo interno sul compimento dell’azione o dell’atto sia esercitato da soggetto diverso da colui che propone o che realizza la condotta risponde alla finalità di evitare che un dipendente possa gestire in autonomia l’intero svolgimento di un processo;
- la stringente proceduralizzazione dei processi, per cui, in relazione alle principali attività sensibili, devono esistere disposizioni e procedure formalizzate idonee ad indicare i principi di comportamento da adottare nonché, ad esempio, le modalità di conservazione ed archiviazione della documentazione rilevante;
- il rispetto dei poteri autorizzativi e di firma, che debbono (a) essere chiaramente definiti e conosciuti all’interno della società, risultando dallo Statuto o dalle procure/deleghe eventualmente conferite, cui deve essere data idonea ed adeguata pubblicità; (b) coerenti con la funzione ed il ruolo rivestito dal soggetto cui sono attribuiti; (c) fondati sulla chiara identificazione di soglie di approvazione di spese, (d) oggetto di flussi informativi aziendali, al fine di assicurare una quanto più tempestiva comunicazione dei poteri e dei relativi cambiamenti.
- la documentabilità, archiviazione e tracciabilità, per quanto possibile e ragionevole, di tutte le operazioni poste in essere nell’ambito di attività sensibili, in modo da garantire che il processo di decisione, autorizzazione e svolgimento sia verificabile e ricostruibile ex post attraverso adeguati supporti telematici e documentali;
- lo svolgimento di controlli e verifiche interne, che, come precisato nella Parte Generale del presente documento, possono essere periodiche o legate ad un evento specifico;
- l’individuazione e tempestiva correzione delle non conformità e sull’adozione di azioni correttive e preventive volte ad eliminare in via definitiva le cause dell’anomalia riscontrata e/o a prevenire il suo verificarsi;
- la formazione dei dipendenti, così da garantire che gli stessi siano “sensibilizzati circa l’importanza della propria attività (…) nel rispetto della politica, consapevoli delle implicazioni derivanti dal non essere conformi ai requisiti del sistema di gestione”.[2
3.2. Le regole di comportamento specifiche.
Con riguardo, invece, alle specifiche condotte da porre in essere in relazione alle aree di attività sensibili elencate nel paragrafo 2 della presente parte speciale, occorre anzitutto evidenziare che Società Prodotti Antibiotici SPA ha adottato un Codice Etico che, al fine di tutelare i propri dipendenti e/o collaboratori, stabilisce che:
- la società “si impegna altresì a rimuovere ogni ostacolo all’attuazione di questi diritti, in modo da garantire il rispetto dell’inviolabilità della persona umana, e da tutelare tutti coloro che operano all’interno di Società Prodotti Antibiotici S.p.A. da qualsiasi atto o comportamento che produca effetto pregiudizievole nei rapporti interpersonali e che discrimini, anche in via indiretta, in ragione di sesso, età, razza, lingua, religione, opinioni politiche e sindacali o condizioni personali e sociali”;
- i responsabili delle Direzioni e delle Divisioni aziendali hanno il dovere di prevenire il verificarsi di discriminazioni e di ogni atto lesivo della dignità della persona, intervenendo tempestivamente qualora vengano riscontrate condotte contrarie ai detti principi.
Tanto premesso, i destinatari del presente Modello di Organizzazione e Gestione, ciascuno per la propria area di attribuzione e competenza, dovranno:
- verificare al momento dell’assunzione e in corso di svolgimento del rapporto di lavoro che eventuali soggetti provenienti da paesi terzi siano in regola con la documentazione necessaria a regolarizzarne il soggiorno. Nello specifico occorrerà:
(a) controllare ed archiviare al momento dell’assunzione copia del permesso di soggiorno del soggetto candidato, qualora già in suo possesso;
(b) accertare, durante lo svolgimento di tutto il rapporto contrattuale, del fatto che eventuali controparti provenienti da paesi terzi siano in regola con il permesso di soggiorno e, in caso di scadenza dello stesso, abbiano provveduto a rinnovarlo.
- accertarsi che apposite agenzie, incaricate di fornire figure di lavoratori interinali, assicurino le garanzie necessarie ad evitare situazioni di potenziali violazioni delle norme in esame per i cittadini stranieri;
- assicurarsi con apposite clausole contrattuali che eventuali soggetti terzi (es. fornitori, società esterne che rendono disponibile personale stabilmente utilizzato presso le sedi delle Società del Gruppo, outsourcer di funzioni operative importanti …) si avvalgano di lavoratori in regola con la normativa in esame e che gli stessi non svolgano od abbiano svolto attività legate l’incitamento alla discriminazione o alla violenza per motivi razziali, etnici, nazionali o religiosi;
- eseguire verifiche sugli appaltatori in caso di appalti di lavori (es. manutenzione impianti), relative al personale impiegato dall’appaltatore e definire in modo puntuale le responsabilità e le modalità di effettuazione delle verifiche;
- garantire che i dipendenti godano di tutti i diritti previsti in tema di orario di lavoro, periodi di riposo, riposo settimanale, aspettativa obbligatoria e ferie;
- assicurare una retribuzione congrua con quanto stabilito dai contratti individuali e collettivi nonché coerente con la quantità e la qualità del lavoro prestato;
- implementare tutte le misure necessarie a tutelare la salute e la sicurezza dei lavoratori (aspetto sul quale, per evitare ridondanti ripetizioni, si rimanda a quanto detto nella Parte Speciale n. 5 del presente Modello di Organizzazione, Gestione e Controllo);
- vietare che in tutte le attività aziendali che comportano una selezione di una controparte (principali aree a rischio interessate: Organizzazione di Eventi, Acquisti di Beni e Servizi, Consulenze, Gestione del Personale, Selezione e Gestione degli agenti, Gestione delle Donazioni e Sponsorizzazioni), la scelta sia fondata su motivi razziali, etnici, nazionali o religiosi;
- monitorare i contenuti delle comunicazioni e/o dei documenti promozionali o di marketing di SPA al fine di assicurare che le stesse non contengano propaganda/idee fondate sulla superiorità o sull’odio razziale o etnico, ovvero sull’istigazione a commettere atti di discriminazione/provocazione alla violenza per motivi razziali, etnici, nazionali o religiosi;
- non porre in essere nei confronti di dipendenti comportamenti direttamente o indirettamente discriminatori e/o ritorsivi connessi a motivi razziali, etnici, nazionali o religiosi (a titolo esemplificativo e non esaustivo, promozioni e/o demansionamenti legati esclusivamente a tali ragioni o modifiche ingiustificate delle condizioni contrattuali).
- I FLUSSI INFORMATIVI A FAVORE DELL’ORGANISMO DI VIGILANZA.
Con riferimento alle attività sensibili individuate nei precedenti paragrafi, i Responsabili di Direzione/Divisione nonché tutti i soggetti che esercitano una funzione che prevede la direzione ed il coordinamento di più risorse, devono periodicamente compilare un apposito report avente ad oggetto, tra le altre cose, la segnalazione di eventuali anomalie o irregolarità riscontrate nello svolgimento delle proprie mansioni, la modifica/integrazione/sostituzione di SOP concernenti processi sensibili, i cambiamenti organizzativi intercorsi nell’organigramma societario o il conferimento/revoca di procure e deleghe di funzioni.
Oltre a tali flussi informativi “periodici” tutti i destinatari del presente Modello di Organizzazione e Gestione dovranno poi segnalare tempestivamente all’Organismo di Vigilanza condotte o eventi che potrebbero integrare una violazione e/o elusione del presente Modello o delle SOP in esso richiamate, utilizzando i canali descritti nella parte generale e precisati nella SOP in tema di whistleblowing.
Tali flussi informativi hanno come scopo quello di permettere all’Organismo di Vigilanza della Società di essere informato su potenziali situazioni a rischio reato e di vigilare sull’applicazione del presente Modello di Organizzazione, Gestione e Controllo e del Codice di Comportamento.
Nel caso in cui nel corso della gestione delle attività svolte emergano criticità di qualsiasi natura, il soggetto preposto deve astenersi dal compiere ogni ulteriore atto e ne deve dare immediata informazione, oltre che al superiore gerarchico e agli altri soggetti cui a seconda dei casi fosse doverosa la comunicazione, anche all’Organismo di Vigilanza.
NOTE
[1] Ai fini del presente articolo, costituisce indice di sfruttamento la sussistenza di una o più delle seguenti condizioni:
- la reiterata corresponsione di retribuzioni in modo palesemente difforme dai contratti collettivi nazionali o territoriali stipulati dalle organizzazioni sindacali più rappresentative a livello nazionale, o comunque sproporzionato rispetto alla quantità e qualità del lavoro prestato;
- la reiterata violazione della normativa relativa all’orario di lavoro, ai periodi di riposo, al riposo settimanale, all’aspettativa obbligatoria, alle ferie;
- la sussistenza di violazioni delle norme in materia di sicurezza e igiene nei luoghi di lavoro;
- la sottoposizione del lavoratore a condizioni di lavoro, a metodi di sorveglianza o a situazioni alloggiative degradanti.
[2] La citazione proviene dal Manuale della Qualità adottato da BIOSPA.
